题目内容
2.绿色电源“二甲醚【(CH3)2O】-氧气燃料电池”的工作原理如图所示,下列说法正确的是( )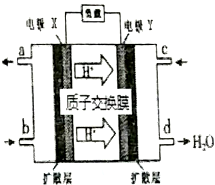
| A. | 氧气应从c处通入,电极Y上发生的反应为:O2+4e-+2H2O═4OH- | |
| B. | 电池在放电过程中,电极X周围溶液的pH增大 | |
| C. | 当该电池向外电路提供2 mol电子时消耗O2约为11.2L | |
| D. | 二甲醚应从b处加入,电极X上发生的反应为:(CH3)2O-12e-+3H2O═2CO2+12H+ |
分析 根据氢离子移动方向知,Y为原电池正极,X为负极,则c处通入的气体是氧气,根据d处生成物知,正极上发生的反应为O2+4e-+4H+═2H2O,电解质溶液为酸性溶液,b处通入的物质是二甲醚,X电极反应式为(CH3)2O-12e-+3H2O=2CO2+12H+,则a处出来的物质是二氧化碳,据此分析解答.
解答 解:根据氢离子移动方向知,Y为原电池正极,X为负极,则c处通入的气体是氧气,根据d处生成物知,正极上发生的反应为O2+4e-+4H+═2H2O,电解质溶液为酸性溶液,b处通入的物质是二甲醚,X电极反应式为(CH3)2O-12e-+3H2O=2CO2+12H+,则a处出来的物质是二氧化碳,
A.氧气应从c处通入,电极Y上发生的反应为O2+4e-+4H+═2H2O,故A错误;
B.电池在放电过程中,电极X发生的电极反应为(CH3)2O-12e-+3H2O=2CO2+12H+,X电极周围溶液的pH减小,故B错误;
C.当该电池向外电路提供2mol电子时消耗O2体积=$\frac{2mol}{4}$×22.4mol/L=11.2L,但是没有说明是在标准状况下,所以无法计算体积,故C错误;
D.二甲醚应从b处加入,X电极上二甲醚得电子发生还原反应,所以电极X上发生的反应为(CH3)2O-12e-+3H2O=2CO2+12H+,故D正确;
故选D.
点评 本题考查了化学电源新型电池,根据氢离子移动方向确定正负极,再根据d处生成物确定电解质溶液酸碱性,难点是电极反应式书写,题目难度中等,侧重于考查学生的分析能力和对基础知识的综合应用能力.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
12.下面是某化学兴趣小组的同学学习元素周期律时设计的两套实验方案.
【实验一】实验步骤如下:
(1)设计该实验方案的目的是:探究同周期元素的性质(或金属性与非金属性)的递变规律.
(2)实验①的现象是生成浅黄色沉淀,反应的化学方程式是Cl2+Na2S=S↓+2NaCl.
【实验二】为验证Cl2、Br2的非金属性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如图.
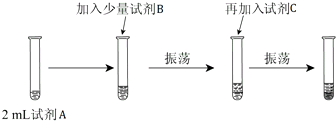
(3)试剂A是NaBr溶液;试剂B是氯水;试剂C是四氯化碳.
(4)试剂C在实验中所起的作用是萃取生成的溴,使现象更明显,
加入C振荡、静置后看到的现象是:液体分成两层,上层接近无色、下层为橙色.
以上反应可以证明Cl2的非金属性强于(填“强于”或“弱于”)Br2的非金属性,反应的离子方程式为:Cl2+2Br-=2Cl-+Br2.
【实验一】实验步骤如下:
| 实验序号 | 实验步骤 |
| ① | 向新制的Na2S溶液中滴加新制的氯水 |
| ② | 将镁条投入1mol/L的稀盐酸中 |
| ③ | 将铝条投入1mol/L的稀盐酸中 |
(2)实验①的现象是生成浅黄色沉淀,反应的化学方程式是Cl2+Na2S=S↓+2NaCl.
【实验二】为验证Cl2、Br2的非金属性强弱,设计了如下实验:(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)实验步骤如图.

(3)试剂A是NaBr溶液;试剂B是氯水;试剂C是四氯化碳.
(4)试剂C在实验中所起的作用是萃取生成的溴,使现象更明显,
加入C振荡、静置后看到的现象是:液体分成两层,上层接近无色、下层为橙色.
以上反应可以证明Cl2的非金属性强于(填“强于”或“弱于”)Br2的非金属性,反应的离子方程式为:Cl2+2Br-=2Cl-+Br2.
13.下列关于浓HNO3与浓H2SO4的叙述正确的是( )
| A. | 常温下都不可用铝制容器贮存 | |
| B. | 常温下都能与铜较快反应 | |
| C. | 露置于空气中,溶液浓度均降低 | |
| D. | 在空气中长期露置,溶液质量均减轻 |
10.下列有关说法不正确的是( )
| A. | 共价键强弱可决定分子晶体的熔、沸点高低 | |
| B. | O2、CO2、N2都是非极性分子 | |
| C. | C3H8中碳原子都采用的是sp3杂化 | |
| D. | CO的一种等电子体为NO+,它的电子式为 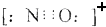 |
17.下列化学用语书写正确的是( )
| A. | 作为相对原子质量标准的原子${\;}_{6}^{14}$C | |
| B. | 氯化镁的电子式: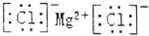 | |
| C. | 用电子式表示氯化氢分子的形成过程: | |
| D. | HClO的结构式为:H-Cl-O |
7.在有机物分子中,当碳原子连有4个不同的原子或原子团时,这种碳原子称为“手性碳原子”.凡具有一个手性碳原子的化合物一定具有光学活性.例如,有机物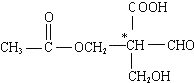 含有一个手性碳原子,具有光学活性,当发生下列化学变化,生成的新有机物仍有光学活性的是( )
含有一个手性碳原子,具有光学活性,当发生下列化学变化,生成的新有机物仍有光学活性的是( )
 含有一个手性碳原子,具有光学活性,当发生下列化学变化,生成的新有机物仍有光学活性的是( )
含有一个手性碳原子,具有光学活性,当发生下列化学变化,生成的新有机物仍有光学活性的是( )| A. | 与NaOH溶液共热 | B. | 与银氨溶液共热 | ||
| C. | 与金属钠反应 | D. | 与氢气发生加成反应 |
14.下列各组化合物中,化学键的类型相同的是( )
| A. | CaCl2和Na2S | B. | Na2O和H2O | C. | CO2和NaCl | D. | HCl和NaOH |
11.下列有关化学用语使用正确的是( )
| A. | 乙烯的结构简式为CH2CH2 | B. | CO2分子的结构式:O=C=O | ||
| C. | 过氧化氢的电子式: | D. | 四氯化碳分子比例模型: |
12.Se是人体必需微量元素,下列关于${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se说法正确的是( )
| A. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se互为同素异形体 | |
| B. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se互为同位素 | |
| C. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se物理性质和化学性质均相同 | |
| D. | ${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se都含有34个中子 |