题目内容
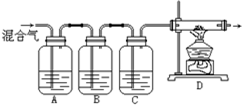 某学生设计一套实验装置如图所示,通过实验除去混在氮气中的氧气、二氧化碳、硫化氢和乙烯等气体,制得干燥的氮气.
某学生设计一套实验装置如图所示,通过实验除去混在氮气中的氧气、二氧化碳、硫化氢和乙烯等气体,制得干燥的氮气.(1)分别指出A、B、C、D四处装置中应加入的试剂和所要除去的杂质:
| A | B | C | D | |
| 应加试剂 | ||||
| 所除杂质 |
考点:物质分离和提纯的方法和基本操作综合应用,实验装置综合
专题:实验设计题
分析:由实验装置可知,除去混在氮气中的氧气、二氧化碳、硫化氢和乙烯等气体,则A为高锰酸钾除去乙烯、硫化氢,B为NaOH吸收二氧化碳,C为浓硫酸可吸收水,D中灼热的铁粉可除去氧气,则最后收集到干燥的氮气;图中A、B两瓶可分别选择溴的四氯化碳溶液、NaOH溶液也可除去,以此来解答.
解答:
解:(1)因乙烯、硫化氢能被氧化,二氧化碳能被碱吸收,则A为高锰酸钾除去乙烯、硫化氢,B为NaOH吸收二氧化碳,C为浓硫酸可吸收水,D中灼热的铁粉可除去氧气,则最后收集到干燥的氮气,故答案为:
(2)A、B两瓶中的试剂可有多种选择和组合,如A瓶中盛溴的四氯化碳溶液以除去乙烯,B瓶盛氢氧化钠溶液以除去二氧化碳和硫化氢,A瓶的有关反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br,故答案为:A瓶中盛溴的四氯化碳溶液以除去乙烯,B瓶盛氢氧化钠溶液以除去二氧化碳和硫化氢;CH2=CH2+Br2→CH2BrCH2Br.
| A | B | C | D | |
| 应加试剂 | 高锰酸钾溶液 | 氢氧化钠溶液 | 浓硫酸 | 铁粉 |
| 所除杂质 | 乙烯、硫化氢 | 二氧化碳 | 水蒸气 | 氧气 |
点评:本题考查混合物分离提纯的综合应用,为高频考点,把握实验装置的作用、物质的性质为解答的关键,侧重分析与实验能力的综合考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
有两个无标签的试剂瓶,分别装有Na2CO3和NaHCO3,有四位同学为鉴别它们,采用了以下不同方法,其中可行的是( )
| A、分别配成溶液,再通入CO2 |
| B、分别配成溶液,再加入Ca(OH)2溶液 |
| C、分别加热,用澄清石灰水检验是否有气体产生 |
| D、分别配成溶液,再进行焰色反应 |
已知氮的氧化物跟NaOH溶液发生的化学反应如下:
2NO2+2NaOH═NaNO3+NaNO2+H2O
NO2+NO+2NaOH═2NaNO2+H2O
现有m mol NO2和n mol NO组成的混合气体,要用NaOH溶液使其完全吸收无气体剩余,现有浓度为a mol?L-1 的NaOH溶液,则需此NaOH溶液的体积是( )
2NO2+2NaOH═NaNO3+NaNO2+H2O
NO2+NO+2NaOH═2NaNO2+H2O
现有m mol NO2和n mol NO组成的混合气体,要用NaOH溶液使其完全吸收无气体剩余,现有浓度为a mol?L-1 的NaOH溶液,则需此NaOH溶液的体积是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
常温下Ksp(AgCl)=1.56×10-10,Ksp(AgI)=1.0×10-16,将等体积的AgCl和AgI的饱和溶液的清夜混合,再向其中加入一定量的AgNO3固体,下列说法正确的是( )
| A、两清夜混合,AgCl和AgI都沉淀 |
| B、向AgCl清夜加入AgNO3固体,c(Ag+)增大,Ksp(AgCl)也增大 |
| C、若AgNO3固体足量,AgCl和AgI都可沉淀,但以AgCl沉淀为主 |
| D、若取0.235克AgI固体放入100ml(忽略体积变化),c(I-)=0.01mol/l |