题目内容
12.我国新修订的《环境保护法》已于2015年1月1日起施行,体现了加强生态文明建设的新要求.①排放下列气体不利于蓝天出现的是a(填字母)
a.NO2b.N2c.CO2
②含有下列离子的废水不需要处理就可排放的是ca.Cr2O72-b.Pb2+c.Ca2+
③汽车尾气中的CO和NO在催化剂的作用下可转化为无害气体,化学方程式为2CO+2NO $\frac{\underline{\;\;△\;\;}}{\;}$ N2+2CO2.
分析 ①二氧化氮有毒,容易造成光化学烟雾;
②含有重金属离子的水有毒,不能直接排放;
③汽车尾气中的CO和NO在催化剂的作用下可转化为无害气体是氮气和二氧化碳,化学方程式为
解答 解:①二氧化氮有毒,容易造成光化学烟雾;氮气、二氧化碳不是污染物;
故选:a;
②Cr2O72- 和Pb2+,都是重金属离子,能引起污染;
故选:c;
③汽车尾气中的CO和NO在催化剂的作用下可转化为无害气体是氮气和二氧化碳,所以化学方程式为2CO+2NO $\frac{\underline{\;\;△\;\;}}{\;}$ N2+2CO2,故答案为:2CO+2NO $\frac{\underline{\;\;△\;\;}}{\;}$ N2+2CO2.
点评 本题考查了生活中常见的污染和治理,熟悉相关知识是解题关键,题目难度不大,注意对相关内容的积累.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
2.将5mL 10mol/L的硫酸稀释到100mL,所得硫酸溶液的物质的量浓度是( )
| A. | 0.2 mol/L | B. | 0.5 mol/L | C. | 2 mol/L | D. | 5mol/L |
3.下列表述中合理的是( )
| A. | 在101kPa下,1g物质完全燃烧所放出的热量叫做该物质的热值 | |
| B. | 把FeCl3的水溶液加热蒸干可得到FeCl3固体 | |
| C. | 用25mL碱式滴定管量取20.00mL高锰酸钾溶液 | |
| D. | 太阳能电池是把太阳能转化为内能的装置 |
7.用酸式滴定管准确移取10.00mL某未知浓度的盐酸溶于一洁净的锥形瓶中,然后用0.20mol•L -1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
(1)根据以上数据可以计算出盐酸的物质的量浓度为0.364mol•L-1.
(2)达到滴定终点的标志是无色变为红色,且30s内不变色.
(3)以下操作造成测定结果偏高的原因可能是AD.
A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液.
| NaOH起始读数 | NaOH终点读数 | |
| 第一次 | 0.50mL | 18.60mL |
| 第二次 | 0.70mL | 19.00mL |
(2)达到滴定终点的标志是无色变为红色,且30s内不变色.
(3)以下操作造成测定结果偏高的原因可能是AD.
A.未用标准液润洗碱式滴定管
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液.
17.实验室中需要配制2mol/L的NaOH溶液850mL,配制时应选用的容量瓶的规格和称取的NaOH的质量分别是( )
| A. | 950 mL,76 g | B. | 500 mL,80 g | C. | 1000 mL,80 g | D. | 1000 mL,76 g |
4.第四周期过渡元素常与H2O、NH3、CN-等形成配合物.
(1)Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,形成配位数为6的配合物,写出该配合物的化学式K4[Fe(CN)6].
(2)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,为do或d10排布时,无颜色;为d1一d9排布时,有颜色,如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]2+有颜色(填“无”或“有”).[Mn(H2O)6]2+配离子中存在的化学键有CD (填标号)
A.金属键 B.离子键 C.共价键 D.配位键
(3)H2S和H2O2的主要物理性质比较如表:
①H2O2分子中O原子采取sp3杂化,写出H2O2的电子式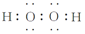
②H2S和H2O2的相对分子质量相同,造成沸点差异的主要原因是H2O2分子间形成氢键;造成溶解度差异的主要原因是H2O2分子与H2O分子间形成氢键.
(1)Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,形成配位数为6的配合物,写出该配合物的化学式K4[Fe(CN)6].
(2)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,为do或d10排布时,无颜色;为d1一d9排布时,有颜色,如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]2+有颜色(填“无”或“有”).[Mn(H2O)6]2+配离子中存在的化学键有CD (填标号)
A.金属键 B.离子键 C.共价键 D.配位键
(3)H2S和H2O2的主要物理性质比较如表:
| 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 202 | 2.6 |
| H2O2 | 423 | 以任意比互溶 |
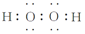
②H2S和H2O2的相对分子质量相同,造成沸点差异的主要原因是H2O2分子间形成氢键;造成溶解度差异的主要原因是H2O2分子与H2O分子间形成氢键.
1.图各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )


| A. | ③>②>④>① | B. | ④>②>①>③ | C. | ②>①>③>④ | D. | ④>②>③>① |
15. 2SO2(g)+2O2(g)?2SO3(g)是生产硫酸的主要反应之一.下表是原料气按V(SO2):V(O2):V(N2)=7:11:82投料,在1.01×105Pa时,不同温度下SO2的平衡转化率.
2SO2(g)+2O2(g)?2SO3(g)是生产硫酸的主要反应之一.下表是原料气按V(SO2):V(O2):V(N2)=7:11:82投料,在1.01×105Pa时,不同温度下SO2的平衡转化率.
(1)该反应是放热反应(填“放热”或“吸热”).
(2)400℃,1.01×105Pa时,将含10 mol SO2的原料气通入一密闭容器中进行反应,平衡时SO2的物质的量是0.08mol.
(3)硫酸厂尾气(主要成分SO2、O2和N2)中低浓度SO2的吸收有很多方法.
①用氨水吸收上述尾气,若SO2与氨水恰好反应得到碱性的(NH4)2SO3溶液时,则有关该溶液的下列关系正确的是ac(填序号).
a. c(NH4+)+c(NH3•H2O)=2[c(SO32-)+c(HSO3-)+c(H2SO3)]
b. c(NH4+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
c. c(NH4+)>c(SO32-)>c(OH-)>c(H+)
②用 MnO2与水的悬浊液吸收上述尾气并生产MnSO4.
a. 得到MnSO4的化学方程式是H2O+SO2=H2SO3、MnO2+H2SO3=MnSO4+H2O.
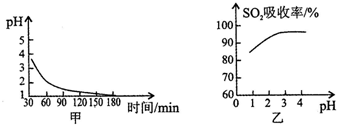
b.该吸收过程生成MnSO4时,溶液的pH变化趋势如图甲,SO2吸收率与溶液pH的关系如图乙. 图甲中pH变化是因为吸收中有部分SO2被氧气氧化转化为H2SO4,生成H2SO4反应的化学方程式是2SO2+O2+2H2O=2H2SO4;由图乙可知pH的降低不利于SO2的吸收(填“有利于”或“不利于”),用化学平衡移动原理解释其原因是溶液中存在SO2+H2O?H2SO3?H++HSO3-,当溶液中酸性增强,平衡向左移动,使SO2气体从体系中逸出..
 2SO2(g)+2O2(g)?2SO3(g)是生产硫酸的主要反应之一.下表是原料气按V(SO2):V(O2):V(N2)=7:11:82投料,在1.01×105Pa时,不同温度下SO2的平衡转化率.
2SO2(g)+2O2(g)?2SO3(g)是生产硫酸的主要反应之一.下表是原料气按V(SO2):V(O2):V(N2)=7:11:82投料,在1.01×105Pa时,不同温度下SO2的平衡转化率.| 温度/ | 400 | 500 | 600 |
| SO2转化率/% | 99.2 | 93.5 | 73.7 |
(2)400℃,1.01×105Pa时,将含10 mol SO2的原料气通入一密闭容器中进行反应,平衡时SO2的物质的量是0.08mol.
(3)硫酸厂尾气(主要成分SO2、O2和N2)中低浓度SO2的吸收有很多方法.
①用氨水吸收上述尾气,若SO2与氨水恰好反应得到碱性的(NH4)2SO3溶液时,则有关该溶液的下列关系正确的是ac(填序号).
a. c(NH4+)+c(NH3•H2O)=2[c(SO32-)+c(HSO3-)+c(H2SO3)]
b. c(NH4+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
c. c(NH4+)>c(SO32-)>c(OH-)>c(H+)
②用 MnO2与水的悬浊液吸收上述尾气并生产MnSO4.
a. 得到MnSO4的化学方程式是H2O+SO2=H2SO3、MnO2+H2SO3=MnSO4+H2O.
b.该吸收过程生成MnSO4时,溶液的pH变化趋势如图甲,SO2吸收率与溶液pH的关系如图乙. 图甲中pH变化是因为吸收中有部分SO2被氧气氧化转化为H2SO4,生成H2SO4反应的化学方程式是2SO2+O2+2H2O=2H2SO4;由图乙可知pH的降低不利于SO2的吸收(填“有利于”或“不利于”),用化学平衡移动原理解释其原因是溶液中存在SO2+H2O?H2SO3?H++HSO3-,当溶液中酸性增强,平衡向左移动,使SO2气体从体系中逸出..