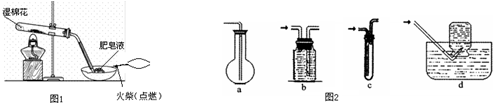
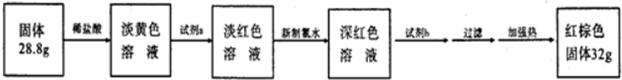
题目内容
4.下列离子方程式书写正确的是( )| A. | Na投入到水中:Na+H2O═Na++OH-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O | |
| C. | 三氯化铁溶液中加入铜粉:Fe3++Cu═Fe2++Cu2+ | |
| D. | 将氯气通入冷的氢氧化钠溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
分析 A.原子个数不守恒;
B.不符合反应客观事实;
C.电荷不守恒;
D.二者反应生成氯化钠、次氯酸钠和水.
解答 解:A.Na投入到水中,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.AlCl3溶液中加入足量的氨水反应生成氢氧化铝沉淀和氯化铵,离子方程式:Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故B错误;
C.三氯化铁溶液中加入铜粉,离子方程式:2Fe3++Cu═2Fe2++Cu2+,故C错误;
D.将氯气通入冷的氢氧化钠溶液中二者反应生成氯化钠、次氯酸钠和水,离子方程式:Cl2+2OH-═Cl-+ClO-+H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应的实质是解题关键,离子方程式书写应遵循客观规律、遵循电荷守恒、原子个数守恒规律,题目难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
14.某校化学兴趣小组采用酸碱中和滴定法测定学校新购入的烧碱的纯度(烧碱中含有不与酸反应的杂质),试根据实验回答.
(1)实验步骤为:①用托盘天平准确称量4.1g烧碱样品.
②将样品配成250ml待测液,需要的仪器除玻璃棒、量筒、烧杯外还需要的玻璃仪器有250ml容量瓶,胶头滴管.
③用碱式滴定管量取10.00ml待测液,注入锥形瓶中.
④在锥形瓶中滴入2~3滴酚酞或甲基橙(填指示剂),用0.2010mol/L的标准盐酸滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色的变化,直到滴定终点.
(2)该小组测得下列数据
根据上述数据,计算烧碱的纯度98%.
(1)实验步骤为:①用托盘天平准确称量4.1g烧碱样品.
②将样品配成250ml待测液,需要的仪器除玻璃棒、量筒、烧杯外还需要的玻璃仪器有250ml容量瓶,胶头滴管.
③用碱式滴定管量取10.00ml待测液,注入锥形瓶中.
④在锥形瓶中滴入2~3滴酚酞或甲基橙(填指示剂),用0.2010mol/L的标准盐酸滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视锥形瓶内溶液颜色的变化,直到滴定终点.
(2)该小组测得下列数据
| 滴定次数 | 待测液体积/ml | 标准盐酸体积/ml | |
| 滴定前读数/ml | 滴定后读数/ml | ||
| 第一次 | 10.00 | 0.20 | 22.90 |
| 第二次 | 10.00 | 0.50 | 20.40 |
| 第三次 | 10.00 | 4.00 | 24.10 |
| 第四次 | 10.00 | 0.00 | 20.00 |
15.已知常温下,溶液中能发生如下反应:①2R-+Z2=R2+2Z-②16H++10Z-+2XO4-=2X2++5Z2+8H2O③2M2++2R2=2M3++2R-由此判断,下列说法中正确的是( )
| A. | Z2+2M2+=2 M3++2Z-不可以进行 | |
| B. | Z元素在①②反应中发生还原反应 | |
| C. | 各粒子还原性由强到弱的顺序是X2+>Z->R->M2+ | |
| D. | 各粒子氧化性由强到弱的顺序是XO4->Z2>R2>M3+ |
19.下面有关氧化还原反应的叙述正确的是( )
| A. | 在反应中不一定所有元素的化合价都发生变化 | |
| B. | 肯定有一种元素被氧化,另一种元素被还原 | |
| C. | 非金属单质在反应中只做氧化剂 | |
| D. | 某元素从化合物变为单质时,该元素一定被还原 |
9.下列叙述不正确的是( )
| A. | 异戊二烯分子里的所有原子不可能在同一平面上 | |
| B. | 浓氨水洗涤做过银镜反应的试管 | |
| C. | 油脂皂化反应得到高级脂肪酸盐与甘油 | |
| D. | 聚合物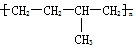 可由单体CH3CH=CH2和CH2=CH2加聚制得 可由单体CH3CH=CH2和CH2=CH2加聚制得 |
16.需要加入氧化剂才能实现的变化是( )
| A. | MnO2→MnSO4 | B. | KI→KIO3 | C. | HNO 3→NO | D. | Al2O 3→Al(OH)3 |
13. 25℃时,三种酸的电离平衡常数如表:
25℃时,三种酸的电离平衡常数如表:
(1)常温下,若三者体积均为200mL 浓度均为0.1mol•L-1,则三者中C(H+)最小的是次氯酸(填名称).
(2)相同条件下,体积均为200mL、浓度均为0.1mol•L-1的CH3COOH(aq)和HCl(aq)分别与100mL 0.2mol•L-1NaOH溶液反应,放出热量较少的是醋酸 (填名称).
(3)下列四种离子结合质子能力由大到小的顺序是a>b>d>c(填序号).
a.CO32-b.ClO- c.CH3COO-d.HCO3-
(4)向次氯酸钠溶液中通入少量二氧化碳,写出该过程中反应的离子方程式:ClO-+CO2+H2O=HCO3-+HClO.
(5)在一定温度下,有 a.盐酸 b.硫酸 c.醋酸三种酸,当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌粒,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为a=b=c(填序号),反应所需时间的长短关系是a=b>c(填序号).
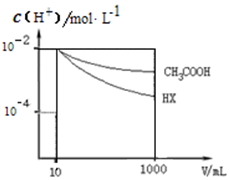
(6)相同条件下,体积均为10mL、c(H+)为0.01mol•L-1的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中c(H+)变化如图所示.
则HX的电离平衡常大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数.
 25℃时,三种酸的电离平衡常数如表:
25℃时,三种酸的电离平衡常数如表:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
(2)相同条件下,体积均为200mL、浓度均为0.1mol•L-1的CH3COOH(aq)和HCl(aq)分别与100mL 0.2mol•L-1NaOH溶液反应,放出热量较少的是醋酸 (填名称).
(3)下列四种离子结合质子能力由大到小的顺序是a>b>d>c(填序号).
a.CO32-b.ClO- c.CH3COO-d.HCO3-
(4)向次氯酸钠溶液中通入少量二氧化碳,写出该过程中反应的离子方程式:ClO-+CO2+H2O=HCO3-+HClO.
(5)在一定温度下,有 a.盐酸 b.硫酸 c.醋酸三种酸,当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌粒,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为a=b=c(填序号),反应所需时间的长短关系是a=b>c(填序号).
(6)相同条件下,体积均为10mL、c(H+)为0.01mol•L-1的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中c(H+)变化如图所示.
则HX的电离平衡常大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数.