题目内容
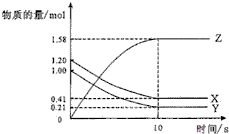 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述错误的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述错误的是( )| A、达到平衡所需要的时间是10s |
| B、平衡时Y的转化率79.0% |
| C、该反应的化学方程式为X(g)+Y(g)?2Z(g) |
| D、前10s,用Z表示的反应速率为0.79mol/(L?s) |
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:根据图象的曲线变化判断物质的量的变化进而判断反应平衡所需时间以及反应速率、转化率的计算,根据参加反应的物质的物质的量之比等于化学计量数之比书写化学方程式.
解答:
解:A.根据图象可知在10s后,X、Y、Z的物质的量不再随时间的变化而变化,即反应达到平衡状态,故A正确;
B.反应开始到10s时,Y的转化率为
=79%,故B正确;
C.由图象可以看出,反应中x、Y的物质的量减少,应为反应物,z的物质的量增多,应为生成物,
当反应进行到3min时,△n(X)=0.79mol,△n(Y)=0.79mol,△n(Z)=1.58mol,
则△n(X):△n(Y):△n(Z)=1:1:2,参加反应的物质的物质的量之比等于化学计量数之比,
则反应的方程式为X(g)+Y(g)?2Z(g),故C正确;
D.反应开始到10s,用Z表示的反应速率
=0.079mol/(L?s),故D错误;
故答案为D.
B.反应开始到10s时,Y的转化率为
| 1.0mol-0.21mol |
| 1.0mol |
C.由图象可以看出,反应中x、Y的物质的量减少,应为反应物,z的物质的量增多,应为生成物,
当反应进行到3min时,△n(X)=0.79mol,△n(Y)=0.79mol,△n(Z)=1.58mol,
则△n(X):△n(Y):△n(Z)=1:1:2,参加反应的物质的物质的量之比等于化学计量数之比,
则反应的方程式为X(g)+Y(g)?2Z(g),故C正确;
D.反应开始到10s,用Z表示的反应速率
| ||
| 10s |
故答案为D.
点评:本题考查化学平衡图象问题,题目难度不大,注意分析图象中各物理量的变化曲线,把握相关物理量的计算.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
生活中遇到的某些问题,常常涉及到化学知识,下列各项叙述不正确的是( )
| A、鱼虾会产生不愉快的腥臭味,可在烹调时加入少量食醋和料酒 |
| B、“酸可以除锈”,“汽油可以去油污”都是发生了化学变化 |
| C、被蜂蚁蜇咬会感觉疼痛难忍,这是由于人的皮肤被注入了甲酸的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 |
| D、居室空气污染的主要来源之一是人们使用的装饰材料、胶合板、内墙涂料会释放出一种刺激性气味的气体,它对人体极为有害,该气体是甲醛. |
增大反应物的浓度、增大气体的压强、升高体系的温度、使用催化剂都可以加快化学反应速率,其中能增大活化分子百分数的是( )
①增大反应物的浓度②增大气体的压强③升高体系的温度④使用催化剂.
①增大反应物的浓度②增大气体的压强③升高体系的温度④使用催化剂.
| A、①② | B、②③ | C、①④ | D、③④ |
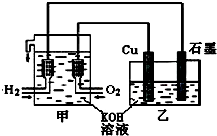 利用如图装置制取Cu2O,乙的总反应化学方程式为:2Cu+H2O=Cu2O+H2↑.下列说法正确的是( )
利用如图装置制取Cu2O,乙的总反应化学方程式为:2Cu+H2O=Cu2O+H2↑.下列说法正确的是( )| A、乙中Cu电极的电极反应式是:2Cu+2OH--2e-=Cu2O+H2O |
| B、甲中通入氧气的电极为负极 |
| C、乙中阴离子向石墨电极移动 |
| D、电路上通过0.5mol电子,可制得0.5mol Cu2O |
下列化学用语的描述正确的是( )
| A、氨水显碱性:NH3?H2O═NH4++OH- |
| B、Na2S溶液显碱性:S2-+2H2O?H2S+2OH- |
| C、硫酸氢钠溶液显酸性:NaHSO4═Na++H++SO42- |
| D、AlCl3溶液显酸性:Al3++3H2O?Al(OH)3↓+3H+ |
下列说法错误的是( )
| A、含有共价键的化合物不一定是共价化合物 |
| B、在共价化合物中一定含有共价键 |
| C、含有离子键的化合物一定是离子化合物 |
| D、离子键就是阴阳离子结合成化合物的静电引力 |
已知单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点就越高.则下列溶液沸点最高的是( )
| A、0.01 mol?L-1的蔗糖溶液 |
| B、0.01 mol?L-1的CaCl2溶液 |
| C、0.01 mol?L-1的NaCl溶液 |
| D、0.02 mol?L-1的CH3COOH溶液 |
工业酒精与用粮食发酵产生的酒精成份不完全相同.严禁用工业酒精勾兑食用酒,否则会使人双目失明甚至死亡.工业酒精中的主要有毒成份是( )
| A、甲醇 | B、甲醛 | C、甲酸 | D、甲苯 |