题目内容
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统
产生很大的伤害,必须进行处理.该法的工艺流程为CrO4-2
Cr2O72-
Cr3+
Cr(OH)3↓
其中第①步存在平衡:2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显色.
(2)能说明第①步反应达平衡状态的是 .(选填编号)
a.Cr2O72-和CrO42-的浓度相同 b.v正 (Cr2O72-)=2v逆(CrO42-)
c.溶液的颜色不变d.溶液的pH值不变
(3)写出第②步中Cr2O72-转变为Cr3+的离子方程式: .
(4)向Cr2(SO4)3溶液中,滴加NaOH,当pH=4.6时,开始出现Cr(OH)3沉淀,随着pH的-H2O
升高,沉淀增多,但当pH≥13时,沉淀消失,出现亮绿色的[Cr(OH)4]-离子.其平衡关系如
+H2O下:H++[Cr(OH)4]-(亮绿色)?Cr(OH)3(s,灰绿色)?Cr3+(紫色)+3OH-.
现向0.05mol?L-1的Cr2(SO4)3溶液50mL中,加入等体积0.6mol?L-1的NaOH溶液,充分反应后,溶液中可观察到的现象为 ,溶液中离子浓度由大到小的顺序为 .
(5)在Na[Cr(OH)4]和Na2Cr2O7混合后的溶液中加入H2SO4酸化,铬元素以 形式存在(填写离子符号).
产生很大的伤害,必须进行处理.该法的工艺流程为CrO4-2
| H+ |
| ①转化 |
| Fe2+ |
| ②还原 |
| OH- |
| ③沉淀 |
其中第①步存在平衡:2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=2,则溶液显色.
(2)能说明第①步反应达平衡状态的是
a.Cr2O72-和CrO42-的浓度相同 b.v正 (Cr2O72-)=2v逆(CrO42-)
c.溶液的颜色不变d.溶液的pH值不变
(3)写出第②步中Cr2O72-转变为Cr3+的离子方程式:
(4)向Cr2(SO4)3溶液中,滴加NaOH,当pH=4.6时,开始出现Cr(OH)3沉淀,随着pH的-H2O
升高,沉淀增多,但当pH≥13时,沉淀消失,出现亮绿色的[Cr(OH)4]-离子.其平衡关系如
+H2O下:H++[Cr(OH)4]-(亮绿色)?Cr(OH)3(s,灰绿色)?Cr3+(紫色)+3OH-.
现向0.05mol?L-1的Cr2(SO4)3溶液50mL中,加入等体积0.6mol?L-1的NaOH溶液,充分反应后,溶液中可观察到的现象为
(5)在Na[Cr(OH)4]和Na2Cr2O7混合后的溶液中加入H2SO4酸化,铬元素以
考点:化学平衡状态的判断,化学平衡的影响因素
专题:化学平衡专题
分析:(1)根据外界条件对平衡的影响来确定平衡移动方向,从而确定离子浓度大小和溶液颜色变化;
(2)根据判断平衡状态的方法:V正=V逆,或各组分的浓度保持不变则说明已达平衡,也可根据化学平衡状态的特征:逆、定、动、变、等来回答判断;
(3)在酸性条件下与来亚铁离子发生氧化还原反应;
(4)根据Cr3++4OH-=CrO22-+2H2O计算反应后剩余的n(OH-),进而计算c(OH-),再根据Kw=c(H+)?c(OH-)计算c(H+),最后利用pH=-lgc(H+)计算pH值进行判断,根据反应后相关离子的物质的比较离子浓度的大小;
(5)在酸性条件下H++[Cr(OH)4]-(亮绿色)?Cr(OH)3(s,灰绿色)?Cr3+(紫色)+3OH-,平衡正向移动,平衡2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O也正向移动.
(2)根据判断平衡状态的方法:V正=V逆,或各组分的浓度保持不变则说明已达平衡,也可根据化学平衡状态的特征:逆、定、动、变、等来回答判断;
(3)在酸性条件下与来亚铁离子发生氧化还原反应;
(4)根据Cr3++4OH-=CrO22-+2H2O计算反应后剩余的n(OH-),进而计算c(OH-),再根据Kw=c(H+)?c(OH-)计算c(H+),最后利用pH=-lgc(H+)计算pH值进行判断,根据反应后相关离子的物质的比较离子浓度的大小;
(5)在酸性条件下H++[Cr(OH)4]-(亮绿色)?Cr(OH)3(s,灰绿色)?Cr3+(紫色)+3OH-,平衡正向移动,平衡2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O也正向移动.
解答:
解:(1)c(H+)增大,平衡2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O右移,溶液呈橙色,故答案为:橙;
(2)2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O
a.Cr2O72-和CrO42-的浓度相同,不一定平衡,故a错误;
b.CrO42-的消耗速率表示v正,Cr2O72-生成速率也表示v正,从开始到平衡2v证(CrO42-)=v正(Cr2O72-)不是平衡状态,故b错误;
c.溶液的颜色不变,证明各组分的浓度不随时间的变化而变化,故c正确;
d.溶液的pH值不变,即溶液的酸性不变,氢离子浓度不变,达到了化学平衡状态,故d正确;
故选cd;
(3)在酸性条件下与来亚铁离子发生氧化还原反应,反应方程式为Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,故答案为:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O;
(4)n(Cr3+)=0.1 mol/L×0.05 L=0.005 mol
Cr3++4OH-=CrO22-+2H2O
0.005mol 0.02 mol
剩余n(OH-)=0.6mol/L×0.05L-0.02 mol=0.01 mol,
使用c(OH-)=
=0.1 mol/L,
所以c(H+)=
mol/L=10-13 mol/L,
故pH=-lg10-13=13,所以此时溶液中主要以[Cr(OH)4]-形式存在,溶液由紫色变为亮绿色;溶液中c(Na+)=
=0.3mol/L,c(OH-)=0.1 mol/L,
c(SO42-)=
=0.075mol/L,所以离子浓度大小关系为:c(Na+)>c(OH-)>c(SO42-)>c([Cr(OH)4]-)>c(H+),故答案为:溶液由紫色变为亮绿色;c(Na+)>c(OH-)>c(SO42-)>c([Cr(OH)4]-)>c(H+);
(5)在酸性条件下H++[Cr(OH)4]-(亮绿色)?Cr(OH)3(s,灰绿色)?Cr3+(紫色)+3OH-,平衡正向移动,平衡2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O也正向移动,所以铬元素以Cr3+、Cr2O72-的形式存在,故答案为:Cr3+、Cr2O72-.
(2)2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O
a.Cr2O72-和CrO42-的浓度相同,不一定平衡,故a错误;
b.CrO42-的消耗速率表示v正,Cr2O72-生成速率也表示v正,从开始到平衡2v证(CrO42-)=v正(Cr2O72-)不是平衡状态,故b错误;
c.溶液的颜色不变,证明各组分的浓度不随时间的变化而变化,故c正确;
d.溶液的pH值不变,即溶液的酸性不变,氢离子浓度不变,达到了化学平衡状态,故d正确;
故选cd;
(3)在酸性条件下与来亚铁离子发生氧化还原反应,反应方程式为Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,故答案为:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O;
(4)n(Cr3+)=0.1 mol/L×0.05 L=0.005 mol
Cr3++4OH-=CrO22-+2H2O
0.005mol 0.02 mol
剩余n(OH-)=0.6mol/L×0.05L-0.02 mol=0.01 mol,
使用c(OH-)=
| 0.01mol |
| 0.05L+0.05L |
所以c(H+)=
| 10-14 |
| 0.1 |
故pH=-lg10-13=13,所以此时溶液中主要以[Cr(OH)4]-形式存在,溶液由紫色变为亮绿色;溶液中c(Na+)=
| 0.6mol?L-1 |
| 2 |
c(SO42-)=
| 3×0.05mol?L-1 |
| 2 |
(5)在酸性条件下H++[Cr(OH)4]-(亮绿色)?Cr(OH)3(s,灰绿色)?Cr3+(紫色)+3OH-,平衡正向移动,平衡2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O也正向移动,所以铬元素以Cr3+、Cr2O72-的形式存在,故答案为:Cr3+、Cr2O72-.
点评:本题主要考查了化学平衡移动原理、氧化还原反应、沉淀溶解平衡等内容,解题须根据题给信息结合相关原理进行解答,题目难度中等.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
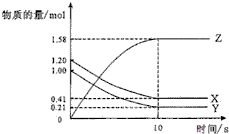 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述错误的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述错误的是( )| A、达到平衡所需要的时间是10s |
| B、平衡时Y的转化率79.0% |
| C、该反应的化学方程式为X(g)+Y(g)?2Z(g) |
| D、前10s,用Z表示的反应速率为0.79mol/(L?s) |
下列说法正确的是( )


| A、图I所示装置用于Cu和浓H2SO4制取少量的SO2气体 |
| B、图Ⅱ装置可验证非金属性:Cl>C>Si |
| C、图Ⅲ可用于收集气体H2、CO2、Cl2、NH3 |
| D、图Ⅳ表示将SO2气体通入溴水中,所得溶液的pH变化 |
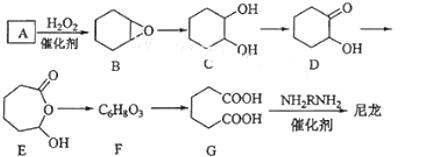
 利用太阳能分解水产生H2,在催化剂作用下H2与CO2反应合成CH3OH,并开发出直接以甲醇为燃料的燃料电池.已知:
利用太阳能分解水产生H2,在催化剂作用下H2与CO2反应合成CH3OH,并开发出直接以甲醇为燃料的燃料电池.已知: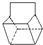 )是双环戊二烯的一种同分异构体,它的一氯代物有
)是双环戊二烯的一种同分异构体,它的一氯代物有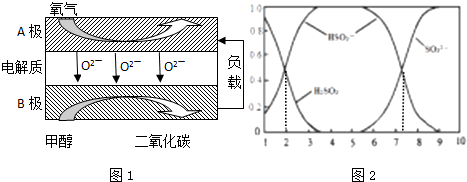
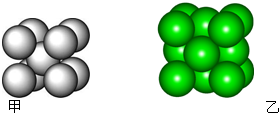 某金属晶体M有两种堆积形式,如图甲和乙,在T℃以上时甲可以转变为乙,这两种结构中最邻近的原子间距离相同.
某金属晶体M有两种堆积形式,如图甲和乙,在T℃以上时甲可以转变为乙,这两种结构中最邻近的原子间距离相同.