题目内容
下列说法错误的是( )
| A、含有共价键的化合物不一定是共价化合物 |
| B、在共价化合物中一定含有共价键 |
| C、含有离子键的化合物一定是离子化合物 |
| D、离子键就是阴阳离子结合成化合物的静电引力 |
考点:化学键,离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:A.共价键可存在于离子化合物中;
B.共价化合物中不能含离子键;
C.含离子键的一定为离子化合物;
D.离子键为阴阳离子之间的作用力.
B.共价化合物中不能含离子键;
C.含离子键的一定为离子化合物;
D.离子键为阴阳离子之间的作用力.
解答:
解:A.共价键可存在于离子化合物中,如NaOH中含离子键和共价键,故A正确;
B.共价化合物中不能含离子键,则共价化合物中一定含共价键,故B正确;
C.含离子键的一定为离子化合物,且离子化合物中可能含共价键,故C正确;
D.离子键为阴阳离子之间的作用力,既有静电引力,也有静电排斥,故D错误;
故选D.
B.共价化合物中不能含离子键,则共价化合物中一定含共价键,故B正确;
C.含离子键的一定为离子化合物,且离子化合物中可能含共价键,故C正确;
D.离子键为阴阳离子之间的作用力,既有静电引力,也有静电排斥,故D错误;
故选D.
点评:本题考查化学键,为高频考点,把握化学键与化合物类别的关系为解答的关键,注意利用实例分析,明确含离子键的一定为离子化合物,题目难度不大.

练习册系列答案
相关题目
下列各组物质均为同系物的是( )
①
②
③CH4与C3H8
④1-丁烯与2-甲基丙烯
⑤CH3CH2COOH与CH3COOH
⑥乙醇与乙二醇.
①

②

③CH4与C3H8
④1-丁烯与2-甲基丙烯
⑤CH3CH2COOH与CH3COOH
⑥乙醇与乙二醇.
| A、①④⑤ | B、①④⑥ |
| C、②③⑤ | D、④⑤⑥ |
设NA为阿伏加德罗常数的值.下列叙述不正确的是( )
| A、一定温度下,15g甲醛和乙酸的混合物中O原子数为0.5NA |
| B、标准状况下,NO和O2各11.2L混合,所得混合气体的分子总数为0.75NA |
| C、14g分子通式为CnH2n的链烃中含有的C=C的数目为NA/n |
| D、在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A、在0.1 mol/L NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| B、在0.1 mol/L Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3) |
| C、向0.2mol/LNaHCO3溶液中加入等体积0.1 mol/LNaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、0.2 mol/L的NaHCO3溶液中c(H+)+c(H2CO3)=c(CO32-)+c(OH-) |
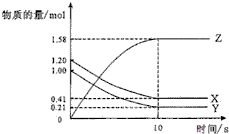 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述错误的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述错误的是( )| A、达到平衡所需要的时间是10s |
| B、平衡时Y的转化率79.0% |
| C、该反应的化学方程式为X(g)+Y(g)?2Z(g) |
| D、前10s,用Z表示的反应速率为0.79mol/(L?s) |
对于学生来讲,“学会生存”比学习知识更重要.下列叙述错误的是( )
| A、快速逃离火灾现场时,应用湿毛巾捂口鼻弯腰呼吸,因为许多易燃有机高分子材料燃烧时会释放出大量有毒气体,而且热气体的密度比空气轻 |
| B、吃米饭或馒头时,多加咀嚼会感到甜味,是因为淀粉发生水解反应生成了麦芽糖 |
| C、油脂是人类的主要食物之一,“地沟油”对人体的危害极大 |
| D、肥皂的去污原理与合成洗涤剂的去污原理不同 |
实验室可提供下列实验操作:①滴加AgNO3溶液;②加NaOH溶液;③加热;④加催化剂MnO2;⑤加蒸馏水过滤后取滤液;⑥过滤后取滤渣;⑦用HNO3酸化.如要鉴定1-氯丙烷中的氯元素,从中选择合适的操作步骤是( )
| A、③⑤⑦① | B、②③⑦① |
| C、②⑤⑦① | D、④②⑥① |
 N2O5是一种新型硝化剂,其性质和制备受到人们的关注.一定温度下,在2L固定容积的密闭容器中发生反应2N2O5(g)?4NO2(g)+O2(g)△H>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示.下列说法中,正确的是( )
N2O5是一种新型硝化剂,其性质和制备受到人们的关注.一定温度下,在2L固定容积的密闭容器中发生反应2N2O5(g)?4NO2(g)+O2(g)△H>0.反应物和部分生成物的物质的量随反应时间变化的曲线如图所示.下列说法中,正确的是( )| A、0~20 s内平均反应速率v(N2O5)=0.1 mol?(L?s)-1 |
| B、10 s时,正、逆反应速率相等,达到平衡 |
| C、20 s时,正反应速率大于逆反应速率 |
| D、曲线a表示NO2的物质的量随反应时间的变化 |