题目内容
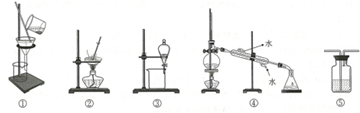
10.实验室制备下列有机物时,试剂的加入顺序或加热方法中错误的是( )| A. | 制乙烯:浓硫酸、乙醇,用酒精灯迅速加热至170℃ | |
| B. | 制硝基苯:浓硝酸、浓硫酸、苯,用55~60℃水浴加热 | |
| C. | 制乙酸乙酯:乙醇、浓硫酸、冰醋酸,用酒精灯缓慢加热 | |
| D. | 制酚醛树脂:苯酚、40%的甲醛溶液、浓盐酸,用沸水浴加热 |
分析 A.应先加入乙醇;
B.制备硝基苯应水浴加热;
C.乙醇和乙酸反应生成乙酸乙酯;
D.苯酚过量,应在酸性条件下.
解答 解:A.应先加入乙醇,再加入浓硫酸,故A错误;
B.制备硝基苯应水浴加热,不能直接加热至60℃,且苯与浓硫酸、浓硝酸反应制备硝基苯,故B正确;
C.乙醇和乙酸在浓硫酸作用下反应生成乙酸乙酯,可直接加热,故C正确;
D.苯酚过量,应在酸性条件下,则将苯酚、40%的甲醛溶液、浓盐酸沸水浴加热制酚醛树脂,故D正确.
故选A.
点评 本题考查化学实验方案的评价,涉及物质的制备,注意常见水浴加热的实验,实验细节是考查的重点,选项D为解答的难点,题目难度较大.

练习册系列答案
相关题目
11.铝和氢氧化钾都是重要的工业产品.工业品氢氧化钾的溶液中含有某些含氧酸杂质,可用离子交换膜法电解提纯.电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示,下列说法正确的( )

| A. | 阳极产生KOH | |
| B. | 阴极产生KOH | |
| C. | 大量H+ 通过离子交换膜从左侧到右侧 | |
| D. | 大量K+通过离子交换膜从右侧到左侧 |
12.下列关于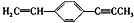 ,说法正确的是( )
,说法正确的是( )
 ,说法正确的是( )
,说法正确的是( )| A. | 最多只能有9个碳原子在同一平面上 | |
| B. | 有6个碳原子可能在同一直线上 | |
| C. | 最多有4个碳原子在同一直线上 | |
| D. | 所有原子一定都在同一平面上 |
9.若把周期表原先的主、副族号取消,由左到右按原顺序编为18列,如碱金属为第1列,稀有气体为第18列,按这个规定,下列说法不正确的是( )
| A. | 计算机芯片的组成元素位于第14列 | |
| B. | 第10列元素全部是金属元素 | |
| C. | 第18列元素单质全部是气体 | |
| D. | 只有第2列元素的原子最外层有2个电子 |
15. 已知H2R为二元弱酸:H2R?HR-+H+ Ka1 HR-?R2-+H+ Ka2
已知H2R为二元弱酸:H2R?HR-+H+ Ka1 HR-?R2-+H+ Ka2
常温下,向某浓度的H2R溶液中逐滴加入一定量浓度的KOH溶液,所得溶液中H2R、HR-、R2-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )
 已知H2R为二元弱酸:H2R?HR-+H+ Ka1 HR-?R2-+H+ Ka2
已知H2R为二元弱酸:H2R?HR-+H+ Ka1 HR-?R2-+H+ Ka2常温下,向某浓度的H2R溶液中逐滴加入一定量浓度的KOH溶液,所得溶液中H2R、HR-、R2-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )
| A. | pH=1.2溶液中:c(K+)+c(H+)=c(OH-)+c(H2R) | |
| B. | pH=2.7溶液中:c2(HR-)/[c(H2R)×c(R2-)]=1000 | |
| C. | 将相同物质的量KHR和K2R固体完全溶于水可配得pH为4.2的混合液 | |
| D. | 向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离程度一直增大 |
2.某反应体系中的物质有:NaOH、Au2O3、Na2S4O6、Au2O、H2O.己知Na2S4O6是生成物之一.则下列说法正确的是( )
| A. | 该反应体系中Au2O是氧化剂 | |
| B. | Na2S4O6是还原产物 | |
| C. | 该反应体系中起还原作用的元素是Au2O中+1价的Au | |
| D. | 该反应体系中每转移2mol电子则消耗1molH2O |
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.4g镁原子变成离子时,失去的电子数为0.3NA | |
| B. | 22.4L甲烷(CH4)所含的原子数为5NA | |
| C. | 98 g H2SO4和98 g H3PO4所含的氧原子数都是4NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA |