题目内容
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 2.4g镁原子变成离子时,失去的电子数为0.3NA | |
| B. | 22.4L甲烷(CH4)所含的原子数为5NA | |
| C. | 98 g H2SO4和98 g H3PO4所含的氧原子数都是4NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA |
分析 A.镁失去2个电子生成二价镁离子;
B.气体状况未知;
C.等质量的H2SO4和H3PO4的物质的量相等,二者含有分子数目相等,每个分子都含有4个O原子,所含氧原子数相同;
D.溶液体积未知.
解答 解:A.2.4g镁原子物质的量为0.1mol,变成镁离子时,失去的电子数为0.2NA,故A错误;
B.气体状况未知,气体摩尔体积不确定,无法计算甲烷的物质的量,故B错误;
C.等质量的H2SO4和H3PO4的物质的量相等,二者含有分子数目相等,每个分子都含有4个O原子,所含氧原子数相同,故C正确;
D.溶液体积未知,依据n=CV可知,无法计算微粒的个数,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的应用及有关计算,明确各个物理量关系是解本题关键,注意气体摩尔体积适用范围及适用条件,题目难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
20.标准状况下,往100mL 0.4mol/L的FeBr2溶液中通入一定体积的Cl2,充分反应后,溶液中有50%的Br-被氧化.则通入的氯气的体积是( )
| A. | 0.448L | B. | 0.672L | C. | 0.896L | D. | 1.344L |
10.实验室制备下列有机物时,试剂的加入顺序或加热方法中错误的是( )
| A. | 制乙烯:浓硫酸、乙醇,用酒精灯迅速加热至170℃ | |
| B. | 制硝基苯:浓硝酸、浓硫酸、苯,用55~60℃水浴加热 | |
| C. | 制乙酸乙酯:乙醇、浓硫酸、冰醋酸,用酒精灯缓慢加热 | |
| D. | 制酚醛树脂:苯酚、40%的甲醛溶液、浓盐酸,用沸水浴加热 |
7.将9.58g Na2CO3•10H2O与NaHCO3的混合物溶于水配成100mL溶液,测得c(Na+)=1mol/L.再取同质量的混合物,加入足量的盐酸,充分加热蒸干至质量不变时,所得固体的质量为( )
| A. | 5.85g | B. | 7.78g | C. | 6.72g | D. | 6g |
11.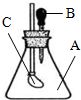 如图所示,锥形瓶内装有干燥的气体A,胶头滴管内盛有液体B,若挤压胶头滴管,使液体B滴入瓶中,振荡,一会儿可见小气球C鼓起.则对于气体A和液体B最可能的是( )
如图所示,锥形瓶内装有干燥的气体A,胶头滴管内盛有液体B,若挤压胶头滴管,使液体B滴入瓶中,振荡,一会儿可见小气球C鼓起.则对于气体A和液体B最可能的是( )
 如图所示,锥形瓶内装有干燥的气体A,胶头滴管内盛有液体B,若挤压胶头滴管,使液体B滴入瓶中,振荡,一会儿可见小气球C鼓起.则对于气体A和液体B最可能的是( )
如图所示,锥形瓶内装有干燥的气体A,胶头滴管内盛有液体B,若挤压胶头滴管,使液体B滴入瓶中,振荡,一会儿可见小气球C鼓起.则对于气体A和液体B最可能的是( )| A. | A是Cl2,B是饱和NaCl溶液 | B. | A是NH3,B是酚酞溶液 | ||
| C. | A是H2,B是水 | D. | A是CO2,B是NaHCO3饱和溶液 |
8.下列关于钠的叙述中不正确的是( )
| A. | 钠燃烧时发出黄色的火焰 | B. | 钠有很强的氧化性 | ||
| C. | 钠燃烧时生成氧化钠 | D. | 钠原子的最外层只有一个电子 |
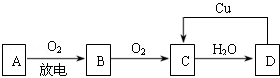
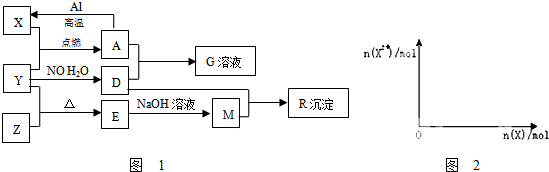
 ;
;