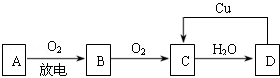
题目内容
5.下列实验中所选装置合理的是BEG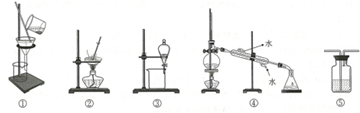
A.分离氯化钠和硝酸钾的混合物,选①和②
B.用CCl4提取碘水中的碘,选③
C.分离Na2CO3溶液和CH3COOC2H5,选④
D.分离苯和甲苯,乙醇和乙二醇,选③
E.用NaOH溶液吸收Cl2,用水吸收氨气,选⑤
F.除去乙醇中的苯酚,选①
G.除去苯中少量的苯酚,选③
分析 A.氯化钠和硝酸钾的溶解度受温度影响不同,利用结晶法分离;
B.碘易溶于CCl4,不易溶于水,应萃取、分液分离;
C.Na2CO3溶液和CH3COOC2H5分层,利用分液分离;
D.分离苯和甲苯,乙醇和乙二醇,均应利用蒸馏法;
E.氯气与NaOH溶液反应可吸收Cl2,氨气极易溶于水,用水吸收氨气;
F.乙醇中的苯酚,不分层;
G.苯中含少量的苯酚,不分层.
解答 解:A.氯化钠和硝酸钾的溶解度受温度影响不同,利用结晶法分离,不能利用②蒸发分离,故A错误;
B.碘易溶于CCl4,不易溶于水,应萃取、分液分离,则选择装置③,故B正确;
C.Na2CO3溶液和CH3COOC2H5分层,利用分液分离,则选择装置③,故C错误;
D.分离苯和甲苯,乙醇和乙二醇,均应利用蒸馏法,则选择装置④,故D错误;
E.氯气与NaOH溶液反应可吸收Cl2,氨气极易溶于水,用水吸收氨气,则选⑤洗气装置,故E正确;
F.乙醇中的苯酚,不分层,应利用蒸馏法,则选择装置④,故F错误;
G.苯中含少量的苯酚,不分层,应加NaOH溶液、分液,选③,故G正确;
故答案为:BEG.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、物质的性质、混合物分离提纯方法为解答的关键,侧重分析与实验能力的考查,注意有机物的性质及实验评价性分析,题目难度不大.

练习册系列答案
相关题目
6.(1)0.5mol H2O的质量为9g,其中含有0.5NA个水分子,共有0.5NA个原子.
(2)在下列提供的试剂中,选择合适的试剂除去下表中各混合物的杂质(括号内物质为杂质),并按要求填写空格.
A.NaOH溶液 B.稀盐酸 C.氯水 D.溴水
(2)在下列提供的试剂中,选择合适的试剂除去下表中各混合物的杂质(括号内物质为杂质),并按要求填写空格.
A.NaOH溶液 B.稀盐酸 C.氯水 D.溴水
| 混合物(括号内为杂质) | 除杂试剂(填序号) | 反 应 离 子 方 程 式 |
| ①Cu (CuO) | ||
| ②NaBr (NaI) |
7.下列有关化学用语表达正确的是( )
| A. | 乙炔分子的比例模型示意图: | B. | 2-甲基-2-戊烯的键线式: | ||
| C. | 乙醇的结构简式:CH3CH2OH | D. | 1,3-丁二烯的分子式:C4H8 |
10.实验室制备下列有机物时,试剂的加入顺序或加热方法中错误的是( )
| A. | 制乙烯:浓硫酸、乙醇,用酒精灯迅速加热至170℃ | |
| B. | 制硝基苯:浓硝酸、浓硫酸、苯,用55~60℃水浴加热 | |
| C. | 制乙酸乙酯:乙醇、浓硫酸、冰醋酸,用酒精灯缓慢加热 | |
| D. | 制酚醛树脂:苯酚、40%的甲醛溶液、浓盐酸,用沸水浴加热 |
17. 在t℃时,AgCl在水中的沉淀溶解平衡曲线如图所示(假设AgCl饱和溶液的密度与水的密度近似相等).下列说法错误的是( )
在t℃时,AgCl在水中的沉淀溶解平衡曲线如图所示(假设AgCl饱和溶液的密度与水的密度近似相等).下列说法错误的是( )
 在t℃时,AgCl在水中的沉淀溶解平衡曲线如图所示(假设AgCl饱和溶液的密度与水的密度近似相等).下列说法错误的是( )
在t℃时,AgCl在水中的沉淀溶解平衡曲线如图所示(假设AgCl饱和溶液的密度与水的密度近似相等).下列说法错误的是( )| A. | 在t℃时,AgCL的Ksp为4×10-10 | |
| B. | 在t℃时,c点溶液中一定有AgCl沉淀析出 | |
| C. | 在t℃时,AgCl的溶解度约为2.9×10-4g | |
| D. | d点溶液,温度升高后c(Ag+)、c(Cl-)均不变 |
15.下列表示物质结构的化学用语或模型正确的是( )
| A. | CO2分子比例模型: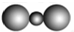 | B. | H2O2的电子式: | ||
| C. | 中子数为18的硫原子:${\;}_{16}^{34}$S | D. | 次氯酸的结构式:H-Cl-O |