题目内容
15. 已知H2R为二元弱酸:H2R?HR-+H+ Ka1 HR-?R2-+H+ Ka2
已知H2R为二元弱酸:H2R?HR-+H+ Ka1 HR-?R2-+H+ Ka2常温下,向某浓度的H2R溶液中逐滴加入一定量浓度的KOH溶液,所得溶液中H2R、HR-、R2-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )
| A. | pH=1.2溶液中:c(K+)+c(H+)=c(OH-)+c(H2R) | |
| B. | pH=2.7溶液中:c2(HR-)/[c(H2R)×c(R2-)]=1000 | |
| C. | 将相同物质的量KHR和K2R固体完全溶于水可配得pH为4.2的混合液 | |
| D. | 向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离程度一直增大 |
分析 A、pH=1.2溶液是KHR溶液,显示酸性,根据溶液中存在的电荷守恒以及物料守恒来回答;
B、二元弱酸:H2R?HR-+H+,Ka1;HR-?R2-+H+,Ka2;溶液中:c2(HR-)/[c(H2R)×c(R2-)]=$\frac{Ka1}{Ka2}$,据此计算回答;
C、pH为4.2的混合液显示酸性,根据图示信息HR-、R2-的物质的量分数相等,各占一半;
D、pH=1.2溶液是KHR溶液,向pH=1.2的溶液中加KOH溶液,KHR溶液和KOH溶液之间会发生反应得到K2R.
解答 解:A、pH=1.2溶液是KHR溶液,显示酸性,不存在R2-,存在H2R,根据溶液中存在的电荷和物料守恒得到:c(K+)+c(H+)=c(OH-)+c(H2R),故A正确;
B、首先根据图中的1、2交点和2、3交点,结合二元弱酸:H2R?HR-+H+,Ka1=$\frac{c({H}^{+})c(H{R}^{-})}{c({H}_{2}R)}$=10-1.2,HR-?R2-+H+,Ka2=$\frac{c({H}^{+})•c({R}^{2-})}{c(H{R}^{-})}$=10-4.2,溶液中:c2(HR-)/[c(H2R)×c(R2-)]=$\frac{Ka1}{Ka2}$=1000,故B正确,
C、pH为4.2的混合液显示酸性,根据图示信息HR-、R2-的物质的量分数相等,各占一半,将相同物质的量KHR和K2R固体完全溶于水,R2-的水解程度较大,所以不可能得到符合条件的混合液,不能这样配得pH为4.2得溶液,故C错误;
D、pH=1.2溶液是KHR溶液,向pH=1.2的溶液中加KOH溶液,KHR溶液和KOH溶液之间会发生反应得到K2R,R2-的水解程度较大,对水的电离起到促进作用,水的电离程度一直增大,故D正确.
故选C.
点评 本题考查学生弱电解质的电离以及盐的水解原理的应用等方面的知识,属于综合知识的考查,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 物质发生化学反应时都伴随着能量变化,伴随能量变化的物质变化一定是化学变化 | |
| B. | 太阳能、煤气、潮汐能是一次能源:电力、蒸汽、地热是二次能源 | |
| C. | 吸热反应就是反应物的总能量比生成物的总能量小的反应:也可以理解为化学键断裂时吸收的能量比化学键形成时放出的能量少的反应 | |
| D. | CO(g)的燃烧热是283.0kJ/mol则2CO2(g)=2CO(g)+O2(g) 反应的△H=+566.0kJ/mol |
| A. | 新制氯水中加入少量固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+cOH-) | |
| B. | pH=9的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.1mol•L-1CH3COOH溶液与0.05mol•L-1NaOH溶液等体积混合:2c(H+)+c((CH3COOH)=c(CH3COO-)+2c(OH-) |
| A. | 制乙烯:浓硫酸、乙醇,用酒精灯迅速加热至170℃ | |
| B. | 制硝基苯:浓硝酸、浓硫酸、苯,用55~60℃水浴加热 | |
| C. | 制乙酸乙酯:乙醇、浓硫酸、冰醋酸,用酒精灯缓慢加热 | |
| D. | 制酚醛树脂:苯酚、40%的甲醛溶液、浓盐酸,用沸水浴加热 |

 )是一种治疗心脏病的药物,可由甲基丙烯、丙烯和
)是一种治疗心脏病的药物,可由甲基丙烯、丙烯和 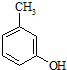 为原料制取.
为原料制取.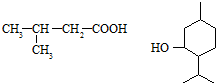 .
.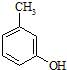 的名称3-甲基苯酚,其属于芳香族化合物的同分异构有4种(不含
的名称3-甲基苯酚,其属于芳香族化合物的同分异构有4种(不含 ).
). +CH3-CH=CH2$\stackrel{AlCl_{3}}{→}$
+CH3-CH=CH2$\stackrel{AlCl_{3}}{→}$ 反应类型属于加成反应.有机反应中通常副反应较多,实际生产中发现生成
反应类型属于加成反应.有机反应中通常副反应较多,实际生产中发现生成 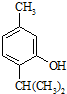 的量远大于生成
的量远大于生成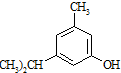 的量,试分析其原因:羟基使得苯环的邻对位氢原子易于取代.
的量,试分析其原因:羟基使得苯环的邻对位氢原子易于取代.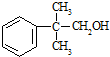 的合成线路:(合成路线常用的表示方式为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物 )
的合成线路:(合成路线常用的表示方式为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物 ) .
. 电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol•L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.
电镀厂曾采用有氰电镀工艺,由于排放的废水中含有的剧毒CN-离子,而逐渐被无氰电镀工艺替代.处理有氰电镀的废水时,可在催化剂TiO2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2.环保工作人员在密闭系统中用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率.将浓缩后含CN-离子的污水与过量NaClO溶液的混合液共200mL(其中CN-的浓度为0.05mol•L-1)倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞.