题目内容
8.类推思维是化学解题中常用的一种思维方法,下列有关离子方程式的类推正确的是( )| 已知 | 类推 | |
| A | 将Fe加入CuSO4溶液中 Fe+Cu2+═Cu+Fe2+ | 将Na加入到CuSO4溶液中 2Na+Cu2+═Cu+2Na+ |
| B | 稀盐酸与NaOH溶液反应至中性 H++OH-=H2O | 稀HNO3与Ba(OH)2溶液反应至中性 H++OH-═H2O |
| C | 用惰性电极电解NaCl溶液 2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | 用惰性电极电解MgBr2溶液 2Br-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Br2 |
| D | 向Ca(ClO)2溶液中通入少量CO2 Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2 Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| A. | A | B. | B | C. | C | D. | D |
分析 A.钠与盐溶液反应,先与水反应;
B.强酸与强碱反应实质是氢离子与氢氧根子反应生成水;
C.电解溴化镁生成溴、氢气和氢氧化镁;
D.二氧化硫具有还原性,能够被次氯酸根离子氧化;
解答 解:A.铁排在金属铜的前面,金属铁可以将金属铜从其盐中置换出来,但是活泼金属钠和盐的反应一定是先和盐中的水反应,不会置换出其中的金属,故A错误;
B.HNO3与Ba(OH)2溶液反应至中性H++OH-═H2O,故B正确;
C.用惰性电极电解MgBr2溶液Mg2++2Br-+2H2O$\frac{\underline{\;电解\;}}{\;}$Mg(OH)2↓+H2↑+Br2,故C错误;
D.向Ca(ClO)2溶液中通入少量SO2,二氧化硫具有还原性,被次氯酸根离子氧化,离子方程式为:Ca2++3ClO-+SO2+H2O═CaSO4↓+Cl-+2HClO,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,为考试的热点,明确反应的实质是解题关键,注意化学式的拆分,题目难度不大.

练习册系列答案
相关题目
7.仪器可以不直接加热的是( )
| A. | 试管 | B. | 坩埚 | C. | 蒸发皿 | D. | 蒸馏焼瓶 |
5.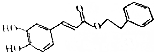 咖啡酸苯乙酯是蜂胶的主要成分,因具有极强的抗炎和抗氧化活性得以在食品、医学以及其他领城广泛应用,其分子结构简式如图.下列关于咖啡酸苯乙酯的说法不正确的是( )
咖啡酸苯乙酯是蜂胶的主要成分,因具有极强的抗炎和抗氧化活性得以在食品、医学以及其他领城广泛应用,其分子结构简式如图.下列关于咖啡酸苯乙酯的说法不正确的是( )
 咖啡酸苯乙酯是蜂胶的主要成分,因具有极强的抗炎和抗氧化活性得以在食品、医学以及其他领城广泛应用,其分子结构简式如图.下列关于咖啡酸苯乙酯的说法不正确的是( )
咖啡酸苯乙酯是蜂胶的主要成分,因具有极强的抗炎和抗氧化活性得以在食品、医学以及其他领城广泛应用,其分子结构简式如图.下列关于咖啡酸苯乙酯的说法不正确的是( )| A. | 咖啡酸苯乙酯的分子式为C17H16O4 | |
| B. | 咖啡酸苯乙酯可以发生水解、取代、消去反应 | |
| C. | 1mol咖啡酸苯乙酯最多可与7mol H2反应 | |
| D. | 1mol咖啡酸苯乙酯最多可与4mol Br2反应 |
13.短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
| A. | 元素X的简单气态氢化物的热稳定性比W的弱 | |
| B. | 元素W的最高价氧化物对应水化物的酸性比Z的弱 | |
| C. | 化合物YX、ZX2、WX3中化学键的类型相同 | |
| D. | 原子半径的大小顺序:rY>rZ>rW>rX |
18.铝和镓的性质相似.处理含Ga2O3的Al2O3时,先加入过量NaOH溶液,再通入适量CO2,有Al(OH)3沉淀,而NaGaO2留在溶液中.由此可以判断( )
| A. | Ga(OH)3酸性强于Al(OH)3 | B. | Al(OH)3酸性强于Ga(OH)3 | ||
| C. | Ga(OH)3碱性强于Al(OH)3 | D. | Al(OH)3碱性强于Ga(OH)3 |
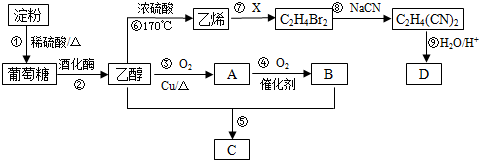
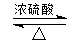 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.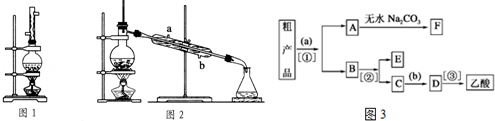
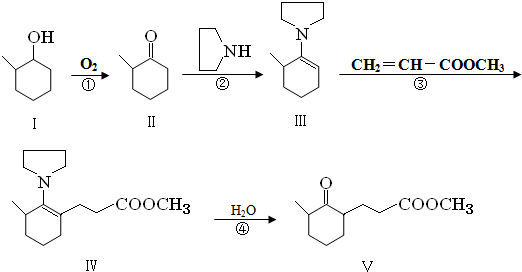
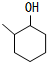 +O2 $→_{△}^{催化剂}$ 2
+O2 $→_{△}^{催化剂}$ 2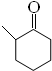 +2H2O(不要求注明反应条件).
+2H2O(不要求注明反应条件).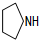 .
.

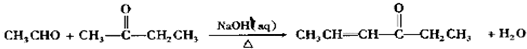
 ;
;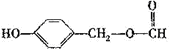 ;
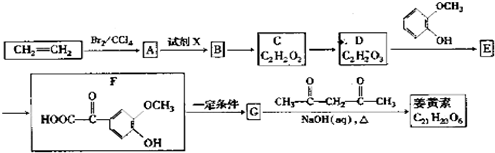
; ),写出制备肉桂醛所需有机物的结构简式
),写出制备肉桂醛所需有机物的结构简式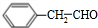 、CH3CHO.
、CH3CHO.