题目内容
化学实验是探索物质世界的重要手段.下列实验方案设计正确的是( )
| A、向裂化汽油中滴加少量酸性高锰酸钾溶液,振荡.若紫红色褪去,即可证明其中含甲苯等苯的同系物 |
| B、选用新制Cu(OH)2悬浊液可以鉴别水、苯、溴苯、乙醛和乙酸 |
| C、采用普通蒸馏装置,将溴的四氯化碳溶液中的溶质与溶剂分离 |
| D、检验某铁粉样品中是否有少量氧化铁杂质,实验步骤为:取少许样品,用盐酸溶解,然后滴加KSCN溶液 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.裂化汽油中含烯烃类物质;
B.水、苯、溴苯、乙醛和乙酸分别与新制Cu(OH)2悬浊液混合,现象分别为无现象、分层后有机层在上层、分层后有机层在下层、砖红色沉淀、蓝色溶液;
C.溴与四氯化碳的沸点差异不大;
D.用盐酸溶解,生成的氯化铁与Fe反应.
B.水、苯、溴苯、乙醛和乙酸分别与新制Cu(OH)2悬浊液混合,现象分别为无现象、分层后有机层在上层、分层后有机层在下层、砖红色沉淀、蓝色溶液;
C.溴与四氯化碳的沸点差异不大;
D.用盐酸溶解,生成的氯化铁与Fe反应.
解答:
解:A.裂化汽油中含烯烃类物质,则向裂化汽油中滴加少量酸性高锰酸钾溶液,振荡.若紫红色褪去,不能证明其中含甲苯等苯的同系物,故A错误;
B.水、苯、溴苯、乙醛和乙酸分别与新制Cu(OH)2悬浊液混合,现象分别为无现象、分层后有机层在上层、分层后有机层在下层、砖红色沉淀、蓝色溶液,现象不同,可以鉴别,故B正确;
C.溴与四氯化碳的沸点差异不大,不能利用普通蒸馏装置分离,故C错误;
D.用盐酸溶解,生成的氯化铁与Fe反应,不能检验铁离子,则应先利用磁铁将铁分离出,对剩余固体用盐酸溶解,然后滴加KSCN溶液,故D错误;
故选B.
B.水、苯、溴苯、乙醛和乙酸分别与新制Cu(OH)2悬浊液混合,现象分别为无现象、分层后有机层在上层、分层后有机层在下层、砖红色沉淀、蓝色溶液,现象不同,可以鉴别,故B正确;
C.溴与四氯化碳的沸点差异不大,不能利用普通蒸馏装置分离,故C错误;
D.用盐酸溶解,生成的氯化铁与Fe反应,不能检验铁离子,则应先利用磁铁将铁分离出,对剩余固体用盐酸溶解,然后滴加KSCN溶液,故D错误;
故选B.
点评:本题考查化学实验方案的评价,为高频考点,涉及物质的鉴别、结构与性质、混合物分离提纯及离子检验等,侧重物质性质及实验操作的考查,注意实验方案的评价性、操作性分析,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
下列表述与示意图相符的是( )


| A、正反应为吸热反应 | ||
| B、升高温度,有利于反应向正方向进行 | ||
| C、A点时,反应向逆反应方向移动 | ||
D、K正与K逆的关系是:K正=
|
常温下,有①氨水 ②NH4Cl溶液 ③Na2CO3溶液 ④NaHCO3溶液各25mL,物质的量浓度均为0.1mol/L,下列说法正确的是( )
| A、四种溶液的pH的大小顺序:①>④>③>② |
| B、将溶液①、②等体积混合所得碱性溶液中:c(NH4+)<c(NH3?H2O) |
| C、向溶液①、②中分别滴加25mL 0.1mol/L盐酸后,溶液中c(NH4+):①>② |
| D、将溶液③、④等体积混合所得溶液中:2 c(OH-)-2c(H+)=3c(H2CO3)+c(HCO3-)-c(CO32-) |
物质变化过程中常常伴随着能量的变化.下列过程中一定向外释放能量的是( )
| A、石油裂化 |
| B、氢气与碘蒸气化合 |
| C、铵盐溶于水 |
| D、形成碳氢键 |
 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.
 )是一种医药中间体,用茴香醛(
)是一种医药中间体,用茴香醛(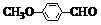 )经两步反应合成D,请写出第②步反应的化学方程式(其他原料自选,并注明必要的反应条件).
)经两步反应合成D,请写出第②步反应的化学方程式(其他原料自选,并注明必要的反应条件).
 转化为
转化为 ,其合成线路如下:
,其合成线路如下: 写(Ⅱ)(Ⅲ)两步反应的化学方程式:
写(Ⅱ)(Ⅲ)两步反应的化学方程式: 对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:
对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题: