题目内容
 对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:
对大气污染物SO2、NOx进行研究具有重要环保意义.请回答下列问题:(1)为减少SO2的排放,常采取的措施是将煤转化为清洁气体燃料.
已知:H2(g)+
| 1 |
| 2 |
C(s)+
| 1 |
| 2 |
写出焦炭与水蒸气反应的热化学方程式:
(2)已知汽缸中生成NO的反应为:N2(g)+O2(g)?2NO(g)△H>0,若1.0mol空气含0.80mol N2和0.20mol O2,1300°C时在1.0L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4mol.
①5s内该反应的平均速率ν(NO)=
②汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是
(3)汽车尾气中NO和CO的转化.当催化剂质量一定时,增大催化剂固体的表面积可提高化学反应速率.如图表示在其他条件不变时,反应2NO(g)+2CO(g)?2CO2(g)+N2(g)中,NO的浓度c(NO)随温度(T)、催化剂表面积(S)和时间(t)的变化曲线.
①该反应的△H
②若催化剂的表面积S1>S2,在图中画出c(NO)在T1、S2条件下达到平衡过程中的变化曲线(并作相应标注).
考点:化学平衡常数的含义,热化学方程式,化学反应速率的影响因素
专题:
分析:(1)依据热化学方程式和盖斯定律计算得到所需让化学方程式;
(2)①计算出平衡时各种物质的物质的量,结合反应速率计算方法和平衡常数的表达式完成;
②汽缸温度越高,单位时间内NO排放量越大,说明平衡正向进行,温度越高速率越快;
(3)①根据到达平衡的时间,判断温度高低,再根据不同温度下到达平衡时NO的浓度高低,判断温度对平衡的影响,据此判断反应热效应;
②催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,据此作图.
(2)①计算出平衡时各种物质的物质的量,结合反应速率计算方法和平衡常数的表达式完成;
②汽缸温度越高,单位时间内NO排放量越大,说明平衡正向进行,温度越高速率越快;
(3)①根据到达平衡的时间,判断温度高低,再根据不同温度下到达平衡时NO的浓度高低,判断温度对平衡的影响,据此判断反应热效应;
②催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,据此作图.
解答:
解:(1)①H2(g)+
O2(g)=H2O(g)△H=-241.8kJ?mol-1
②C(s)+
O2(g)=CO(g)△H=-110.5kJ?mol-1
依据盖斯定律计算②-①得到C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ?mol-1;
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ?mol-1;
(2)①在1.0L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4mol,5s内该反应的平均速率ν(NO)=
=1.6×10-4 mol/(L?s),依据化学方程式写出反应的平衡常数为:
;
故答案为:1.6×10-4 mol/(L?s),
;
②气缸温度越高,单位时间内NO排放量越大,原因是温度升高,反应速率加快,平衡右移,
故答案为:温度升高,反应速率加快,平衡右移;
(3)①、温度T2到达平衡的时间短,反应速率快,故温度T2>T1,温度越高,平衡时NO的浓度越高,说明升高温度平衡向逆反应移动,故正反应为放热反应,即△H<0,
故答案为:<;
②、催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,故c(NO) 在T1、S2条件下达到平衡过程中的变化曲线为: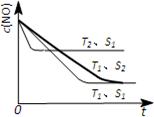 ,故答案为:
,故答案为: .
.
| 1 |
| 2 |
②C(s)+
| 1 |
| 2 |
依据盖斯定律计算②-①得到C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ?mol-1;
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ?mol-1;
(2)①在1.0L密闭容器内经过5s反应达到平衡,测得NO为8.0×10-4mol,5s内该反应的平均速率ν(NO)=
| ||
| 5s |
| c2(NO) |
| c(N2)c(O2) |
故答案为:1.6×10-4 mol/(L?s),
| c2(NO) |
| c(N2)c(O2) |
②气缸温度越高,单位时间内NO排放量越大,原因是温度升高,反应速率加快,平衡右移,
故答案为:温度升高,反应速率加快,平衡右移;
(3)①、温度T2到达平衡的时间短,反应速率快,故温度T2>T1,温度越高,平衡时NO的浓度越高,说明升高温度平衡向逆反应移动,故正反应为放热反应,即△H<0,
故答案为:<;
②、催化剂的表面积S1>S2,则催化剂S1到达平衡的时间比催化剂S2短,催化剂不影响平衡移动,平衡时NO的浓度相同,故c(NO) 在T1、S2条件下达到平衡过程中的变化曲线为:
 ,故答案为:
,故答案为: .
.
点评:本题主要考查热化学方程式书写,化学反应速率、影响化学平衡的因素、化学平衡图象以及热化学方程式的书写等,难度不大,(3)中注意根据“先拐先平数值大”原则判断温度高低是关键,作图时注意到达平衡的时间与平衡时NO的浓度.

练习册系列答案
相关题目
将CO2转化成有机物可有效实现碳循环.下列反应中,最节能的是( )
A、CO2+3H2
| |||
B、6CO2+6H2O
| |||
C、CO2+CH4
| |||
D、2CO2+6H2
|
化学实验是探索物质世界的重要手段.下列实验方案设计正确的是( )
| A、向裂化汽油中滴加少量酸性高锰酸钾溶液,振荡.若紫红色褪去,即可证明其中含甲苯等苯的同系物 |
| B、选用新制Cu(OH)2悬浊液可以鉴别水、苯、溴苯、乙醛和乙酸 |
| C、采用普通蒸馏装置,将溴的四氯化碳溶液中的溶质与溶剂分离 |
| D、检验某铁粉样品中是否有少量氧化铁杂质,实验步骤为:取少许样品,用盐酸溶解,然后滴加KSCN溶液 |

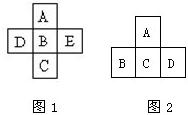 (Ⅰ)A、B、C、D、E五种元素在周期表里的位置如图1所示:
(Ⅰ)A、B、C、D、E五种元素在周期表里的位置如图1所示: