题目内容
下列各组微粒能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写正确的是( )
| 选项 | 微粒组 | 所加试剂 | 离子方程式 |
| A | NH4+、Fe2+、SO42- | 少量Ba(OH)2溶液 | 2NH4++SO42-+Ba2++2OH- →BaSO4↓+2NH3?H2O |
| B | Mg2+、HCO3-、Cl- | 过量NaOH溶液 | Mg2++2HCO3-+4OH- →Mg(OH)2↓+2CO32-+2H2O |
| C | Fe2+、NO3-、HSO3- | NaHSO4溶液 | HSO3-+H+→SO2↑+H2O |
| D | K+、NH3?H2O、CO32- | 通入少量CO2 | 2NH3?H2O+CO2 →2NH4++CO32- |
| A、A | B、B | C、C | D、D |
考点:离子方程式的书写,离子共存问题
专题:离子反应专题
分析:A.氢氧化钡少量,反应按照氢氧化钡的组成进行,亚铁离子优先与氢氧根离子反应;
B.氢氧化镁过量,镁离子、碳酸氢根离子完全反应分别生成氢氧化镁沉淀、碳酸根离子;
C.硫酸氢钠为强酸性溶液,硝酸根离子在酸性条件下能够氧化亚铁离子和亚硫酸根离子;
D.氨水能够与二氧化碳反应生成铵根离子和碳酸根离子.
B.氢氧化镁过量,镁离子、碳酸氢根离子完全反应分别生成氢氧化镁沉淀、碳酸根离子;
C.硫酸氢钠为强酸性溶液,硝酸根离子在酸性条件下能够氧化亚铁离子和亚硫酸根离子;
D.氨水能够与二氧化碳反应生成铵根离子和碳酸根离子.
解答:
解:A.氢氧化钡少量,亚铁离子优先与氢氧根离子反应,正确的离子方程式为:Fe2++SO42-+Ba2++2OH-=BaSO4↓+Fe(OH)2↓,故A错误;
B.氢氧化钠过量,镁离子和碳酸氢根离子完全反应,反应的离子方程式为:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O,故B正确;
C.硫酸氢钠溶液为强酸性溶液,硝酸根离子在酸性条件下能够氧化亚铁离子和亚硫酸氢根离子,如果硝酸根离子足量,反应的离子方程为:HSO3-+NO3-+Fe2++H+═NO↑+Fe3++SO42-+H2O,故C错误;
D.一水合氨与二氧化碳反应生成铵根离子与碳酸根离子,反应的离子方程式为:2NH3?H2O+CO2=2NH4++CO32-,故D正确;
故选BD.
B.氢氧化钠过量,镁离子和碳酸氢根离子完全反应,反应的离子方程式为:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O,故B正确;
C.硫酸氢钠溶液为强酸性溶液,硝酸根离子在酸性条件下能够氧化亚铁离子和亚硫酸氢根离子,如果硝酸根离子足量,反应的离子方程为:HSO3-+NO3-+Fe2++H+═NO↑+Fe3++SO42-+H2O,故C错误;
D.一水合氨与二氧化碳反应生成铵根离子与碳酸根离子,反应的离子方程式为:2NH3?H2O+CO2=2NH4++CO32-,故D正确;
故选BD.
点评:本题考查了离子方程式的正误判断,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,选项C为难点和易错点,注意硝酸根离子在酸性条件下具有强氧化性.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
在一个2L的容器中,放入2mol气体A,5分钟后,测得这种气体A还剩余0.5mol,该反应中气体A的化学反应速率是( )
| A、1.5mol/(L?min) |
| B、0.15mol/(L?min) |
| C、0.75mol/(L?min) |
| D、0.075mol/(L?min) |
将CO2转化成有机物可有效实现碳循环.下列反应中,最节能的是( )
A、CO2+3H2
| |||
B、6CO2+6H2O
| |||
C、CO2+CH4
| |||
D、2CO2+6H2
|
下列反应中不属于氧化还原反应的是( )
| A、Cl2+2NaOH═NaCl+NaClO+H2O |
| B、NH3+HCl═NH4Cl |
| C、Br2+2KI═I2+2KBr |
| D、CO2+Ca(OH)2═CaCO3+H2O |
下列叙述正确的是( )
| A、常温下,无论是纯水,还是酸、碱、盐的稀溶液中,c(H+)?c(OH-)=1×10-14 |
| B、c(H+)=1×10-7 mol?L-1的溶液一定是中性溶液 |
| C、0.2 mol?L-1 醋酸溶液中的c(H+)是0.1 mol?L-1 醋酸溶液中的c(H+)的2倍 |
| D、任何浓度的溶液都可以用pH来表示其酸碱性的强弱 |
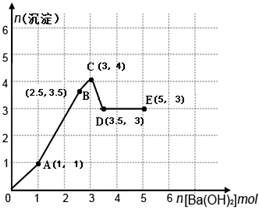 向物质的量各有1mol的NH4Al(SO4)2和H2SO4混合稀溶液中逐滴加入一定量Ba(OH)2溶液,产生沉淀的量随着Ba(OH)2加入量的变化如图所示.下列离子方程式书写正确的是( )
向物质的量各有1mol的NH4Al(SO4)2和H2SO4混合稀溶液中逐滴加入一定量Ba(OH)2溶液,产生沉淀的量随着Ba(OH)2加入量的变化如图所示.下列离子方程式书写正确的是( )| A、O→A:H++SO42-+Ba2++OH-→BaSO4↓+H2O |
| B、A→B:2Al3++3SO42-+3Ba2++6OH-→3BaSO4↓+2Al(OH)3↓ |
| C、B→C:2NH4++SO42-+Ba2++2OH-→BaSO4↓+2NH3?H2O |
| D、D→E:NH4++OH-→NH3?H2O |
化学实验是探索物质世界的重要手段.下列实验方案设计正确的是( )
| A、向裂化汽油中滴加少量酸性高锰酸钾溶液,振荡.若紫红色褪去,即可证明其中含甲苯等苯的同系物 |
| B、选用新制Cu(OH)2悬浊液可以鉴别水、苯、溴苯、乙醛和乙酸 |
| C、采用普通蒸馏装置,将溴的四氯化碳溶液中的溶质与溶剂分离 |
| D、检验某铁粉样品中是否有少量氧化铁杂质,实验步骤为:取少许样品,用盐酸溶解,然后滴加KSCN溶液 |
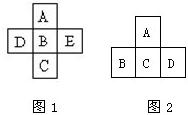 (Ⅰ)A、B、C、D、E五种元素在周期表里的位置如图1所示:
(Ⅰ)A、B、C、D、E五种元素在周期表里的位置如图1所示: