��Ŀ����
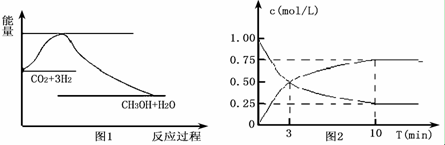
2��ʵ�֡����ܼ��š��͡���̼���á���һ����Ҫ���������ν�CO2ת��Ϊ�����õ��ʣ�Ŀǰ��ҵ����һ�ַ�������CO2����ȼ�ϼ״���һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g������ͼ1��ʾ�÷�Ӧ��������������λΪkJ•mol-1���ı仯����1�����ڸ÷�Ӧ������˵���У���ȷ����C������ĸ����
A����H��0����S��0 B����H��0����S��0
C����H��0����S��0 D����H��0����S��0
��2��Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊl L���ܱ������У�����l mol CO2��4mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g�������CO2��CH3OH��g����Ũ����ʱ��仯����ͼ2��ʾ��
�ٴӷ�Ӧ��ʼ��ƽ�⣬CO2��ƽ����Ӧ����v��CO2��=0.075 mol•L-1•min-1��H2��ת����w��H2��=56.25%��
�ڸ÷�Ӧ��ƽ�ⳣ������ʽK=$\frac{[C{H}_{3}OH]•[{H}_{2}O]}{[C{O}_{2}]•[{H}_{2}]^{3}}$��
�����д�ʩ����ʹ��ѧƽ��������Ӧ�����ƶ�����BD ������ĸ����
A�������¶� B����CH3OH��g����ʱҺ�����
C��ѡ���Ч���� D���ٳ���l molCO2��4molH2
��3��25�棬1.01��105Paʱ��16g Һ̬�״���ȫȼ�գ����ָ���ԭ״̬ʱ���ų�363.3kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ��CH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-726.6 kJ•mol-1��
���� ��1�����ݷ�Ӧ��ͼ������жϣ�CO2��g��+3H2��g��?CH3OH��g��+H2O��g������Ӧ���ؼ��ٵķ�Ӧ��S��0����Ӧ������������������������жϷ�Ӧ�Ƿ��ȷ�Ӧ����H��0��
��2�������Ϊl L���ܱ������У�����l mol CO2��4mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g�������CO2��CH3OH��g����Ũ����ʱ��仯��ͼ2��ʾ��������̼�Ƿ�Ӧ���淴Ӧ����Ũ�ȼ�С���״���������淴Ӧ����Ũ������10nim�ڴﵽƽ�⣬���ɼ״�Ũ��Ϊ0.75mol/L��������̼Ũ�ȱ仯��0.75mol/L�������ݻ�ѧƽ������ʽ��ʽ�����жϣ������ݻ�ѧƽ�ⳣ���ĸ�����дƽ�ⳣ������ʽ�������ݻ�ѧ��Ӧ��Ӱ�����غ�������������жϣ�
A����Ӧ�Ƿ��ȷ�Ӧ������ƽ��������У�B����CH3OH��g����ʱҺ���������С���������ƽ��������У�
C��ѡ���Ч����ֻ�ܸı����ʣ����ı仯ѧƽ�⣻D���ٳ���l molCO2��4molH2������ѹǿƽ��������У�
��3��25�棬1.01��105Paʱ��16g Һ̬�״���ȫȼ�գ����ָ���ԭ״̬ʱ���ų�363.3kJ��������������д�Ȼ�ѧ����ʽ�ķ���д���÷�Ӧ���Ȼ�ѧ����ʽΪ��CH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-726.6 kJ•mol-1��
��� �⣺��1�����ݷ�Ӧ��ͼ������жϣ�CO2��g��+3H2��g��?CH3OH��g��+H2O��g������Ӧ���ؼ��ٵķ�Ӧ��S��0����Ӧ������������������������жϷ�Ӧ�Ƿ��ȷ�Ӧ����H��0��
�ʴ�Ϊ��C��
��2�������Ϊl L���ܱ������У�����l mol CO2��4mol H2��һ�������·�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g�������CO2��CH3OH��g����Ũ����ʱ��仯��ͼ2��ʾ��������̼�Ƿ�Ӧ���淴Ӧ����Ũ�ȼ�С���״���������淴Ӧ����Ũ������10nim�ڴﵽƽ�⣬���ɼ״�Ũ��Ϊ0.75mol/L��������̼Ũ�ȱ仯��0.75mol/L����
�����ݻ�ѧƽ����ʽ����Ϊ��
CO2��g��+3H2��g��?CH3OH��g��+H2O��g��
��ʼ����mol/L�� 1 4 0 0
�仯����mol/L�� 0.75 2.25 0.75 0.75
ƽ������mol/L�� 0.25 1.75 0.75 0.75
CO2��ƽ����Ӧ����v��CO2��=$\frac{0.75mol/L}{10min}$=0.075mol•L-1•min-1 ��H2��ת����w��H2��=$\frac{2.25mol/L}{4mol/L}$��100%=56.25%��
�ʴ�Ϊ��0.075 mol•L-1•min-1��56.25%��
�ڸ÷�Ӧ��ƽ�ⳣ������ʽK=$\frac{[C{H}_{3}OH]•[{H}_{2}O]}{[C{O}_{2}]•[{H}_{2}]^{3}}$���ʴ�Ϊ��$\frac{[C{H}_{3}OH]•[{H}_{2}O]}{[C{O}_{2}]•[{H}_{2}]^{3}}$��
�۴�ʩ����ʹ��ѧƽ��������Ӧ�����ƶ����ǣ�
A����Ӧ�Ƿ��ȷ�Ӧ������ƽ��������У���A����
B����CH3OH��g����ʱҺ���������С�����������ƽ��������У���B��ȷ��
C��ѡ���Ч����ֻ�ܸı����ʣ����ı仯ѧƽ�⣬��C����
D���ٳ���l molCO2��4molH2������ѹǿƽ��������У���D��ȷ��
�ʴ�Ϊ��BD��
��3��25�棬1.01��105Paʱ��16g Һ̬�״����ʵ���Ϊ0.5mol����ȫȼ�գ����ָ���ԭ״̬ʱ���ų�363.3kJ��������������д�Ȼ�ѧ����ʽ�ķ���д���÷�Ӧ���Ȼ�ѧ����ʽΪ��CH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-726.6 kJ•mol-1��
�ʴ�Ϊ��CH3OH��l��+$\frac{3}{2}$O2��g��=CO2��g��+2H2O��l����H=-726.6 kJ•mol-1��
���� ���⿼���˷�Ӧ���ʱ��жϣ��Ȼ�ѧ����ʽ����дԭ��ѧƽ���Ӱ�������ж�ƽ���ƶ�����ѧƽ��ļ����Ӧ�ã�ͼ������ǹؼ����ۺ��Խϴ��Ѷ��еȣ�


| A�� | Teԭ�ӵ����ԭ��������127.5 | |
| B�� | TeԪ�ؿ��ܻ��ж���ͬλ�� | |
| C�� | Teԭ��5p�Dz���2�ԳɶԵ��� | |
| D�� | Teԭ���������6���˶�״̬��ͬ�ĵ��� |

| ѡ�� | �� | �� | �� | �Թ������� |
| A | Ũ��ˮ | ��ʯ�� | Al��SO4��3��Һ | �ȳ�������ʧ |
| B | Ũ���� | ͭ | ����KI��Һ | �Թܿڳ��ֺ���ɫ��Һ��Ϊ��ɫ |
| C | Ũ���� | �������� | ʯ����Һ | �ȱ�����ɫ |
| D | ˫��ˮ | �������� | ������ | ��Һ���ֻ��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
| A�� | pH=7����Һ�У�Fe3+��NH4+��Cl-��N03- | |
| B�� | ˮ�������c��H+��=$\sqrt{{k}_{w}}$����Һ�У�Na+��S042-��C032-��K+ | |
| C�� | ��ˮ�����c��OH-��=1��10-2mol•L-1����Һ�У�Cl-��CH3COO-��K+��AlO2- | |
| D�� | $\frac{c��O{H}^{-}��}{c��{H}^{+}��}$=1012����Һ�У�NH4+��Al3+��N03-��Cl- |
| A�� | ���������Ե������ڷ�Ӧ��һ���������� | |
| B�� | ������ԭ��Ӧ��ʵ���ǵ���ת�� | |
| C�� | ijԪ�ش�����̬��Ϊ����̬����Ԫ��һ�������� | |
| D�� | ��Ӧ�е���һ��Ԫ�ر�����ʱ��һ������һ��Ԫ�ر���ԭ |
| A�� | ������ˮ���γɵ�Al��OH��3����������ˮ�������������ˮ�ľ��� | |
| B�� | ���������������������ͻ���� | |
| C�� | Fe2O3�׳����죬��������ɫ�������Ϳ�� | |
| D�� | Na2O2����ǿ�����ԣ�����������������еĹ����� |
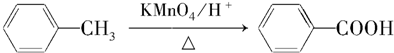

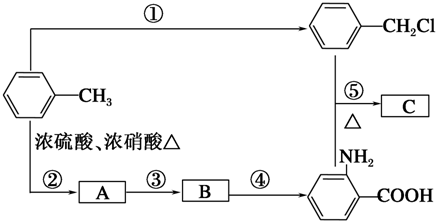
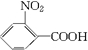 ��A���ʵĽṹ��ʽ��
��A���ʵĽṹ��ʽ��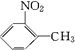 ��
��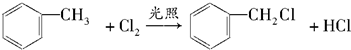 ��ȡ����Ӧ
��ȡ����Ӧ ��ȡ����Ӧ��
��ȡ����Ӧ��