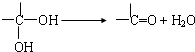
题目内容
12.已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质).现用A与石墨作电极,B的浓溶液作电解质,构成原电池.有关物质之间的转化关系如下图:(注意:其中有些反应的条件及部分生成物被略去)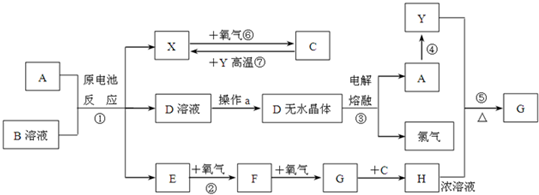
请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.
(2)A与石墨作电极,B的浓溶液作电解质,构成原电池,
负极反应:Mg-2e-=Mg2+;正极反应:2NH4++2e-=NH3↑+H2↑.
(3)从D溶液制备D的无水晶体的“操作A”为将D溶液在HCl气流中蒸干.
(4)反应②的化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(5)反应⑤的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
分析 C为无色液体,由气体X(X由原电池反应得到,可能是H2)和氧气反应得到,故C应是H2O,X是H2,根据反应⑦可知非金属Y是C.由电解D无水晶体得到A与Cl2,可知D为氯化物且是离子化合物,结合A+B溶液发生原电池反应得到X、D、E,可知B为氯化物,且B是一种盐,受热极易分解,反应生成的H2与E气体,B应水解呈酸性,由转化关系:E→F→G→H,属于常温下气体E的连续氧化得到气体G,在中学阶段中N、S元素化合物符合转化关系,考虑反应①是金属与NH4Cl溶液发生的原电池反应,可推出E为NH3、F为NO、G为NO2,则H为HNO3.(1)中反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,应为Mg与二氧化碳的反应,可推出A为Mg,则D为MgCl2,结合反应①可推知B为NH4Cl,验证符合转化关系,据此解答.
解答 解:C为无色液体,由气体X(X由原电池反应得到,可能是H2)和氧气反应得到,故C应是H2O,X是H2,根据反应⑦可知非金属Y是C.由电解D无水晶体得到A与Cl2,可知D为氯化物且是离子化合物,结合A+B溶液发生原电池反应得到X、D、E,可知B为氯化物,且B是一种盐,受热极易分解,反应生成的H2与E气体,B应水解呈酸性,由转化关系:E→F→G→H,属于常温下气体E的连续氧化得到气体G,在中学阶段中N、S元素化合物符合转化关系,考虑反应①是金属与NH4Cl溶液发生的原电池反应,可推出E为NH3、F为NO、G为NO2,则H为HNO3.(1)中反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,应为Mg与二氧化碳的反应,可推出A为Mg,则D为MgCl2,结合反应①可推知B为NH4Cl,验证符合转化关系,
(1)反应④为Mg与二氧化碳的反应生成MgO与碳,反应方程式为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C,
故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
(2)Mg与石墨作电极,NH4Cl的浓溶液作电解质,构成原电池,Mg为负极,石墨为正极,负极反应:Mg-2e-=Mg2+,正极反应:2NH4++2e-=NH3↑+H2↑,
故答案为:Mg-2e-=Mg2+;2NH4++2e-=NH3↑+H2↑;
(3)从MgCl2溶液制备MgCl2的无水晶体,应注意防止水解,应将D溶液在HCl气流中蒸干,
故答案为:将D溶液在HCl气流中蒸干;
(4)反应②是氨的催化氧化,反应化学方程为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(5)反应⑤是碳与浓硝酸反应生成CO2、NO2、H2O,方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,
故答案为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
点评 本题考查无机物的推断、原电池、金属镁的性质、氮及其化合物的性质,侧重于学生的分析能力和元素化合物知识的综合运用的考查,为高考常见题型,注意把握题给信息,结合转化关系进行推断,(2)为易错点,该原电池实质为铵根离子水解,Mg再与氢离子反应生成氢气,难度中等.

| A. | 氢氟酸 | B. | 浓盐酸 | C. | 溴水 | D. | 碘化银固体 |
NaBr+H2SO4→HBr+NaHSO4
CH3CH2OH+HBr?CH3CH2Br+H2O
CH3CH2CH2CH2OH+HBr?CH3CH2CH2CH2Br+H2O
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br-被浓硫酸氧化为Br2等.有关数据列表如下:
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是减少副产物烯和醚的生成,防止溴离子被浓硫酸氧化为溴单质.(填字母)
a.圆底烧瓶 b.量筒 c.温度计 d.普通漏斗
(2)制备实验中常采用80%的硫酸而不用98%的浓硫酸,其主要原因是减少副产物烯和醚的生成,防止溴离子被浓硫酸氧化为溴单质.
(3)在制备溴乙烷时,采用边反应边蒸出产物的方法,这样有利于平衡向生成溴乙烷的方向移动(或提高乙醇的转化率,提高溴乙烷的产率等);但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是1-溴丁烷的沸点和正丁醇相差较小,正丁醇会随1-溴丁烷同时蒸出.
(4)将制得的1-溴丁烷粗产品置于分液漏斗中,依次加入NaHSO3溶液和水,振荡、静置后,
1-溴丁烷在下层(填“上层”、“下层”或“不分层”),加入NaHSO3溶液的目的是除去产物中杂质溴.
(5)将实验(4)所得的1-溴丁烷粗产品干燥后,进行蒸馏操作,即可得到纯净的1-溴丁烷.
(6)某实验小组在制取1-溴丁烷的实验中所取1-丁醇(CH3CH2CH2CH2OH)7.4g.NaBr13.0g,最终制得1-溴丁烷9.6g,则1-溴丁烷的产率是70%.(保留2位有效数字)
| A. | 乙醇、乙酸都能与钠反应 | |
| B. | 乙醇、乙酸互为同分异构体 | |
| C. | 乙醇、乙酸都是高分子化合物 | |
| D. | 乙醇、乙酸都能使紫色石蕊试液变红色 |
| A. | 2-甲基丙烷 | B. | 环戊烷 | C. | 2,2二甲基丁烷 | D. | 2,2-甲基丙烷 |
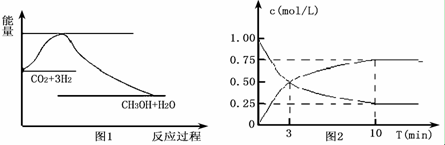
 如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白.
如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白.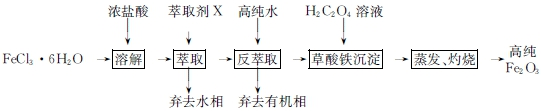
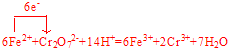 .
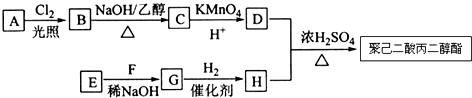
.
 .
. .
.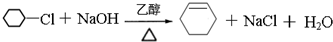 .
.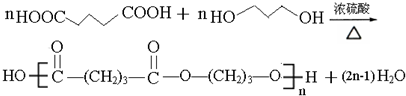 .
.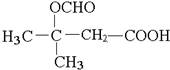 (写出其中一种结构简式).
(写出其中一种结构简式).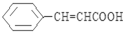 )的合成路线示意图.
)的合成路线示意图.