题目内容
4.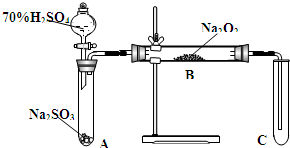 类比思想是化学学习常用的方法.已知Na2O2能与CO2反应,甲同学受到启发,提出一个相似的观点:Na2O2与SO2也能够反应.该同学用如图所示的装置进行实验,充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃.
类比思想是化学学习常用的方法.已知Na2O2能与CO2反应,甲同学受到启发,提出一个相似的观点:Na2O2与SO2也能够反应.该同学用如图所示的装置进行实验,充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃.试回答下列问题:
(1)请写出Na2O2与CO2反应的化学方程式:2Na2O2+2CO2═2Na2CO3+O2.
(2)乙同学认为此装置存在缺陷,请你帮其完成装置的改进并简述理由:
①在A、B之间加一个干燥管,理由产生的二氧化硫没有干燥,水蒸气会与Na2O2反应.
②在B、C之间加一个装有NaOH溶液的洗气瓶,理由除去SO2气体,防止污染空气.
(3)任何的推论都要经过检验,请完成对白色固体成分的探究:限选实验试剂:稀盐酸、硝酸、NaOH稀溶液、蒸馏水、BaCl2溶液、澄清石灰水、品红溶液.
①提出合理假设:假设1:白色固体为Na2SO3;假设2:白色固体为Na2SO3与Na2SO4 的混合物;
假设3:白色固体为Na2SO4 .
②设计实验方案证明以上三种假设,完成下列填空.
步骤1:SO32-检验:取少量白色固体于试管,加入足量的稀盐酸,塞上单孔胶塞,将生成的气体通入品红溶液.
步骤2:SO42-检验:在步骤1反应后的溶液中加入足量的氯化钡溶液.
步骤3:结论:若步骤1现象明显,而步骤2没明显现象,则假设1成立;若步骤1现象不明显,步骤2现象明显,则假设3成立;若上述两个实验现象均有,则假设2成立.
分析 (1)Na2O2与CO2反应生成碳酸钠和氧气;
(2)①装置A是二氧化硫的发生装置,生成的二氧化硫气体中含有水蒸气,AB间需要加一个干燥装置,避免水蒸气的存在与过氧化钠反应影响探究二氧化硫和过氧化钠的反应;
②装置C是验证氧气生成,A中生成的二氧化硫气体是污染性气体,不能排放到空气中;在BC间加一个吸收装置;
(3)①依据类推可知二氧化硫和过氧化钠反应生成亚硫酸钠和氧气,亚硫酸钠和氧气反应可以生成硫酸钠,据此推断白色固体可能的组成;
②利用亚硫酸钠和盐酸反应生成二氧化硫气体验证亚硫酸根离子的存在,依据硫酸根离子和氯化钡溶液反应生成硫酸钡白色沉淀验证硫酸根离子的存在.
解答 解:(1)Na2O2与CO2反应生成碳酸钠和氧气,该反应为2Na2O2+2CO2═2Na2CO3+O2,故答案为:2Na2O2+2CO2═2Na2CO3+O2;
(2)①装置A是二氧化硫的发生装置,生成的二氧化硫气体中含有水蒸气,AB间需要加一个干燥装置,避免水蒸气的存在影响探究二氧化硫和过氧化钠的反应,
故答案为:产生二氧化硫没有干燥,水蒸气会与Na2O2反应;
②装置C是验证氧气生成,A中生成的二氧化硫气体是污染性气体,不能排放到空气中;所以在BC间加一个吸收装置,用一个盛有氢氧化钠溶液的洗气瓶吸收二氧化硫,
故答案为:NaOH;除去SO2气体,防止污染空气;
(3)①依据类推可知二氧化硫和过氧化钠反应生成亚硫酸钠和氧气,亚硫酸钠和氧气反应可以生成硫酸钠,据此推断白色固体可能的组成为:亚硫酸钠、硫酸钠、亚硫酸钠和硫酸钠的混合物,所以假设3为:白色固体为Na2SO4,
故答案为:白色固体为Na2SO4 ;
②依据硫酸根离子和氯化钡溶液反应生成硫酸钡白色沉淀验证硫酸根离子的存在;利用亚硫酸钠和盐酸反应生成二氧化硫气体验证亚硫酸根离子的存在,故答案为:稀盐酸;氯化钡溶液.
点评 本题考查了物质性质的实验设计和实验验证分析判断,题目难度中等,明确二氧化硫、二氧化碳和过氧化钠性质的分析应用是解题关键,试题侧重考查学生的分析、理解能力及知识迁移能力.

 学业测评一课一测系列答案
学业测评一课一测系列答案①C2H2②CCl4③
 ④H2O⑤NH3.
④H2O⑤NH3.| A. | ⑤④③②① | B. | ④⑤②③① | C. | ②⑤④③① | D. | ①③②⑤④ |
| A. | 浓硝酸保存在棕色玻璃试剂瓶中 | |
| B. | 少量的钠保存在煤油中 | |
| C. | 氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中 | |
| D. | FeSO4溶液中加入少量Fe粉和稀盐酸 |
 已知:有机氯化剂磺酰氯SO2Cl2的制法:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0
已知:有机氯化剂磺酰氯SO2Cl2的制法:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0(1)SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H1=akJ/mol
SO2Cl2(g)+SCl2(g)?2SOCl2(g)△H2=bkJ/mol
比较a<b(填<、>、=).
(2)反应速率v与反应物浓度的关系可用实验方法测定,v=k•cm(SO2)•cn (Cl2),k为反应速率常数.根据下述实验结果,求m=1n=1.
| c(SO2)/mol•L-1 | c(Cl2)/mol•L-1 | v/mol•L-1•S-1 |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 8.0k |
A.1-S(bod) B.S(bod) C.1-S(aob) D.S(aob)
(4)若在催化剂作用下,将n molSO2与n molCl2充入容积可变的密闭容器中,并始终保持温度为T,压强为P,起始气体总体积为10L,t min时反应达到平衡,此时气体总体积为8L.
①此温度下,该反应的平衡常数Kp=$\frac{16}{9P}$(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
②相同条件下,若将0.5nmolSO2与0.5nmolCl2充入该容器达平衡状态时,混合物中SO2Cl2的物质的量是0.2n.
(5)SO2Cl2遇水发生剧烈水解生成两种强酸,写出其化学方程式SO2Cl2+2H2O=H2SO4+2HCl.
已知25℃,Ksp(AgCl)=1.8×10-10,Ksp(Ag2SO4)=1.4×10-5,向SO2Cl2溶于水所得溶液中逐滴加入AgNO3溶液,最先生成的沉淀是Cl-,当第二种离子开始沉淀时,溶液中$\frac{{c}^{2}(C{l}^{-})}{c(S{O}_{4}^{2-})}$=2.3×10-15.
| A. | 淀粉→葡萄糖→CO2和H2O(释放能量维持生命活动) | |
| B. | 纤维素→葡萄糖→CO2和H2O(释放能量维持生命活动) | |
| C. | 油脂→甘油和高级脂肪酸→CO2和H2O(释放能量维持生命活动) | |
| D. | 麦芽糖→葡萄糖→CO2和H2O(释放能量维持生命活动) |
| 选项 | X | Y | Z |  |
| A | 含氧酸 | 一元强酸 | HclO4 | |
| B | 易溶碱 | 强碱 | NaOH | |
| C | 盐 | 酸式盐 | NaHCO3 | |
| D | 非电解质 | 氧化物 | CO2 |
| A. | A | B. | B | C. | C | D. | D |
