题目内容
12. 已知:有机氯化剂磺酰氯SO2Cl2的制法:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0
已知:有机氯化剂磺酰氯SO2Cl2的制法:SO2(g)+Cl2(g)?SO2Cl2(g)△H<0(1)SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H1=akJ/mol
SO2Cl2(g)+SCl2(g)?2SOCl2(g)△H2=bkJ/mol
比较a<b(填<、>、=).
(2)反应速率v与反应物浓度的关系可用实验方法测定,v=k•cm(SO2)•cn (Cl2),k为反应速率常数.根据下述实验结果,求m=1n=1.
| c(SO2)/mol•L-1 | c(Cl2)/mol•L-1 | v/mol•L-1•S-1 |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 8.0k |
A.1-S(bod) B.S(bod) C.1-S(aob) D.S(aob)
(4)若在催化剂作用下,将n molSO2与n molCl2充入容积可变的密闭容器中,并始终保持温度为T,压强为P,起始气体总体积为10L,t min时反应达到平衡,此时气体总体积为8L.
①此温度下,该反应的平衡常数Kp=$\frac{16}{9P}$(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
②相同条件下,若将0.5nmolSO2与0.5nmolCl2充入该容器达平衡状态时,混合物中SO2Cl2的物质的量是0.2n.
(5)SO2Cl2遇水发生剧烈水解生成两种强酸,写出其化学方程式SO2Cl2+2H2O=H2SO4+2HCl.
已知25℃,Ksp(AgCl)=1.8×10-10,Ksp(Ag2SO4)=1.4×10-5,向SO2Cl2溶于水所得溶液中逐滴加入AgNO3溶液,最先生成的沉淀是Cl-,当第二种离子开始沉淀时,溶液中$\frac{{c}^{2}(C{l}^{-})}{c(S{O}_{4}^{2-})}$=2.3×10-15.
分析 (1)反应放热反应物的总能量高于生成物总能量,结合盖斯定律分析;
(2)根据v=k•cm(SO2)•cn (Cl2),利用三组数据列式比较可计算m、n值.
(3)由v=$\frac{△c}{△t}$可知,v正与t的乘积为浓度减小量,v逆与t的乘积为浓度增加量,以此分析SO2的平衡浓度;
(4)①平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,压强之比等于物质的量之比;
②将nmolSO2与nmolCl2充入容积可变的密闭容器中,得到SO2Cl2,0.4nmol,则恒压容器中成正比例关系,则0.5nmol二氧化硫和0.5nmolCl2,反应生成SO2Cl20.2nmol;
(5)SO2Cl2遇水发生剧烈水解,且产生白雾,白雾是水解生成HCl与空气中水蒸气结合所致,则-SO2-基团结合2个-OH生成H2SO4;氯化银的溶解度远远小于Ag2SO4的溶解度,SO2Cl2溶于水所得溶液中c(H2SO4):c(HCl)=1:2,溶液中离子浓度为硫酸根离子的2倍,故AgCl最先沉淀,根据溶度积可知,溶液中c(Ag+)=$\frac{{K}_{sp}(AgCl)}{C(C{l}^{-})}$,c(SO42-)=$\frac{{K}_{sp}(A{g}_{2}S{O}_{4})}{{C}^{2}(A{g}^{+})}$,据此计算溶液中$\frac{{c}^{2}(C{l}^{-})}{c(S{O}_{4}^{2-})}$.
解答 解:(1)SO2(g)+Cl2(g)?SO2Cl2(g)△H<0①该反应放热,说明反应物的总能量高于生成物,
SO2(g)+Cl2(g)+SCl2(g)?2SOCl2(g)△H1=akJ/mol②,依据盖斯定律将②-①得SO2Cl2(g)+SCl2(g)?2SOCl2(g)△H2=bkJ/mol③,说明②放出的热量多,③放出的热量少,a、b均为副值,所以a<b,
故答案为:<;
(2)v=k•cm(SO2)•cn (Cl2),设三组数据编号分别为①②③,
则有$\frac{②}{①}$=2m=2,m=1;$\frac{③}{②}$=4n=4,n=1,
故答案为:1;1;
(3)恒温下,若在容积固定的2L密闭容器中,充入SO2、Cl2各2mol,SO2的起始浓度为1mol/L,观察图象,纵坐标为SO2的反应速率,横坐标为时间,由微分法可知,二者之积为浓度,故V(正)×t(平衡)表示B向正反应方向进行时减少的浓度,V(逆)×t(平衡)表示SO2向逆反应方向进行时增大的浓度,故1-S(aob) 的面积表示SO2的平衡浓度,
故答案为:C;
(4)①设反应的二氧化硫物质的量为x,
SO2(g)+Cl2(g)?SO2Cl2(g)
起始量(mol) n n 0
变化量(mol) x x x
平衡量(mol)n-x n-x x
起始气体总体积为10L,t min时反应达到平衡,此时气体总体积为8L,$\frac{2n}{2n-2x+x}$=$\frac{10}{8}$,x=$\frac{2}{5}$n,在一定条件下达到平衡状态时,体系的总压强为P,其中SO2(g)、Cl2(g)、SO2Cl2(g)物质的量分别为0.6nmol、0.6nmol、0.4nmol,压强之比等于物质的量之比,Kp=$\frac{\frac{0.4nmol}{0.6nmol+0.6nmol+0.4nmol}P}{(\frac{0.6nmol}{0.6nmol+0.6nmol+0.4nmol}P)^{2}}$=$\frac{16}{9P}$,
故答案为:$\frac{16}{9P}$;
②将nmolSO2与nmolCl2充入容积可变的密闭容器中,得到SO2Cl2,0.4nmol,则恒压容器中成正比例关系,相同条件下,若将0.5nmolSO2与0.5nmolCl2充入该容器,到达平衡状态时,消耗二氧化硫物质的量为0.2n,混合物中SO2Cl2的物质的量是0.2nmol,
故答案为:0.2n;
(5)SO2Cl2遇水发生剧烈水解,且产生白雾,白雾是水解生成HCl与空气中水蒸气结合所致,则-SO2-基团结合2个-OH生成H2SO4,反应方程式为:SO2Cl2+2H2O=H2SO4+2HCl,Ksp(AgCl)=1.8×10-10,Ksp(Ag2SO4)=1.4×10-5,氯化银的溶解度远远小于Ag2SO4的溶解度,SO2Cl2溶于水所得溶液中c(H2SO4):c(HCl)=1:2,溶液中离子浓度为硫酸根离子的2倍,故AgCl最先沉淀,即最先生成的沉淀是Cl-,当第二种离子SO4 2-开始沉淀时,溶液中c(Cl-)=1×10-5mol/L,c(Ag+)=$\frac{{K}_{sp}(AgCl)}{C(C{l}^{-})}$=$\frac{1.8×1{0}^{-10}}{1×1{0}^{-5}}$=1.8×10-5,c(SO42-)=$\frac{{K}_{sp}(A{g}_{2}S{O}_{4})}{{C}^{2}(A{g}^{+})}$=$\frac{1.4×1{0}^{-5}}{(1.8×1{0}^{-5})^{2}}$,溶液中$\frac{{c}^{2}(C{l}^{-})}{c(S{O}_{4}^{2-})}$=$\frac{(1×1{0}^{-5})^{2}}{\frac{1.4×1{0}^{-5}}{(1.8×1{0}^{-5})^{2}}}$≈2.3×10-15.
故答案为:SO2Cl2+2H2O=H2SO4+2HCl;Cl-;2.3×10-15.
点评 本题考查反应热大小比较、反应速率、化学平衡、溶度积有关计算等,关键是明确原理以及对信息获取应用,需要学生具备扎实的基础与灵活运用的能力,题目难度较大.

①碱性氧化物一定是金属氧化物
②根据是否仅含一种元素分为纯净物与混合物
③酸性氧化物一定是非金属氧化物
④硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
⑤根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸
⑥MgO、Na2O2、CuO、Al2O3是金属氧化物,也是碱性氧化物.
| A. | ① | B. | ③⑤⑥ | C. | ②④⑤ | D. | 全部错误 |
 生物质资源是一种污染小的可再生能源,可由其制得多种化工原料,如甲醛、甲醇和二甲醚等.
生物质资源是一种污染小的可再生能源,可由其制得多种化工原料,如甲醛、甲醇和二甲醚等.(1)已知:①2CH3OH(l)+3O2(g)﹦2CO2(g)+4H2O(g)△H=-1275.6KJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566.0KJ/mol
③H2O(g)=H2O(l)△H=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ•mol-1.
(2)由生物质能获得的CO和H2,可以合成多种有机物.当CO和H2以物质的量之比1:1进行催化反应,其原子利用率达100%,合成的物质可能是cd
a.汽油 b.甲醇 c.甲醛 d.乙酸
(3)工业上合成甲醇的反应:CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ/mol.
①下列对该反应的有关说法不正确的是a
a.当v(CO)=2v(H2)时,该反应处于平衡状态
b.恒温恒压下,容器内气体的密度不再改变时,表明反应达到平衡状态
c.在原平衡体系中充入一定量的氦气,平衡可能发生移动
d.恒温恒压下,改变反应物的投入量,△H的值不发生变化
e.温度一定时,缩小容器的体积,平衡将向右移动,c(CO)将变大
②若在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH平衡时浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 平衡常数 | K1 | K2 | K3 |
| 反应物转化率 | a1 | a2 | a3 |
a.c3>2c1=2c2
b.Q1+Q2=90.8 Q3=2Q1
c.K1=K2=K3
d.a2+a3<100%
(4)CO和H2催化合成二甲醚的反应为:3H2(g)+3CO(g)?CH3OCH3(g)+CO2(g),一定温度下,在1L密闭容器中充入3molH2和3molCO进行反应,若用po表示该体系开始时的总压强,p表示平衡时的总压强,则平衡时CO的转化率为$\frac{3(p-{p}_{0})}{2{p}_{0}}$×100%(用po、p的式子表示)
(5)如图为绿色电源“直接二甲醚燃料电池”工作原理示意图,a电极的反应式为(CH3)2O-12e-+3H2O=2CO2+12H+.
| A. | 0.2 mol | B. | 0.4 mol | C. | 0.8 mol | D. | 0.9 mol |
| A. | 该反应中C失去电子,被还原 | |
| B. | 该反应中氢气得到电子,被还原 | |
| C. | 该反应中,每转移2mole-则生成1mol氢气. | |
| D. | 该反应属于复分解反应 |
| A. | 第三周期第IA族 | B. | 第四周期第IA族 | C. | 第五周期第IA族 | D. | 第二周期第IIA族 |
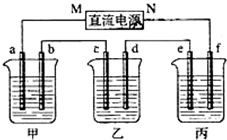 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.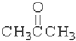 ③
③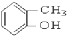 ④
④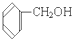 ⑤
⑤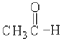 ⑥
⑥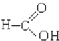
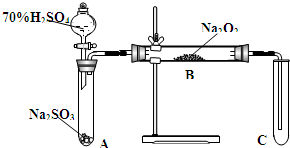 类比思想是化学学习常用的方法.已知Na2O2能与CO2反应,甲同学受到启发,提出一个相似的观点:Na2O2与SO2也能够反应.该同学用如图所示的装置进行实验,充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃.
类比思想是化学学习常用的方法.已知Na2O2能与CO2反应,甲同学受到启发,提出一个相似的观点:Na2O2与SO2也能够反应.该同学用如图所示的装置进行实验,充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃.