题目内容
3.下列说法正确的是( )| A. | 按系统命名法,化合物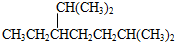 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| B. | 等物质量的苯与苯甲酸完全燃烧消耗氧气的量不相等 | |
| C. | 苯与甲苯互为同系物,均能使高锰酸钾溶液褪色 | |
| D. | 结构片段为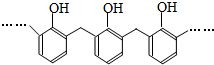 的高聚物,其单体是甲醛和苯酚 的高聚物,其单体是甲醛和苯酚 |
分析 A.该命名不满足取代基的编号之和最小原则;
B.烃CxHy完全燃烧耗氧量由(x+$\frac{y}{4}$)值决定;烃的含氧衍生物CxHyOz完全燃烧耗氧量由(x+$\frac{y}{4}$-$\frac{z}{2}$)值决定,据此判断;
C.苯和甲苯互为同系物,但苯不能使KMnO4酸性溶液褪色;
D.根据苯酚和甲醛发生缩聚反应.
解答 解:A.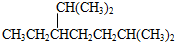 的命名中,选取最长碳原子的碳链为主碳链,离取代基近的一端编号确定支链位置,正确命名为2,6-二甲基-3-乙基庚烷,故A错误;
的命名中,选取最长碳原子的碳链为主碳链,离取代基近的一端编号确定支链位置,正确命名为2,6-二甲基-3-乙基庚烷,故A错误;
B.苯的x+$\frac{y}{4}$=6+$\frac{6}{4}$=7.5,即1mol苯消耗氧气7.5mol,苯甲酸的x+$\frac{y}{4}$=7+$\frac{6}{4}$-1=7.5,即1mol苯甲酸消耗氧气7.5mol,所以等物质的量的苯和苯甲酸完全燃烧消耗氧气的量相等,故B错误;
C.苯和甲苯互为同系物,但苯不能使KMnO4酸性溶液褪色,故C错误;
D.苯酚和甲醛发生缩聚反应得到酚醛树酯,结构片段
故选:D.
点评 本题主要考查了物质的命名、燃烧规律、物质的性质以及缩聚反应,需要注意的是酚醛发生缩聚反应的规律,题目难度中等.

练习册系列答案
相关题目
14.具有如下电子层结构的原子,其相应元素一定属于同一主族的是( )
| A. | 2p能级上只有1个空轨道的原子和3p能级上只有1个空轨道的原子 | |
| B. | 最外层电子排布为3s2的原子和最外层电子排布为4s2的原子 | |
| C. | 最外层电子排布为ns2的原子和最外层电子排布为ns2np6的原子 | |
| D. | 2p能级上有2个未成对电子的原子和3p能级上有2个未成对电子的原子 |
11.短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族.下列说法不正确的是( )
| A. | 原子半径大小顺序:r(Z)>r(W)>r(X)>r(Y) | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物对应水化物的酸性比W的强 | |
| D. | Y的气态简单氢化物的热稳定性比W的强 |
8.已知Ksp[Mg(OH)2]=1.8×10-11 mol3•L-3,则Mg(OH)2在pH=12的NaOH溶液中的溶解度为( )
| A. | 1.8×10-7 mol•L-1 | B. | 1.0×10-5 mol•L-1 | ||
| C. | 1.0×10-7 mol•L-1 | D. | 1.8×10-9 mol•L-1 |
12.用1L某浓度的NaOH溶液吸收一定量的CO2,所得溶液中CO32-与HCO3-物质的量浓度分别为0.5mol/L、0.7mol/L,则c(NaOH)为( )
| A. | 2.0 mol/L | B. | 0.6 mol/L | C. | 1.7 mol/L | D. | 1.2 mol/L |
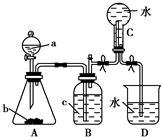 如图装置是某种气体X的制取装置和收集装置(必要时可加热).所用的试剂从下列试剂中选取2~3种:硫化亚铁、二氧化锰、铜屑、氯化铵、稀硝酸、浓盐酸、蒸馏水.请回答下列问题:
如图装置是某种气体X的制取装置和收集装置(必要时可加热).所用的试剂从下列试剂中选取2~3种:硫化亚铁、二氧化锰、铜屑、氯化铵、稀硝酸、浓盐酸、蒸馏水.请回答下列问题: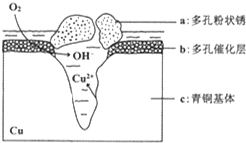 铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题:
铜是一种重要的有色金属,近年来用途越来越广泛.请回答下列问题: