题目内容
12.双安妥明(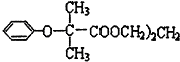 )可用于降低血液中的胆固醇,该物质合成线路如图所示:
)可用于降低血液中的胆固醇,该物质合成线路如图所示: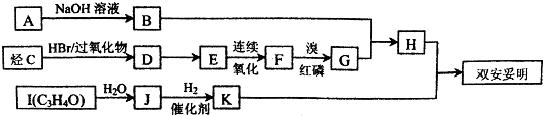
已知:I.RCH2COOH$\stackrel{Br_{2},P}{→}$
 $\stackrel{苯酚钠}{→}$
$\stackrel{苯酚钠}{→}$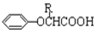
II.RCH-CH2$\stackrel{HBr,过氧化物}{→}$RCH2CH2Br
III.已知:C的密度是同温同压下H2密度的28倍,且支链有一个甲基;I能发生银镜反应且1molI(C3H4O)能与2molH2发生加成反应;K的结构具有对称性.试回答:
(1)A的结构简式
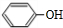 ,J中所含官能团名称为醛基、羟基.
,J中所含官能团名称为醛基、羟基.(2)C的名称为2-甲基-1-丙烯.
(3)反应D→E的化学方程式为CH(CH3)2CH2Br+NaOH$→_{△}^{水}$CH(CH3)2CH2OH+NaBr,反应类型是取代反应.
(4)“H+K→双安妥明”的化学方程式为
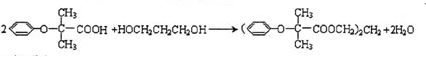 .
.(5)与F互为同分异构体,且属于酯的有机物有4种.其中核磁共振氢谱有三个谱峰,峰面积之比为6:1:1的结构简式为HCOOCH(CH3)2.
分析 由双安妥明的结构 可知,合成双安妥明的物质为HOCH2CH2CH2OH、
可知,合成双安妥明的物质为HOCH2CH2CH2OH、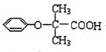 ,I的分子式为C3H4O,经过系列反应生成K,根据C原子数目可知,K为HOCH2CH2CH2OH,I能发生银镜反应,分子中含有-CHO,且1molI能与2mol氢气发生加成反应,说明分子中还含有C=C双键,故I为CH2=CH-CHO,J为HOCH2CH2CHO,H为
,I的分子式为C3H4O,经过系列反应生成K,根据C原子数目可知,K为HOCH2CH2CH2OH,I能发生银镜反应,分子中含有-CHO,且1molI能与2mol氢气发生加成反应,说明分子中还含有C=C双键,故I为CH2=CH-CHO,J为HOCH2CH2CHO,H为 ,B与G反应生成
,B与G反应生成 ,由反应信息I可知,合成H的物质为苯酚钠、BrC(CH3)2COOH,C的密度是同温同压下H2密度的28倍,C的相对分子质量为56,则$\frac{56}{14}$=4,C的分子式为C4H8,且支链有一个甲基,经过系列转化生成G,根据C原子数目可知,G为BrC(CH3)2COOH,故B为苯酚钠,A与氢氧化钠反应生成B,故A为苯酚
,由反应信息I可知,合成H的物质为苯酚钠、BrC(CH3)2COOH,C的密度是同温同压下H2密度的28倍,C的相对分子质量为56,则$\frac{56}{14}$=4,C的分子式为C4H8,且支链有一个甲基,经过系列转化生成G,根据C原子数目可知,G为BrC(CH3)2COOH,故B为苯酚钠,A与氢氧化钠反应生成B,故A为苯酚 ;F在溴/红磷作用下生成G,根据反应信息I,可知F为CH(CH3)2COOH,E连续氧化生成F,故E为CH(CH3)2CH2OH,D转化生成E,D为CH(CH3)2CH2Br,由反应信息II可知,C为C(CH3)2=CH2,据此解答.
;F在溴/红磷作用下生成G,根据反应信息I,可知F为CH(CH3)2COOH,E连续氧化生成F,故E为CH(CH3)2CH2OH,D转化生成E,D为CH(CH3)2CH2Br,由反应信息II可知,C为C(CH3)2=CH2,据此解答.
解答 解:由双安妥明的结构 可知,合成双安妥明的物质为HOCH2CH2CH2OH、
可知,合成双安妥明的物质为HOCH2CH2CH2OH、 ,I的分子式为C3H4O,经过系列反应生成K,根据C原子数目可知,K为HOCH2CH2CH2OH,I能发生银镜反应,分子中含有-CHO,且1molI能与2mol氢气发生加成反应,说明分子中还含有C=C双键,故I为CH2=CH-CHO,J为HOCH2CH2CHO,H为
,I的分子式为C3H4O,经过系列反应生成K,根据C原子数目可知,K为HOCH2CH2CH2OH,I能发生银镜反应,分子中含有-CHO,且1molI能与2mol氢气发生加成反应,说明分子中还含有C=C双键,故I为CH2=CH-CHO,J为HOCH2CH2CHO,H为 ,B与G反应生成
,B与G反应生成 ,由反应信息I可知,合成H的物质为苯酚钠、BrC(CH3)2COOH,C的密度是同温同压下H2密度的28倍,C的相对分子质量为56,则$\frac{56}{14}$=4,C的分子式为C4H8,且支链有一个甲基,经过系列转化生成G,根据C原子数目可知,G为BrC(CH3)2COOH,故B为苯酚钠,A与氢氧化钠反应生成B,故A为苯酚
,由反应信息I可知,合成H的物质为苯酚钠、BrC(CH3)2COOH,C的密度是同温同压下H2密度的28倍,C的相对分子质量为56,则$\frac{56}{14}$=4,C的分子式为C4H8,且支链有一个甲基,经过系列转化生成G,根据C原子数目可知,G为BrC(CH3)2COOH,故B为苯酚钠,A与氢氧化钠反应生成B,故A为苯酚 ;F在溴/红磷作用下生成G,根据反应信息I,可知F为CH(CH3)2COOH,E连续氧化生成F,故E为CH(CH3)2CH2OH,D转化生成E,D为CH(CH3)2CH2Br,由反应信息II可知,C为C(CH3)2=CH2.
;F在溴/红磷作用下生成G,根据反应信息I,可知F为CH(CH3)2COOH,E连续氧化生成F,故E为CH(CH3)2CH2OH,D转化生成E,D为CH(CH3)2CH2Br,由反应信息II可知,C为C(CH3)2=CH2.
(1)通过以上分析知,A的结构简式为: ,J为HOCH2CH2CHO,含有官能团为醛基、羟基,
,J为HOCH2CH2CHO,含有官能团为醛基、羟基,
故答案为: ;醛基、羟基;
;醛基、羟基;
(2)C为C(CH3)2=CH2,名称为:2-甲基-1-丙烯,故答案为:2-甲基-1-丙烯;
(3)反应D→E的化学方程式为:CH(CH3)2CH2Br+NaOH$→_{△}^{水}$CH(CH3)2CH2OH+NaBr,属于取代反应,
故答案为:CH(CH3)2CH2Br+NaOH$→_{△}^{水}$CH(CH3)2CH2OH+NaBr,取代反应;
(4)“H+K→双安妥明”的化学方程式为: ,
,
故答案为: ;
;
(4)F为CH(CH3)2COOH,与F互为同分异构体且属于酯的物质有:甲酸丙酯、甲酸异丙酯、乙酸乙酯、丙酸甲酯,含所以共有4种,其中核磁共振氢谱有三个谱峰,峰面积之比为6:1:1的结构简式为:HCOOCH(CH3)2,
故答案为:4;HCOOCH(CH3)2.
点评 本题考查有机物的推断与合成,要求学生对给予反应信息进行利用,根据双安妥明的结构特点分析合成的原料,再结合正推与逆推相结合进行推断,充分利用反应过程C原子数目,对学生的逻辑推理由较高的要求,难度中等.

 名校课堂系列答案
名校课堂系列答案 下列“试剂”和“试管中的物质”不能完成“实验目的”的是( )
下列“试剂”和“试管中的物质”不能完成“实验目的”的是( )| 实验目的 | 试剂 | 试管中的物质 | |
| A | 羟基对苯环的活性有影响 | 饱和溴水 | ①苯②苯酚溶液 |
| B | 甲基对苯环的活性有影响 | 酸性KMnO4溶液 | ①苯②甲苯 |
| C | 苯分子中没有碳碳双键 | Br2的CCl2溶液 | ①苯②乙烯 |
| D | 碳酸的酸性比苯酚强 | 石蕊溶液 | ①苯酚溶液②碳酸溶液 |
| A. | A | B. | B | C. | C | D. | D |
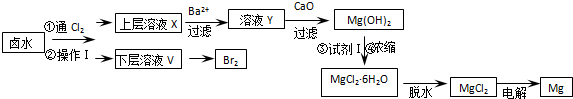
(1)操作Ⅰ的名称是萃取分液,所用主要玻璃仪器的名称是分液漏斗、烧杯.
(2)加入Ba2+的目的是除去溶液中的SO42-.用CaO调节溶液Y的pH,可以使Mg2+沉淀完全.由下表中数据可知,理论上选择pH范围是11.0<PH<12.2.
| 开始沉淀时 | 沉淀完全时 | |
| Mg2+ | pH=9.6 | pH=11.0 |
| Ca2+ | pH=12.2 | c(OH-)=1.8mol/L |
(4)化肥厂生产铵态氮肥(NH4)2SO4的部分流程如图:
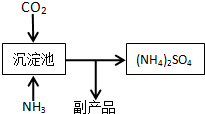
向装有CaSO4悬浊液的沉淀池中先通氨气,再通CO2的原因(请从溶解度和平衡移动角度分析)NH3极易溶于水且溶于水后电离出氢氧根离子,溶液显碱性,增加了二氧化碳的溶解性,生成了更多的CO32-,CO32-离子交换Ca2+形成更难溶的CaCO3,使CaSO4(s)?Ca2+(aq)+SO42-(aq)溶解平衡向右移动,提高(NH4)2SO4的产量.
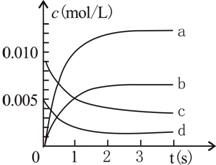 800℃时,在2L密闭容器内加入N0和02,发生反应:2N0(g)+O2(g)?2N02(g),测得n(N0)随时间的变化如表,请回答:
800℃时,在2L密闭容器内加入N0和02,发生反应:2N0(g)+O2(g)?2N02(g),测得n(N0)随时间的变化如表,请回答:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示N02变化的曲线是b;
(3)能说明该反应已达到平衡状态的是ad.
a.容器内气体总物质的量保持不变
b.正反应和逆反应的速率都为0
c.容器内N0、02、N02物质的量之比为2:1:2
d.容器内N0气体的体积分数不变.
| A. | 向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体 | |
| B. | 取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ | |
| C. | 向某无色溶液中加入稀盐酸无现象,再加入BaCl2溶液产生白色沉淀,证明含SO42ˉ | |
| D. | 已知I3-?I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 |
| A. | 电解饱和食盐水可制取金属钠 | |
| B. | 钠与氧气反应的产物与反应条件有关 | |
| C. | 氧化钠与水反应生成氢氧化钠 | |
| D. | 钠可以从四氯化钛中置换出钛 |
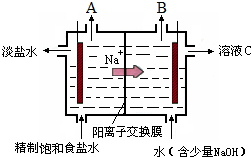 氯碱工业中电解饱和食盐水的原理示意图如图所示:
氯碱工业中电解饱和食盐水的原理示意图如图所示: