题目内容
2.下列属于氧化还原反应的是( )| A. | SO2+H2O═H2SO3 | B. | H2CO3═CO2↑+H2O | ||
| C. | 2NaOH+H2SO4═Na2SO4+2H2O | D. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 |
分析 氧化还原反应的实质为电子转移、特征为化合价升降,所以氧化还原反应中一定存在元素化合价变化,据此对各选项进行判断.
解答 解:A.SO2+H2O═H2SO3,为化合反应,反应中不存在化合价变化,不属于氧化还原反应,故A错误;
B.H2CO3═CO2↑+H2O,为分解反应,反应中不存在化合价变化,不属于氧化还原反应,故B错误;
C.2NaOH+H2SO4═Na2SO4+2H2O,为复分解反应,反应中不存在化合价变化,不属于氧化还原反应,故C错误;
D.C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2为燃烧反应,存在C、O元素化合价变化,属于氧化还原反应,故D正确;
故选D.
点评 本题考查了氧化还原反应的判断,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握四种基本反应类型与氧化还原反应之间的关系,试题有利于提高学生的灵活应用能力.

练习册系列答案
相关题目
15.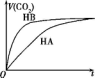 等体积、浓度均为0.2mol•L-1的三种溶液:①HA溶液、②HB溶液、③NaHCO3溶液,已知将①②分别与③混合,实验测得所产生的CO2气体体积(V)随时间(t)变化如图所示.下列说法不正确的是( )
等体积、浓度均为0.2mol•L-1的三种溶液:①HA溶液、②HB溶液、③NaHCO3溶液,已知将①②分别与③混合,实验测得所产生的CO2气体体积(V)随时间(t)变化如图所示.下列说法不正确的是( )
 等体积、浓度均为0.2mol•L-1的三种溶液:①HA溶液、②HB溶液、③NaHCO3溶液,已知将①②分别与③混合,实验测得所产生的CO2气体体积(V)随时间(t)变化如图所示.下列说法不正确的是( )
等体积、浓度均为0.2mol•L-1的三种溶液:①HA溶液、②HB溶液、③NaHCO3溶液,已知将①②分别与③混合,实验测得所产生的CO2气体体积(V)随时间(t)变化如图所示.下列说法不正确的是( )| A. | 酸性:HB>HA>H2CO3 | |
| B. | 反应结束后所得两溶液中:c(A-)>c(B-) | |
| C. | 上述三种溶液中由水电离的c(OH-)相对大小:NaHCO3>HA>HB | |
| D. | HA溶液和NaHCO3溶液反应所得的溶液中:c(A-)+c(HA)=0.1 mol•L-1 |
10.下列说法正确的是( )
| A. | 只含一种分子的物质是纯净物,只含一种元素的物质也是纯净物 | |
| B. | 医疗上的血液透析利用了胶体的性质 | |
| C. | NH3溶于水后所得的溶液可以导电,所以NH3为电解质 | |
| D. | 从海水中可以得到NaCl,电解NaCl溶液可制备Na |
17.在1.01×105Pa下,完全燃烧1体积乙醇和乙烯的混合气体,需同温同压下的氧气( )
| A. | 6体积 | B. | 4体积 | C. | 3体积 | D. | 无法确定 |
14.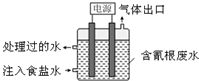 某些工业废水中常是含有氰根(CN-)的无机物,有一定的毒性,有的还是剧毒.图所示装置是工业上采用的电解法除去含CN-废水的装置.工作时控制溶液为碱性,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列叙述不正确的是( )
某些工业废水中常是含有氰根(CN-)的无机物,有一定的毒性,有的还是剧毒.图所示装置是工业上采用的电解法除去含CN-废水的装置.工作时控制溶液为碱性,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列叙述不正确的是( )
 某些工业废水中常是含有氰根(CN-)的无机物,有一定的毒性,有的还是剧毒.图所示装置是工业上采用的电解法除去含CN-废水的装置.工作时控制溶液为碱性,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列叙述不正确的是( )
某些工业废水中常是含有氰根(CN-)的无机物,有一定的毒性,有的还是剧毒.图所示装置是工业上采用的电解法除去含CN-废水的装置.工作时控制溶液为碱性,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列叙述不正确的是( )| A. | 用石墨作阴极,铁作阳极 | |
| B. | 阴极的电极反应式为:2H2O+2e-=H2↑+2OH- | |
| C. | 阳极的电极反应式为:Cl-+2OH--2e-=ClO-+H2O | |
| D. | 除去CN-的反应:2CN-+5ClO-+H2O=N2↑+2CO2↑+5Cl-+2OH- |
11.下列实验操作或结论正确的是( )
| A. | 配制一定物质的量浓度的溶液时,容量瓶必须洁净、干燥,不漏水 | |
| B. | 实验室里需要480 mL 2.0 mol/L的氢氧化钠溶液,配制该溶液时先称量氢氧化钠固体38.4 g,然后再按照溶解、冷却、移液、定容、摇匀的步骤进行操作 | |
| C. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液的浓度偏大 | |
| D. | 实验室配制500 mL 0.2 mol/L的硫酸亚铁溶液,其操作是用天平称量27.8 g绿矾,将其放入500 mL容量瓶,加水溶解、稀释、定容、摇匀 |
12.不用任何试剂鉴别硫酸、硫酸钠、碳酸钠、氯化钡四种无色溶液,将它们两两混合现象如下:
由表可知:
( 1)B为BaCl2;C为Na2SO4(填化学式)
(2)要确定A、D还要进行的实验操作是:在A、D溶液中分别加入稀盐酸,若有生成气体现象,证明是Na2CO3(填化学式)
(3)写出A和D反应的离子方程式:CO32-+2H+=CO2↑+H2O.
| A | B | C | D | |
| A | -- | 白色沉淀 | 无现象 | 无色气体 |
| B | 白色沉淀 | -- | 白色沉淀 | 白色沉淀 |
| C | 无现象 | 白色沉淀 | -- | 无现象 |
| D | 无色气体 | 白色沉淀 | 无现象 | -- |
( 1)B为BaCl2;C为Na2SO4(填化学式)
(2)要确定A、D还要进行的实验操作是:在A、D溶液中分别加入稀盐酸,若有生成气体现象,证明是Na2CO3(填化学式)
(3)写出A和D反应的离子方程式:CO32-+2H+=CO2↑+H2O.
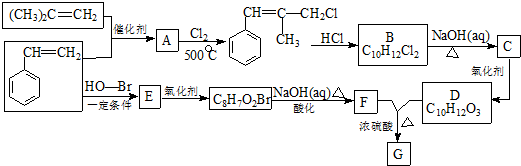
 .
.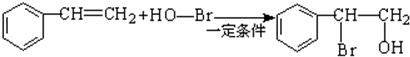 .
.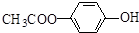 和
和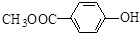 .
.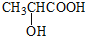 ) 的合成路线:
) 的合成路线: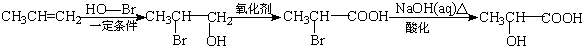 .
.