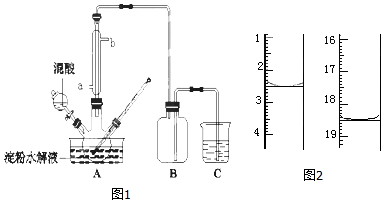
题目内容
3.氯原子核外有17种不同运动状态的电子,它的最外层电子排布式是3s23p5.分析 Cl元素为17号元素,原子核外有17个电子,每一个电子的运动状态都不相同,其核外电子排布为1s22s22p63s23p5,据此分析.
解答 解:Cl元素为17号元素,原子核外有17个电子,每一个电子的运动状态都不相同,所以氯原子核外有17种不同运动状态的电子,Cl原子的核外电子排布为1s22s22p63s23p5,则最外层电子排布式是3s23p5;
故答案为:17;3s23p5.
点评 本题考查了原子核外电子的运动状态、核外电子排布式,题目难度不大,侧重于基础知识的考查,注意把握核外电子排布式的书写方法.

练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
13.化合物X是一种医药中间体,其结构简式如图所示.下列有关X的说法正确的是( )
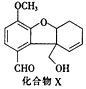

| A. | 分子中含2个手性碳原子 | |
| B. | 分子中所有碳原子均处于同一平面 | |
| C. | 能发生银镜反应,不能发生酯化反应 | |
| D. | 1molX最多能与4molH2发生加成反应 |
14.下列有关同位素的说法正确的是( )
| A. | 18O的中子数为8 | B. | 16O和18O质子数相差2 | ||
| C. | 16O与18O核电荷数相等 | D. | 1个16O与1个18O质量相等 |
11.下列离子方程式与所述事实相符且正确的是( )
| A. | 钠与水反应:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 纯碱溶液去油污:CO32-+H2O═HCO3-+OH- | |
| C. | Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+═SO42-+3S↓+2H2O | |
| D. | 明矾溶液中加入过量的氢氧化钡溶液:Al3++SO42-+Ba2++4OH-═BaSO4↓+AlO2-+2H2O |
18.设NA为阿伏加德罗常数值.下列有关叙述正确的是( )
| A. | 10.7gNH4C1中含有的共用电子对数为NA | |
| B. | 0.5mol•L-1CH3COONa溶液中含有CH3COO-的数目少于0.5 NA | |
| C. | 22gN2O和22gCO2所含有的质子数均为11NA | |
| D. | 足量的镁与一定量的浓硫酸充分反应,放出2.24LSO2和H2混合气体时,转移电子数为0.2NA |
8.下列关于乙炔的化学用语正确的是( )
| A. | 摩尔质量:26 | B. | 球棍模型: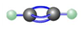 | C. | 电子式: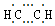 | D. | 结构式:CH≡CH |
16.因存在浓度差而产生电动势的电池称为浓差电池.利用如图所示装置进行实验,开始先闭合K2,断开Kl,一段时间后,再断开K2,闭合Kl,形成浓差电池,电流计指针偏转(Ag+浓度越大,氧化性越强).下列说法不正确的是( )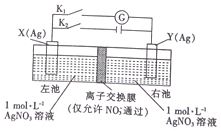

| A. | 闭合K2,断开Kl一段时间后,X电极质量增加 | |
| B. | 闭合K2,断开Kl一段时间后,右池c(AgNO3)增大 | |
| C. | 断开K2,闭合K1,X 电极发生氧化反应 | |
| D. | 断开K2,闭合K1,NO3-从左池向右池移动 |
17.下列反应中,光照对反应几乎没有影响的是( )
| A. | 氯气与氢气反应 | B. | 次氯酸分解 | C. | 甲烷与氯气反应 | D. | 氢气与氮气反应 |