题目内容
17.下列反应中,光照对反应几乎没有影响的是( )| A. | 氯气与氢气反应 | B. | 次氯酸分解 | C. | 甲烷与氯气反应 | D. | 氢气与氮气反应 |
分析 选项中只有氮气与氢气光照下不反应,需要在催化剂、高温、高压下反应,以此来解答.
解答 解:A.氯气与氢气反应生成HCl,光照下反应剧烈,可能发生爆炸,故A不选;
B.HClO光照分解生成HCl和氧气,故B不选;
C.甲烷与氯气光照下发生取代反应,故C不选;
D.氢气与氮气反应条件为催化剂、高温、高压,光照不反应,故D选;
故选D.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.某化学研究性学习小组用CO还原Fe2O3,并在实验结束后用磁铁吸出生成的黑色粉末X进行探究.
[探究目的]分析黑色粉末X的组成,并进行相关实验.
[查阅资料]
I.CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引.
II.Fe3O4+8H+=2Fe3++Fe2++4H2O
[猜想假设]黑色粉末X的组成可能是Fe、Fe3O4,或二者的混合物.
[实验探究]
(1)实验①中产生气泡的离子方程式为Fe+2H+═Fe2++H2↑.
(2)根据②中溶液未呈红色,不能推断出黑色粉末X中无Fe3O4,请用离子方程式解释原因:Fe3O4+8H+═2Fe3++Fe2++4H2O、Fe+2Fe3+═3Fe2+.
(3)为了证明黑色粉末X中是否含有Fe3O4,该小组进行如图所示实验:

请根据数据分析说明黑色粉末X中是否含有Fe3O4.方法1:因为32gFe2O3中含Fe元素为22.4g,而25.6g>22.4g,所以X中还含有O元素,还含有Fe3O4;
方法2:因为产生产生4.48L氢气,需要Fe单质为11.2g,而25.6g>11.2g,所以X中还含有Fe3O4.
[探究目的]分析黑色粉末X的组成,并进行相关实验.
[查阅资料]
I.CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引.
II.Fe3O4+8H+=2Fe3++Fe2++4H2O
[猜想假设]黑色粉末X的组成可能是Fe、Fe3O4,或二者的混合物.
[实验探究]
| 编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管中,注入足量的一定浓度的盐酸,微热 | 黑色粉末逐渐溶解,同时有气泡产生,溶液呈浅绿色. |
| ② | 向上述试管中滴加几滴KSCN溶液,振荡 | 溶液没有呈现红色 |
(2)根据②中溶液未呈红色,不能推断出黑色粉末X中无Fe3O4,请用离子方程式解释原因:Fe3O4+8H+═2Fe3++Fe2++4H2O、Fe+2Fe3+═3Fe2+.
(3)为了证明黑色粉末X中是否含有Fe3O4,该小组进行如图所示实验:

请根据数据分析说明黑色粉末X中是否含有Fe3O4.方法1:因为32gFe2O3中含Fe元素为22.4g,而25.6g>22.4g,所以X中还含有O元素,还含有Fe3O4;
方法2:因为产生产生4.48L氢气,需要Fe单质为11.2g,而25.6g>11.2g,所以X中还含有Fe3O4.
12.下列关于有机物的叙述中
①乙烯、聚氯乙烯和苯分子中均含有碳碳双键
②苯、油脂均不能使酸性KMnO4溶液褪色
③氯苯分子中所有原子都处于同一平面
④甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种.
⑤一定条件下,乙酸乙酯、葡萄糖、蛋白质都能与水发生水解反应
⑥
⑦一定条件下,完全燃烧14g含氧质量分数为a的乙烯、乙醛混合气体,生成水的质量为18(1-a)g
其中全部不正确的是( )
①乙烯、聚氯乙烯和苯分子中均含有碳碳双键
②苯、油脂均不能使酸性KMnO4溶液褪色
③氯苯分子中所有原子都处于同一平面
④甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种.
⑤一定条件下,乙酸乙酯、葡萄糖、蛋白质都能与水发生水解反应
⑥

⑦一定条件下,完全燃烧14g含氧质量分数为a的乙烯、乙醛混合气体,生成水的质量为18(1-a)g
其中全部不正确的是( )
| A. | ①③⑥⑦ | B. | ③④⑤⑥ | C. | ①②④⑤ | D. | ①⑤⑥⑦ |
2.NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的 催化剂研究催化剂常具有较强的选择性,即专一性.已知:
反应 I:4NH3(g)+5O2(g)$\stackrel{PtRu}{?}$4NO(g)+6H2O(g)△H=-905.0kJ•mol-1
反应 II:4NH3(g)+3O2(g)$?_{高温}^{CU/TiO_{2}}$2N2(g)+6H2O(g)△H
(1)
△H=-1260KJ/mol.
(2)在恒温恒容装置中充入一定量的 NH3 和 O2,在某催化剂的作用下进行反应 I,则下 列有关叙述中正确的是A.
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内 4v 正(NH3)=6v 逆(H2O)时,说明反应已达平衡
C.当容器内 $\frac{n(NO)}{n(N{H}_{3})}$=1 时,说明反应已达平衡
(3)氨催化氧化时会发生上述两个竞争反应 I、II.为分析某催化剂对该反应的选择性,在 1L 密闭容器中充入 1mol NH3和 2mol O2,测得有关物质的量关系如图:
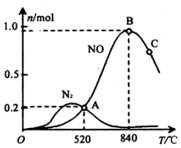
①该催化剂在高温时选择反应I(填“I”或“II”).
②520℃时,4NH3(g)+5O2?4NO(g)+6H2O(g)的平衡常数K=$\frac{0.{2}^{4}×0.{9}^{6}}{0.{4}^{4}×1.4{5}^{5}}$(不要求得出计算结果,只需列出数字计算式).
③有利于提高 NH3 转化为 N2 平衡转化率的措施有E
A.使用催化剂 Pt/Ru
B.使用催化剂 Cu/TiO2
C.增大 NH3和 O2 的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
(4)采用氨水吸收烟气中的 SO2,
①若氨水与 SO2恰好完全反应生成正盐,则此时溶液呈碱性(填“酸”或“碱”). 常温下弱电解质的电离平衡常数如下:氨水:Kb=1.8×10-5mol•L-1;H2SO3:Ka1=1.3×10-2mol•L-1,Ka2=6.3×10-8mol•L-1
②上述溶液中通入SO2(填“SO2”或 NH3”)气体可使溶液呈中性,此时溶液中$\frac{c{(NH}_{4}^{+})}{c(S{{O}_{3}}^{2-})}$>2(填“>”“<”或“=”)
反应 I:4NH3(g)+5O2(g)$\stackrel{PtRu}{?}$4NO(g)+6H2O(g)△H=-905.0kJ•mol-1
反应 II:4NH3(g)+3O2(g)$?_{高温}^{CU/TiO_{2}}$2N2(g)+6H2O(g)△H
(1)
| 化学键 | H-O | O=O | N≡N | N-H |
| 键能KJ•mol-1 | 463 | 496 | 942 | 391 |
(2)在恒温恒容装置中充入一定量的 NH3 和 O2,在某催化剂的作用下进行反应 I,则下 列有关叙述中正确的是A.
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内 4v 正(NH3)=6v 逆(H2O)时,说明反应已达平衡
C.当容器内 $\frac{n(NO)}{n(N{H}_{3})}$=1 时,说明反应已达平衡
(3)氨催化氧化时会发生上述两个竞争反应 I、II.为分析某催化剂对该反应的选择性,在 1L 密闭容器中充入 1mol NH3和 2mol O2,测得有关物质的量关系如图:

①该催化剂在高温时选择反应I(填“I”或“II”).
②520℃时,4NH3(g)+5O2?4NO(g)+6H2O(g)的平衡常数K=$\frac{0.{2}^{4}×0.{9}^{6}}{0.{4}^{4}×1.4{5}^{5}}$(不要求得出计算结果,只需列出数字计算式).
③有利于提高 NH3 转化为 N2 平衡转化率的措施有E
A.使用催化剂 Pt/Ru
B.使用催化剂 Cu/TiO2
C.增大 NH3和 O2 的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
(4)采用氨水吸收烟气中的 SO2,
①若氨水与 SO2恰好完全反应生成正盐,则此时溶液呈碱性(填“酸”或“碱”). 常温下弱电解质的电离平衡常数如下:氨水:Kb=1.8×10-5mol•L-1;H2SO3:Ka1=1.3×10-2mol•L-1,Ka2=6.3×10-8mol•L-1
②上述溶液中通入SO2(填“SO2”或 NH3”)气体可使溶液呈中性,此时溶液中$\frac{c{(NH}_{4}^{+})}{c(S{{O}_{3}}^{2-})}$>2(填“>”“<”或“=”)
9.下列有关说法正确的是( )
| A. | NaOH是只含离子键的离子化合物 | |
| B. | HCl溶于水没有破坏共价键 | |
| C. | 碳在O2中燃烧时,破坏碳和O2中化学键吸收的总能量大于形成CO2中化学键释放的总能量 | |
| D. | 在Cl2+2NaBr=2NaCl+Br2反应过程中有离子键和共价键的断裂,也有离子键和共价键形成 |
6.下列事实不能说明X元素比Y元素的非金属性强的是( )
| A. | 与H2化合时X单质比Y单质容易 | |
| B. | X的最高价氧化物的水化物的酸性比Y的最高价氧化物的水化物的酸性强 | |
| C. | 在氧化还原反应中,甲失的电子比乙多 | |
| D. | X单质可以把Y从其氢化物中置换出来 |

 $→_{H+}^{KMnO_{4}}$
$→_{H+}^{KMnO_{4}}$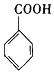
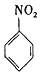 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$ (苯胺,易被氧化)
(苯胺,易被氧化) .
. .
. .
. 最合理的方案(不超过3步).
最合理的方案(不超过3步). $→_{反应条件}^{反应物}$…$→_{反应条件}^{反应物}$
$→_{反应条件}^{反应物}$…$→_{反应条件}^{反应物}$