题目内容
8.某学生为了证明HCl溶液能使石蕊试液变红的微粒是H+,他所设计的下列实验中,没有意义的是( )①向滴有石蕊试液的盐酸中滴入硝酸银溶液至过量,观察溶液颜色的变化
②向稀盐酸、释硫酸、稀硝酸中分别滴入几滴石蕊试液,观察溶液颜色的变化
③向氯化钠溶液中滴人几滴石蕊试液,观察溶液颜色的变化
④向盐酸中加人碳酸钠溶液至不再冒出气泡,再滴入几滴石蕊试液,观察溶液颜色的变化
⑤向盐酸中加少量蒸馏水稀释,再滴入石蕊试液,观察溶液颜色的变化.
| A. | ①④ | B. | ②③ | C. | ⑤ | D. | ③④⑤ |
分析 证明HCl溶液能使石蕊试液变红的微粒是H+,可分别对氢离子和氯离子的性质进行探究,以此解答该题.
解答 解:①向滴有石蕊试液的盐酸中滴入硝酸银溶液至过量,观察溶液颜色的变化,氯离子参加反应,反应后呈酸性,能说明使石蕊试液变红的微粒是H+;
②稀盐酸、释硫酸、稀硝酸都含有氢离子,分别滴入几滴石蕊试液,观察溶液颜色的变化,可证明使石蕊试液变红的微粒是H+;
③向氯化钠溶液中滴人几滴石蕊试液,观察溶液颜色的变化,可证明氯离子不能使石蕊试液变红;
④向盐酸中加人碳酸钠溶液至不再冒出气泡,反应后呈中性或弱碱性,再滴入几滴石蕊试液,溶液不变红,可说明;
⑤向盐酸中加少量蒸馏水稀释,氢离子和氯离子浓度都降低,再滴入石蕊试液,观察溶液颜色的变化,不能证明.
故选C.
点评 本题考查物质的性质实验设计,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的严密性和可行性的评价,难度不大.

练习册系列答案
相关题目
14.某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,SO42-的物质的量浓度为9mol/L,加入足量铁粉,则反应后的溶液中Fe2+离子浓度为(假设反应前后溶液体积不变)( )
| A. | 4.5mol/L | B. | 18mol/L | C. | 3mol/L | D. | 9mol/L |
15.分类是化学学习与研究的常用方法,下列分类正确的是( )
| A. | SiO2、SO2、SO3均属于酸性氧化物 | |
| B. | H2SiO3、H2SO3、H2SO4均属于强酸 | |
| C. | 根据是否具有丁达尔效应,将分散系分为溶液、胶体和浊液 | |
| D. | 根据是否能导电,将物质分为电解质和非电解质 |
12.下列关于有机物的说法中正确的是( )
| A. | 2013年11月山东现“夺命快递”--化学品泄漏致1死7中毒.该化学品为氟乙酸甲酯,它是一种无色透明液体,不溶于水,易溶于乙醇、乙醚.它属于酯类,也属于卤代烃 | |
| B. | 酸性高锰酸钾溶液既可以用来鉴别甲烷和乙烯,也可以用来除去甲烷中的乙烯 | |
| C. | 已烷可以使溴水褪色是因为发生了取代反应 | |
| D. | 某种醇在适当条件下与足量的乙酸发生酯化反应,生成的酯的相对分子质量a与原来醇的相对分子量b的关系是a=b+84,则该醇分子中具有两个醇羟基 |
13.以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+等金属离子,通过添加过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀.根据上述实验事实,下列说法中,不正确的是( )
| A. | 溶解度 MnS<PbS | |
| B. | MnS存在沉淀溶解平衡 MnS(s)?Mn2+(aq)+S2-(aq) | |
| C. | Cu2+转化为沉淀的原理为 MnS(s)+Cu2+(aq)═CuS(s)+Mn2+(aq) | |
| D. | 沉淀转化能用于除去溶液中的某些杂质离子 |
17.2016杭州G20峰会期间,夜晚的空中被激光照射出美丽的光束,产生此现象主要是因为大气中存在( )
| A. | 纯净物 | B. | 溶液 | C. | 胶体 | D. | 浊液 |
18.下列物质中,既能发生水解反应又能发生氢化反应的是( )
| A. | 甘油 | B. | 植物油 | C. | 乙酸乙酯 | D. | 高级脂肪酸 |
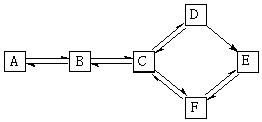 有A、B、C、D、E、F六种有机化合物,存在下图所示转化关系.已知A属于烃,且相对分子质量不超过30;在加热条件下,B可与氢氧化钠溶液反应,向反应后所得液中加入过量的硝酸,再加入硝酸银溶液,生成淡黄色沉淀.
有A、B、C、D、E、F六种有机化合物,存在下图所示转化关系.已知A属于烃,且相对分子质量不超过30;在加热条件下,B可与氢氧化钠溶液反应,向反应后所得液中加入过量的硝酸,再加入硝酸银溶液,生成淡黄色沉淀. 氨和硝酸都是重要的工业原料.
氨和硝酸都是重要的工业原料.