题目内容
15.分类是化学学习与研究的常用方法,下列分类正确的是( )| A. | SiO2、SO2、SO3均属于酸性氧化物 | |
| B. | H2SiO3、H2SO3、H2SO4均属于强酸 | |
| C. | 根据是否具有丁达尔效应,将分散系分为溶液、胶体和浊液 | |
| D. | 根据是否能导电,将物质分为电解质和非电解质 |
分析 A.和碱反应生成铵和水的氧化物为酸性氧化物;
B.水溶液中电离出的阳离子全部是氢离子的化合物为酸,水溶液中全部电离的酸为强酸;
C.分散系的本质特征为分散质微粒直径大小,丁达尔现象为性质;
D.水溶液中或熔融状态下导电的化合物为电解质,水溶液中和熔融状态下都不导电的化合物为非电解质.
解答 解:A.SiO2、SO2、SO3均和碱反应生成盐和水属于酸性氧化物,故A正确;
B.H2SiO3、H2SO3均属于弱酸,H2SO4是强酸,故B错误;
C.根据分散质微粒直径大小,将分散系分为溶液、胶体和浊液,故C错误;
D.根据化合物在水溶液中或熔融状态是否能导电,将物质分为电解质和非电解质,故D错误;
故选A.
点评 本题考查了物质分类、物质性质、分散系分类、电解质非电解质概念等知识点,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
5.下列物质的电子式书写正确的是( )
| A. | Na2O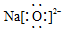 | B. | H2S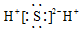 | C. | H2O2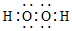 | D. | N2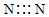 |
6.下列物质中,属于共价化合物的是( )
| A. | BaCl2 | B. | NaOH | C. | Br2 | D. | HF |
3.化学与生活密切相关,下列说法正确的是( )
| A. | 甘油和植物油都属于油脂 | |
| B. | 柠檬有酸味,属于酸性食物 | |
| C. | 食品中的抗氧化剂不能起到防腐作用 | |
| D. | 残留有少量食盐水的铁锅易生锈,因为发生了电化学腐蚀 |
10.某无色溶液中可能含有Na+、NH4+、Ba2+、Cu2+、SO42-、SO32-、Cl-、Br-、CO32-中的若干种.为检验其中含有的离子,进行如下实验:
①取10mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体.
下列关于原溶液的说法正确的是( )
①取10mL溶液,加入足量氯水,无气体产生,再加入CCl4溶液分层,下层为橙红色;
②分液后,将①中上层溶液加入足量BaCl2和HCl溶液,产生白色沉淀2.33g;
③另取10mL原溶液,加入过量的浓氢氧化钠溶液并加热,收集到标准状况下448mL气体.
下列关于原溶液的说法正确的是( )
| A. | 肯定存在NH4+、Cl-、Br- | |
| B. | 是否存在Na+需要通过焰色反应来确定 | |
| C. | SO42-、SO32-至少含有一种 | |
| D. | 肯定不存在Ba2+、Cu2+、SO32-、CO32- |
20.能正确表示下列反应的离子反应方程式为( )
| A. | 钠投入足量水中:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 氯气溶于水:Cl2+H2O=2H++Cl-+ClO- | |
| C. | 向明矾溶液中滴加过量Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| D. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O |
9.将下列各组物质分别同时加入到水中,能大量共存且得到无色透明溶液的是( )
| A. | CaCl2 HCl KNO3 | B. | K2SO4 BaCl2 NaOH | ||
| C. | NaOH H2SO4 MgSO4 | D. | Fe2O3 CuSO4 NaCl |