题目内容
14.某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,SO42-的物质的量浓度为9mol/L,加入足量铁粉,则反应后的溶液中Fe2+离子浓度为(假设反应前后溶液体积不变)( )| A. | 4.5mol/L | B. | 18mol/L | C. | 3mol/L | D. | 9mol/L |
分析 足量的Fe与CuSO4、Fe2(SO4)3、H2SO4的混合溶液反应最终得到FeSO4,由元素守恒可知,可知n(Fe)=n(FeSO4)=n(SO42-),再根据c=$\frac{n}{V}$计算Fe2+离子浓度.
解答 解:足量的Fe与CuSO4、Fe2(SO4)3、H2SO4的混合溶液反应最终得到FeSO4,由元素守恒可知,可知n(Fe)=n(FeSO4)=n(SO42-)=9mol/L×0.1L=0.9mol,所以反应后的溶液中Fe2+离子浓度为$\frac{0.9mol}{0.1L}$=9mol/L,故选D.
点评 本题考查化学方程式有关计算,难度中等,关键是明确足量的Fe与硫酸铁反应得到Fe,注意利用守恒思想解答,简化计算步骤.

练习册系列答案
相关题目
5.下列物质的电子式书写正确的是( )
| A. | Na2O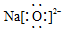 | B. | H2S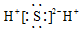 | C. | H2O2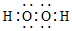 | D. | N2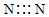 |
9.在实验中,下列说法不正确的是( )
| A. | 制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 | |
| B. | 可以不用任何试剂就可以鉴别AlCl3和NaOH、Na2CO3和HCl、NaAlO2和HCl | |
| C. | 除去CO2气体中混有的少量SO2可以将气体通入KMnO4溶液中或饱和NaHCO3溶液 | |
| D. | H2在Cl2中燃烧火焰呈淡蓝色 |
6.下列物质中,属于共价化合物的是( )
| A. | BaCl2 | B. | NaOH | C. | Br2 | D. | HF |
3.化学与生活密切相关,下列说法正确的是( )
| A. | 甘油和植物油都属于油脂 | |
| B. | 柠檬有酸味,属于酸性食物 | |
| C. | 食品中的抗氧化剂不能起到防腐作用 | |
| D. | 残留有少量食盐水的铁锅易生锈,因为发生了电化学腐蚀 |
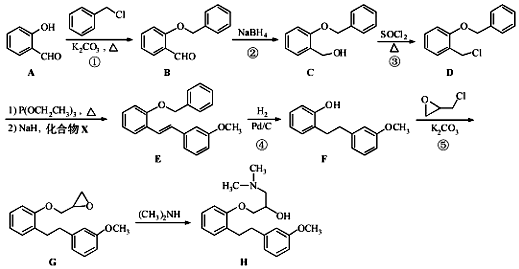
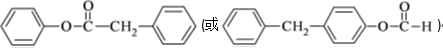 .
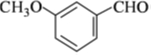
.
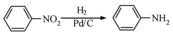 .化合物
.化合物 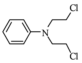 是合成抗癌药物美法伦的中间体,请写出以
是合成抗癌药物美法伦的中间体,请写出以 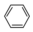 和
和  为原料制备该化合物的合成路线流程图(无机试剂任用).
为原料制备该化合物的合成路线流程图(无机试剂任用).