题目内容
17.某基态原子第四能层上有1个电子,该原子可能为K、Cr、Cu.分析 根据构造原理知,4s能级大于3p能级而小于3d能级,原子核外电子排列时要遵循能量最低原理,所以排列电子时先排列3p能级再4s能级后排3d能级,且当轨道上电子处于全空、全满或半满时最稳定,以此解答该题.
解答 解:基态原子第四能层上有1个电子,则3d能级电子数可能为0、5、10,如为0,则为K,如为5,则为Cr,如为10,则为Cu,故答案为:K、Cr、Cu.
点评 本题考查原子结构和元素性质,侧重考查分析推断能力,根据构造原理来分析解答即可,注意Cr和Cu基态原子核外电子排布式的书写特点,为易错点.

练习册系列答案
相关题目
8.工业上利用反应2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑冶炼硅单质,有关叙述错误的是( )
| A. | 每当固体质量减轻5.6g时,生成2.8g Si | |
| B. | 氧化剂和还原剂的物质的量之比为1:2 | |
| C. | 硅单质在常温下不与任何酸、碱反应 | |
| D. | 单质硅与单质碳均具有一定的还原性 |
12.几种前四周期元素的原子半径及主要化合价如表所示:下列叙述正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/pm | 160 | 143 | 102 | 56 | 117 |
| 主要化合价 | +2 | +3 | +6,+4,-2 | -1 | +6,+4,-2 |
| A. | 元素A和B的最高价氧化物均可用作耐火材料 | |
| B. | 由元素B,C组成的化合物可以通过单质与单质化合制得,也可以在溶液中通过复分解反应制得 | |
| C. | 气态氢化物的还原性:C>E | |
| D. | D元素的非金属性最强,其最高价氧化物对应水化物的酸性最强 |
2.下列有关氢元素的叙述正确的是( )
| A. | ${\;}_{\;}^{1}$H(氕)、${\;}_{\;}^{2}$H(氘)、${\;}_{\;}^{3}$H(氚)是三种氢元素 | |
| B. | 所有氢元素粒子的核外都只有一个电子 | |
| C. | 所有氢元素粒子的化学性质都相同 | |
| D. | 能用符号H表示的原子在元素周期表中的位置相同 |
3.下列实验或操作能达到目的是( )
| A. | 用AgNO3溶液鉴别KCl溶液和MgCl2溶液 | |
| B. | 用BaCl2溶液鉴别Na2CO3溶液与Na2SO4溶液 | |
| C. | 用加热、称重的方法鉴别NaCl固体和Ca(HCO3)2固体 | |
| D. | 检验某溶液中是否含有H+时,可滴入少量的酚酞试液 |
20.为达到预期的实验目的,下列操作正确的是( )
| A. | 配制0.1mol/L的盐酸500mL,应选用的仪器有胶头滴管、烧杯、玻璃棒、天平、500mL容量瓶 | |
| B. | 欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 | |
| C. | 为鉴别KCl、AlCl3和MgCl2溶液,分别向三种溶液中滴加NaOH溶液至过量 | |
| D. | 测定硫酸铜晶体中结晶水含量,加热坩埚中晶体完全失水后需在空气中冷却,再称量 |
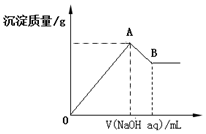 在含有0.60molCl-、0.80molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定浓度NaOH溶液,产生沉淀情况如图(不考虑Mg2+和Al3+水解及水电离对离子数目的影响).若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x.
在含有0.60molCl-、0.80molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定浓度NaOH溶液,产生沉淀情况如图(不考虑Mg2+和Al3+水解及水电离对离子数目的影响).若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x.