题目内容
8.工业上利用反应2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑冶炼硅单质,有关叙述错误的是( )| A. | 每当固体质量减轻5.6g时,生成2.8g Si | |
| B. | 氧化剂和还原剂的物质的量之比为1:2 | |
| C. | 硅单质在常温下不与任何酸、碱反应 | |
| D. | 单质硅与单质碳均具有一定的还原性 |
分析 反应2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑中,Si元素化合价降低,被还原,SiO2为氧化剂,C元素化合价升高,被氧化,C为还原剂,结合反应的化学方程式解答该题.
解答 解:A、由反应方程式可知消耗2mol的碳和1mol的二氧化硅,生成1mol的硅,即固体质量减轻2×12+60-28=56g,生成28g Si,所以每当固体质量减轻5.6g时,生成2.8g Si,故A正确;
B、SiO2为氧化剂,C元素化合价升高,被氧化,C为还原剂,物质的量之比为:1:2,故B正确;
C、硅与氢氟酸反应生成四氟化硅和氢气,与NaOH反应生成硅酸钠和氢气,故C错误;
D、硅与碳最外层是4个电子,可以失电子达稳定结构,所以单质硅与单质碳均具有一定的还原性,故D正确;
故选C.
点评 本题考查氧化还原反应,为高考高频考点,侧重于化学与工业生产的考查,有利于培养学生的良好的科学素养,提高学习的积极性,注意从元素化合价的角度解答该题,难度不大.

练习册系列答案
相关题目
18.下列除去杂质的实验方法不正确的是( )
| A. | 除去Cl2中少量HC1气体:通过饱和食盐水后再干燥气体 | |
| B. | 除去Na2CO3固体中少量NaHCO3:置于坩埚中加热 | |
| C. | 除去Fe(OH)3胶体中溶有的少量NaCl:加入适量水后过滤 | |
| D. | 除去CuCl2溶液中少量的FeCl3:加入稍过量的CuO后过滤 |
19.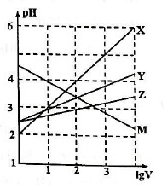 常温下取0.1mol•L-1的NaA和NaB两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O?HA+NaHCO3、2NaB+CO2+H2O?2HB+Na2CO3.则HA和HB的1L溶液分别加水稀释至体积为VL时可能有如下的曲线,则下列说法正确的是( )
常温下取0.1mol•L-1的NaA和NaB两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O?HA+NaHCO3、2NaB+CO2+H2O?2HB+Na2CO3.则HA和HB的1L溶液分别加水稀释至体积为VL时可能有如下的曲线,则下列说法正确的是( )
 常温下取0.1mol•L-1的NaA和NaB两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O?HA+NaHCO3、2NaB+CO2+H2O?2HB+Na2CO3.则HA和HB的1L溶液分别加水稀释至体积为VL时可能有如下的曲线,则下列说法正确的是( )
常温下取0.1mol•L-1的NaA和NaB两种盐溶液各1L,分别通入0.02mol CO2,发生如下反应:NaA+CO2+H2O?HA+NaHCO3、2NaB+CO2+H2O?2HB+Na2CO3.则HA和HB的1L溶液分别加水稀释至体积为VL时可能有如下的曲线,则下列说法正确的是( )| A. | X是HA,M是HB | |
| B. | 常温下PH:NaA溶液>NaB溶液 | |
| C. | 对于$\frac{c({R}^{-})}{c(HR)c(O{H}^{-})}$的值(R代表A或B),一定存在HA>HB | |
| D. | 若常温下浓度均为0.1mol•L-1的NaA和HA的混合溶液的PH>7,则c(A-)>c(HA) |
12.取80毫升的水,最合适的仪器是( )
| A. | 天平(附砝码) | B. | 10毫升的量筒 | C. | 20毫升的量筒 | D. | 100毫升的量筒 |




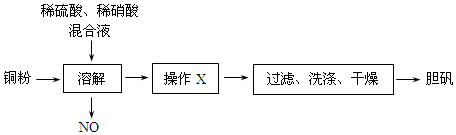
 亚硝酸钠(NaNO,)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水和过氧化钠为原料制备亚硝酸钠的装置如图所示.
亚硝酸钠(NaNO,)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水和过氧化钠为原料制备亚硝酸钠的装置如图所示.