题目内容
6.三写出与下列离子方程式相对应的化学方程式.(只需写一个化学方程式即可)(1)Cu2++2OH-=Cu(OH)2↓CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
(2)H++OH-=H2OHCl+NaOH=NaCl+H2O
(3)HCO3-+H+=CO2↑+H2ONaHCO3+HCl=CO2↑+H2O+NaCl.
分析 (1)Cu2++2OH-=Cu(OH)2↓可以表示可溶性铜盐与可溶性强碱反应生成氢氧化铜沉淀和可溶性盐;
(2)H++OH-=H2O可以表示强酸或者强酸的酸式盐与可溶性强碱反应生成可溶性盐和水;
(3)HCO3-+H+=CO2↑+H2O表示可溶性碳酸氢盐与可溶性强酸或者可溶性强酸的酸式盐反应生成二氧化碳和水和可溶性盐.
解答 解:(1)Cu2++2OH-=Cu(OH)2↓可以表示可溶性铜盐与可溶性强碱反应生成氢氧化铜沉淀和可溶性盐,例如硫酸铜与氢氧化钠反应生成氢氧化铜和硫酸钠,方程式:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
故答案为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(2)H++OH-=H2O可以表示强酸或者强酸的酸式盐与可溶性强碱反应生成可溶性盐和水,例如盐酸与氢氧化钠反应生成氯化钠和水,方程式:HCl+NaOH=NaCl+H2O;
故答案为:HCl+NaOH=NaCl+H2O;
(3)HCO3-+H+=CO2↑+H2O表示可溶性碳酸氢盐与可溶性强酸或者可溶性强酸的酸式盐反应生成二氧化碳和水和可溶性盐,例如碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,方程式:NaHCO3+HCl=CO2↑+H2O+NaCl;
故答案为:NaHCO3+HCl=CO2↑+H2O+NaCl.
点评 本题考查了离子方程式、化学方程式的书写,明确离子方程式的意义及书写方法是解题关键,注意化学式的拆分,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列说法中不正确的是( )
| A. | P2O5可用于干燥Cl2和NH3 | |
| B. | NO2溶于水时发生氧化还原反应 | |
| C. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 | |
| D. | 液氨汽化时要吸收大量的热,可用作制冷剂 |
1.在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O (g)?CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$,该反应为放热反应(填吸热或放热).若改变条件使平衡向正反应方向移动,则平衡常数③(填序号)
①一定不变 ②一定减小 ③可能增大 ④增大、减小、不变皆有可能
(2)能判断该反应是否达到化学平衡状态的依据是bc.
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O) (d)c(CO)=c(CO2)
(3)将不同量的CO (g) 和H2O (g) 分别通入到体积为2L的恒容密闭容器中,进行反应CO (g)+H2O (g)?CO2(g)+H2(g),得到如表三组数据:
①实验B中平衡时H2O (g)的物质的量是0.6mol.
②通过计算可知,CO的转化率实验A大于 实验B(填“大于”、“等于”或“小于”).
③若实验C中达到平衡所需时间 t小于3(填“大于”、“等于”或“小于”)
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(C{O}_{2})•c({H}_{2})}{c(CO)•c({H}_{2}O)}$,该反应为放热反应(填吸热或放热).若改变条件使平衡向正反应方向移动,则平衡常数③(填序号)
①一定不变 ②一定减小 ③可能增大 ④增大、减小、不变皆有可能
(2)能判断该反应是否达到化学平衡状态的依据是bc.
(a)容器中压强不变 (b)混合气体中c(CO)不变
(c)v逆(H2)=v正(H2O) (d)c(CO)=c(CO2)
(3)将不同量的CO (g) 和H2O (g) 分别通入到体积为2L的恒容密闭容器中,进行反应CO (g)+H2O (g)?CO2(g)+H2(g),得到如表三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | CO2 | CO | |||
| A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| C | 1000 | 1 | 2 | c | d | t |
②通过计算可知,CO的转化率实验A大于 实验B(填“大于”、“等于”或“小于”).
③若实验C中达到平衡所需时间 t小于3(填“大于”、“等于”或“小于”)
11.超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层.科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO(g)+2CO(g)$\stackrel{催化剂}{?}$2CO2(g)+N2(g)△H<0
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)前2s内的平均反应速率υ(N2)=1.875×10-4mol/(L•s),CO的平衡转化率为25%.(结果均保留两位有效数字)
(2)写出该反应的平衡常数K的表达式K=$\frac{{c}^{2}(C{O}_{2}).c({N}_{2})}{{c}^{2}(NO).{c}^{2}(CO)}$.
(3)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是CD.
A.选用更有效的催化剂B.升高反应体系的温度
C.降低反应体系的温度D.缩小容器的体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.某同学设计了三组实验,实验条件已经填在下面实验设计表中.
①以上三组实验的实验目的是分别验证温度、催化剂比表面积对化学反应速率的影响规律.
②请在给出的坐标图中,画出上表中的第三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图.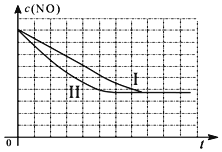
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO) (mol/L) | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO) (mol/L) | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)前2s内的平均反应速率υ(N2)=1.875×10-4mol/(L•s),CO的平衡转化率为25%.(结果均保留两位有效数字)
(2)写出该反应的平衡常数K的表达式K=$\frac{{c}^{2}(C{O}_{2}).c({N}_{2})}{{c}^{2}(NO).{c}^{2}(CO)}$.
(3)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是CD.
A.选用更有效的催化剂B.升高反应体系的温度
C.降低反应体系的温度D.缩小容器的体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.某同学设计了三组实验,实验条件已经填在下面实验设计表中.
| 实验 编号 | T(℃) | NO初始浓度 (mol/L) | CO初始浓度 (mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| Ⅱ | 280 | 1.20×10-3 | 5.80×10-3 | 124 |
| Ⅲ | 350 | 1.20×10-3 | 5.80×10-3 | 124 |
②请在给出的坐标图中,画出上表中的第三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图.

18.溶液、胶体和浊液这三种分散系的根本区别是( )
| A. | 外观 | B. | 分散质粒子的大小 | ||
| C. | 是否能通过滤纸 | D. | 是否有丁达尔效应 |
10.下列实验可实现检验或鉴别目的是( )
| A. | 根据反应MnO4-+5Fe2++8H+=Mn2-+5Fe3++4H2O可知,用酸性KMnO4溶液可检验FeSO4•7H2O是否变质 | |
| B. | 用CO2鉴别NaAlO2溶液和CH3COONa溶液 | |
| C. | 用湿润的碘化钾淀粉试剂鉴别Br2(g)和NO2 | |
| D. | 用KOH溶液鉴别SO3(g)和SO2 |
 如图中的两条线分别代表的是:1g C3H6和1g M气体在相同容积的容器中,测得容器中的压强和温度的关系,试根据图形判断M气体的相对分子质量为( )
如图中的两条线分别代表的是:1g C3H6和1g M气体在相同容积的容器中,测得容器中的压强和温度的关系,试根据图形判断M气体的相对分子质量为( )