题目内容
16.(1)某温度下,Kw=10-12.若保持温度不变,向少量水中加入400g的NaOH固体,并加水稀释至1L,才能使溶液中水电离产生的H+、OH-的浓度乘积即:c(H+)水•c(OH-)水=10-26.若保持温度不变,向水中通入的HCl气体恰好使溶液中c(H+)/c(OH-)=1010,则此时水电离的c(OH-)=10-11mol•L-1.(2)一定温度下,现有a.盐酸,b.硫酸,c.醋酸 三种酸
①当三种酸体积相同,物质的量浓度相同时,使其恰好完全中和所需NaOH的物质的量由大到小的顺序是b>a=c.(用a、b、c表示)
②当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是c>a=b.(用a、b、c表示)
③当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为a=b=c.(用a、b、c表示)
(3)现有两瓶pH=2的盐酸和醋酸溶液,简述如何用最简单的方法区别盐酸和醋酸.(限选试剂:石蕊试液、酚酞试液、pH试纸、蒸馏水).采用的方法为各取等体积醋酸和盐酸用蒸馏水稀释相同倍数(如100倍),然后用pH试纸分别测其pH值,pH值变化大的是盐酸.
(4)执信中学A学生为了测定某烧碱样品的纯度,准确称量8.2g含有少量中性易溶杂质的样品,配成500mL待测溶液.用0.200 0mol•L-1的标准盐酸进行滴定,选择甲基橙作指示剂,试根据实验回答下列问题:
①滴定过程中,眼睛应注视锥形瓶中溶液颜色变化;滴定终点时,溶液从黄色变为橙色,并且半分钟内不恢复原来的颜色.
②观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果偏高(填“偏高”、“偏低”或“无影响”);若将锥形瓶用待测液润洗,然后再加入10.00mL待测液,则滴定结果偏高(填“偏高”、“偏低”或“无影响”).
③根据如表数据,通过标准酸滴定,计算待测烧碱溶液的物质的量浓度是0.4000 mol•L-1,烧碱样品的纯度是97.56%.(本小题计算结果保留4位有效数字)
| 滴定次数 | 待测溶液 体积(mL) | 标准酸体积 | |
| 滴定前的刻度(mL) | 滴定后的 刻度(mL) | ||
| 第①次 | 10.00 | 0.40 | 20.50 |
| 第②次 | 10.00 | 4.10 | 24.00 |
| 第③次 | 10.00 | 2.20 | 23.80 |
分析 (1)水电离产生的H+、OH-的浓度乘积即:c(H+)水•c(OH-)水=10-26,则c(H+)=10-13mol/L,根据Kw=10-12计算c(OH),然后计算氢氧化钠的质量;
若保持温度不变,向水中通入的HCl气体恰好使溶液中$\frac{c({H}^{+})}{c(O{H}^{-})}$=1010,已知Kw=10-12,则c(H+)=0.1mol/L,然后计算水电离的c(OH-);
(2)HCl为一元强酸,H2SO4为二元强酸,体积、pH相同时,c(H+)相同;而CH3COOH为弱酸,其c(CH3COOH)>c(H+);物质的量浓度相同时,c(H+)关系:硫酸>盐酸>醋酸;据此分析;
(3)可根据强弱酸稀释时溶液PH的变化不同来分析;
(4)①滴定过程中眼睛需要观察锥形瓶中溶液颜色变化,以判定滴定终点;碱性时甲基橙为黄色,滴定终点时甲基橙变为橙色;
②根据c(待测)=$\frac{c(标准)×c(待测)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断误差;
③先分析所耗盐酸标准液的体积的有效性,然后求出所耗盐酸标准液的体积平均值,然后根据c(待测)=$\frac{c(标准)×c(待测)}{V(待测)}$计算,根据烧碱样品的纯度是$\frac{氢氧化钠质量}{样品质量}$×100%来计算纯度.
解答 解:(1)水电离产生的H+、OH-的浓度乘积即:c(H+)水•c(OH-)水=10-26,则c(H+)=10-13mol/L,已知Kw=10-12,c(OH)=$\frac{1{0}^{-12}}{1{0}^{-13}}$=10mol/L,则氢氧化钠的物质的量为10mol/L×1L=10mol,则质量为10mol×40g/mol=400g;
若保持温度不变,向水中通入的HCl气体恰好使溶液中$\frac{c({H}^{+})}{c(O{H}^{-})}$=1010,已知Kw=10-12,则c(H+)=0.1mol/L,则水电离的c(OH-)=$\frac{1{0}^{-12}}{0.1}$=10-11mol/L;
故答案为:400;10-11;
(2)①物质的量浓度相同、体积相同时三种酸的物质的量相同,1mol硫酸消耗2molNaOH,所以醋酸和HCl均能消耗1molNaOH,所以使其恰好完全中和所需NaOH的物质的量由大到小的顺序是:b>a=c,
故答案为:b>a=c;
②当三种酸溶液氢离子浓度相同、体积也相同时,分别加入足量锌,由于醋酸为弱电解质,醋酸的物质的量浓度增大;盐酸和硫酸为强酸,含有的氢离子浓度相等,所以相同状况下产生气体的体积关系为:c>a=b;
故答案为:c>a=b;
③当其c(H+)相同、体积相同时,与锌反应生成的氢气,开始时的速率相同,即:a=b=c;
故答案为:a=b=c;
(3)弱酸稀释时促进电离,两种酸稀释相同的倍数后溶液中的氢离子浓度不等来比较,则各取等体积醋酸和盐酸用蒸馏水稀释相同倍数(如100倍),然后用pH试纸分别测其pH值,pH值变化大的是盐酸;
故答案为:各取等体积醋酸和盐酸用蒸馏水稀释相同倍数(如100倍),然后用pH试纸分别测其pH值,pH值变化大的是盐酸;
(4)①滴定过程中眼睛需要观察锥形瓶中溶液颜色变化,以判定滴定终点;用0.2000mol•L-1的标准盐酸进行滴定NaOH溶液,锥形瓶中为NaOH溶液和甲基橙,碱性时甲基橙为黄色,滴定终点时甲基橙变为橙色,到达滴定终点时:溶液从黄色变为橙色,并且半分钟内不恢复原来的颜色;
故答案为:锥形瓶中溶液颜色变化;黄;橙;并且半分钟内不恢复原来的颜色;
②观察酸式滴定管液面时,开始俯视,滴定终点平视,则滴定结果,读数偏大,V(标准)偏大,由c(待测)=$\frac{c(标准)×c(待测)}{V(待测)}$可知,测定结果偏高;
若将锥形瓶用待测液润洗,则待测溶液中溶质的物质的量偏大,消耗的标准溶液的体积偏大,由c(待测)=$\frac{c(标准)×c(待测)}{V(待测)}$可知,测定结果偏高;
故答案为:偏高;偏高;
③所耗盐酸标准液的体积分别为:20.1mL,19.9mL、21.6mL,前两组数据均有效,盐酸标准液的平均体积为20.00mL;c(待测)=$\frac{c(标准)×c(待测)}{V(待测)}$=$\frac{0.2000mol/L×20.00mL}{10.00mL}$=0.4000 mol•L-1,烧碱样品的纯度=$\frac{0.5L×0.4000mol/L×40g/mol}{8.2g}$×100%=97.56%,
故答案为:0.4000 mol•L-1;97.56%.
点评 本题考查了混合溶液酸碱性定性判断、pH的计算、中和滴定操作方法及误差分析,题目难度中等,注意把握pH的有关计算、中和滴定的操作和误差分析方法,试题培养了学生的分析能力及化学实验能力.

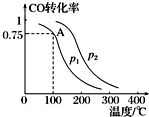 利用CO和H2可以合成甲醇,反应原理为CO(g)+2H2(g)═CH3OH(g).一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如图所示.
利用CO和H2可以合成甲醇,反应原理为CO(g)+2H2(g)═CH3OH(g).一定条件下,在容积为V L的密闭容器中充入a mol CO与2a mol H2合成甲醇,平衡转化率与温度、压强的关系如图所示.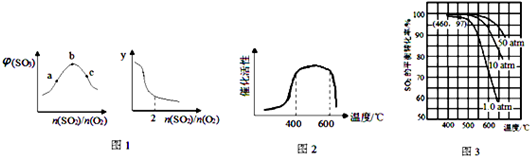
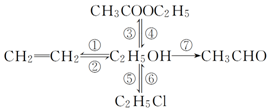 写出下列各物质相互转化的化学方程式,并说明各步的反应类型.
写出下列各物质相互转化的化学方程式,并说明各步的反应类型.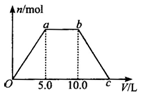 向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体体积(V)的关系如图所示,试回答:
向Ba(OH)2和NaOH的混合稀溶液中通入足量的CO2气体,生成沉淀的物质的量(n)和通入CO2气体体积(V)的关系如图所示,试回答: