题目内容
20.在一定温度下(已知在该温度下,容器内所有物质均为气态),10L密闭容器中加入5molSO2、4molO2,经10min后反应达平衡时有2molSO2发生了反应.试计算:(要求写出规范解题步骤)(1)用O2表示该反应的反应速率;
(2)SO2的转化率;
(3)该温度下的平衡常数K(保留三位有效数字).
分析 依据化学平衡三段式列式;
2SO2+O2=2SO3
起始量(mol) 5 4 0
变化量(mol) 2 1 2
平衡量(mol) 3 3 2
根据反应速率、转化率、平衡常数的概念分别计算得到.
解答 解:依据化学平衡三段式列式;
2SO2+O2=2SO3
起始量(mol) 5 4 0
变化量(mol) 2 1 2
平衡量(mol) 3 3 2
(1)用O2表示该反应的反应速率,V(O2)=$\frac{\frac{1mol}{10L}}{10min}$=0.010 mol/(L•min),
答:用O2表示该反应的反应速率为0.020 mol/(L•min);
(2)SO2的转化率=$\frac{2mol}{5mol}$×100%=40%,答:SO2的转化率为40%;
(3)该温度下的平衡常数K=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{2})c({O}_{2})}=\frac{(\frac{2mol}{10L})^{2}}{(\frac{3mol}{10L})^{2}(\frac{3mol}{10L})}$=1.48,
答:该温度下的平衡常数K为1.48.
点评 本题考查化学平衡的三段式计算方法,反应速率、转化率、平衡常数计算应用,题目难度中等.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
12.下列有机物能与NaOH反应的是( )
| A. | 乙烷 | B. | 乙醇 | C. | 乙酸 | D. | 苯 |
10.下列反应既属于氧化还原反应又符合图示能量变化的是( )


| A. | 灼热的炭与CO2的反应 | B. | 铝片与稀盐酸的反应 | ||
| C. | Ba(OH)2•8H2O和NH4Cl的反应 | D. | 甲烷在氧气中的燃烧反应 |
 对于反应2A(g)+B(g)?2C(g)在反应过程中C的质量分WC随温度变化如图所示,试确定:
对于反应2A(g)+B(g)?2C(g)在反应过程中C的质量分WC随温度变化如图所示,试确定: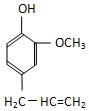 某有机化合物A因其具有麻醉作用,常用作局部麻醉剂和镇痛剂.它的结构简式如图所示,请回答:
某有机化合物A因其具有麻醉作用,常用作局部麻醉剂和镇痛剂.它的结构简式如图所示,请回答: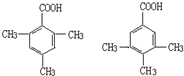 中的一种.
中的一种.