题目内容
高纯晶体硅是信息技术的关键材料.
(1)硅元素位于周期表的 周期 族,在周期表的以下区域中,可以找到类似硅的半导体材料的是 (填字母序号).
a.过渡元素区域
b.金属和非金属元素的分界线附近
c.含有氟、氯、硫、磷等元素的区域
(2)工业上用石英砂和焦炭可制得粗硅.
已知:(如图1)
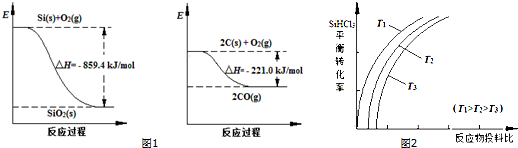
请将以下反应的热化学方程式补充完整:
SiO2(s)+2C(s)═Si(s)+2CO(g)△H=
(3)粗硅经系列反应可生成硅烷(SiH4),硅烷分解生成高纯硅.已知硅烷的分解温度远低于甲烷,用原子结构解释其原因: ,Si元素的非金属性弱于C元素,硅烷的热稳定性弱于甲烷.
(4)将粗硅转化成三氯氢硅(SiHCl3),进一步反应也可制得高纯硅.
①SiHCl3中含有的SiCl4、AsCl3等杂质对晶体硅的质量有影响.根据下表数据,可用 方法提纯SiHCl3.
②用SiHCl3制备高纯硅的反应为 SiHCl3 (g)+H2(g)
Si(s)+3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时,各反应物的物质的量之比)的变化关系如图2所示.下列说法正确的是 (填字母序号).
a.该反应的平衡常数随温度升高而增大
b.横坐标表示的投料比应该是
c.实际生产中为提高SiHCl3的利用率,应适当升高温度.
(1)硅元素位于周期表的
a.过渡元素区域
b.金属和非金属元素的分界线附近
c.含有氟、氯、硫、磷等元素的区域
(2)工业上用石英砂和焦炭可制得粗硅.
已知:(如图1)

请将以下反应的热化学方程式补充完整:
SiO2(s)+2C(s)═Si(s)+2CO(g)△H=
(3)粗硅经系列反应可生成硅烷(SiH4),硅烷分解生成高纯硅.已知硅烷的分解温度远低于甲烷,用原子结构解释其原因:
(4)将粗硅转化成三氯氢硅(SiHCl3),进一步反应也可制得高纯硅.
①SiHCl3中含有的SiCl4、AsCl3等杂质对晶体硅的质量有影响.根据下表数据,可用
| 物质 | SiHCl3 | SiCl4 | AsCl3 |
| 沸点/℃ | 32.0 | 57.5 | 131.6 |
| 一定条件 |
a.该反应的平衡常数随温度升高而增大
b.横坐标表示的投料比应该是
| n(SiHCl3) |
| n(H2) |
c.实际生产中为提高SiHCl3的利用率,应适当升高温度.
考点:元素周期表的结构及其应用,热化学方程式,化学平衡的影响因素,硅和二氧化硅
专题:
分析:(1)依据硅是14号元素分析其位置,依据元素周期表的递变规律寻找半导体材料;
(2)由图1可得热化学方程式:
①Si(s)+O2(g)═SiO2(s)△H1=-859.4kJ?mol-1
②O2(g)+2C(s)═2CO(g)△H2=-221.0kJ?mol-1
根据盖斯定律可知,热化学方程式SiO2(s)+2C(s)═Si(s)+2CO(g)可由②-①得,△H=△H2-△H1=-859.4-(-221.0)kJ?mol-1=+638.4 kJ?mol-1;
(3)硅烷的分解温度远低于甲烷的原因为:C和Si最外层电子数相同(或“是同主族元素”),C原子半径小于Si(或“C原子电子层数少于Si”) Si元素的非金属性弱于C元素,硅烷的热稳定性弱于甲烷;
(4)①根据各物质沸点的不同分离提纯物质,可用蒸馏(或分馏)法;
②a.因为随着温度的升高,SiHCl3的转化率增大,平衡右移,则该反应的平衡常数随温度升高而增大;
b.增大一种反应物的浓度,能提高其它反应物的转化率,而本身的转化率反而降低,故横坐标表示的投料比应该是
;
c.因为随着温度的升高,SiHCl3的转化率增大,平衡右移,故实际生产中为提高SiHCl3的利用率,应适当升高温度.
(2)由图1可得热化学方程式:
①Si(s)+O2(g)═SiO2(s)△H1=-859.4kJ?mol-1
②O2(g)+2C(s)═2CO(g)△H2=-221.0kJ?mol-1
根据盖斯定律可知,热化学方程式SiO2(s)+2C(s)═Si(s)+2CO(g)可由②-①得,△H=△H2-△H1=-859.4-(-221.0)kJ?mol-1=+638.4 kJ?mol-1;
(3)硅烷的分解温度远低于甲烷的原因为:C和Si最外层电子数相同(或“是同主族元素”),C原子半径小于Si(或“C原子电子层数少于Si”) Si元素的非金属性弱于C元素,硅烷的热稳定性弱于甲烷;
(4)①根据各物质沸点的不同分离提纯物质,可用蒸馏(或分馏)法;
②a.因为随着温度的升高,SiHCl3的转化率增大,平衡右移,则该反应的平衡常数随温度升高而增大;
b.增大一种反应物的浓度,能提高其它反应物的转化率,而本身的转化率反而降低,故横坐标表示的投料比应该是
| n(H2) |
| n(SiHCl3) |
c.因为随着温度的升高,SiHCl3的转化率增大,平衡右移,故实际生产中为提高SiHCl3的利用率,应适当升高温度.
解答:
解:(1)Si是14号元素,处于周期表中第三周期第ⅣA 族,元素周期表中,在金属与非金属的分界线附近的元素既有金属的性质有非金属的性质,能作半导体材料,故b正确;
故答案为:三;ⅣA; b;
(2)由图1可得热化学方程式:
①Si(s)+O2(g)═SiO2(s)△H1=-859.4kJ?mol-1
②O2(g)+2C(s)═2CO(g)△H2=-221.0kJ?mol-1
根据盖斯定律可知,热化学方程式SiO2(s)+2C(s)═Si(s)+2CO(g)可由②-①得,△H=△H2-△H1=-859.4-(-221.0)kJ?mol-1=+638.4 kJ?mol-1,
故答案为:+638.4 kJ?mol-1;
(3)C和Si最外层电子数相同(或“是同主族元素”),C原子半径小于Si(或“C原子电子层数少于Si”) Si元素的非金属性弱于C元素,硅烷的热稳定性弱于甲烷,故硅烷的分解温度远低于甲烷,
故答案为:C和Si最外层电子数相同(或“是同主族元素”),C原子半径小于Si(或“C原子电子层数少于Si”) Si元素的非金属性弱于C元素,硅烷的热稳定性弱于甲烷;
(4)①根据各物质沸点的不同分离提纯物质,可用蒸馏(或分馏)法,故答案为:蒸馏(或分馏);
②a.因为随着温度的升高,SiHCl3的转化率增大,平衡右移,则该反应的平衡常数随温度升高而增大,故a正确;
b.增大一种反应物的浓度,能提高其它反应物的转化率,而本身的转化率反而降低,故横坐标表示的投料比应该是
,故b错误;
c.因为随着温度的升高,SiHCl3的转化率增大,平衡右移,故实际生产中为提高SiHCl3的利用率,应适当升高温度,故c正确;
故选ac.
故答案为:三;ⅣA; b;
(2)由图1可得热化学方程式:
①Si(s)+O2(g)═SiO2(s)△H1=-859.4kJ?mol-1
②O2(g)+2C(s)═2CO(g)△H2=-221.0kJ?mol-1
根据盖斯定律可知,热化学方程式SiO2(s)+2C(s)═Si(s)+2CO(g)可由②-①得,△H=△H2-△H1=-859.4-(-221.0)kJ?mol-1=+638.4 kJ?mol-1,
故答案为:+638.4 kJ?mol-1;
(3)C和Si最外层电子数相同(或“是同主族元素”),C原子半径小于Si(或“C原子电子层数少于Si”) Si元素的非金属性弱于C元素,硅烷的热稳定性弱于甲烷,故硅烷的分解温度远低于甲烷,
故答案为:C和Si最外层电子数相同(或“是同主族元素”),C原子半径小于Si(或“C原子电子层数少于Si”) Si元素的非金属性弱于C元素,硅烷的热稳定性弱于甲烷;
(4)①根据各物质沸点的不同分离提纯物质,可用蒸馏(或分馏)法,故答案为:蒸馏(或分馏);
②a.因为随着温度的升高,SiHCl3的转化率增大,平衡右移,则该反应的平衡常数随温度升高而增大,故a正确;
b.增大一种反应物的浓度,能提高其它反应物的转化率,而本身的转化率反而降低,故横坐标表示的投料比应该是
| n(H2) |
| n(SiHCl3) |
c.因为随着温度的升高,SiHCl3的转化率增大,平衡右移,故实际生产中为提高SiHCl3的利用率,应适当升高温度,故c正确;
故选ac.
点评:本题主要考查的是元素周期表的应用、盖斯定律应用、化学平衡常数和平衡移动等,题目难度中等,注意相关知识的积累.

练习册系列答案
相关题目
垃圾分类从你我他开始.废弃塑料瓶属于( )
A、 |
B、 |
C、 |
D、 |
pH相同、体积相同的氨水和氢氧化钠溶液分别采取下列措施,有关叙述正确的是…( )
| A、加入适量的氯化铵晶体后,两溶液的pH均碱小 |
| B、温度下降10°C,两溶液的pH均不变 |
| C、分别加水稀释10倍,两溶液的pH仍相等 |
| D、用同浓度的盐酸中和,消耗盐酸的体积相同 |
下列说法正确的是( )
| A、同一主族的金属元素,从上到下阳离子的氧化性逐渐增强 |
| B、最外层电子数相同的微粒,其化学性质一定相似 |
| C、同周期金属元素的氧化物对应水化物的碱性从左到右依次增强 |
| D、第ⅦA族元素从上到下,其氢化物稳定性减弱而还原性增强 |
下列判断正确的是( )
| A、标准状况下,2.24LCH3OH含有的分子数等于0.1NA |
| B、相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 |
| C、0.1 mol?L-1的碳酸钠溶液的pH大于0.1 mol?L-1的醋酸钠溶液的pH |
| D、3.4g NH3中含N-H键数目为0.2NA |
下列反应离子方程式正确的是( )
| A、大理石溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、氯气通入冷的氢氧化钠溶液中:2Cl2+2OH-=3Cl-+ClO-+H2O |
| C、向澄清石灰水中加入少量小苏打溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| D、氨水中通入过量二氧化硫:2NH3?H2O+SO2=2NH4++SO32-+2H2O |