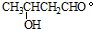题目内容
下列说法正确的是( )
| A、同一主族的金属元素,从上到下阳离子的氧化性逐渐增强 |
| B、最外层电子数相同的微粒,其化学性质一定相似 |
| C、同周期金属元素的氧化物对应水化物的碱性从左到右依次增强 |
| D、第ⅦA族元素从上到下,其氢化物稳定性减弱而还原性增强 |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.同一主族的金属元素,从上到下金属性逐渐增强,故对应阳离子的氧化性逐渐减弱;
B.根据微粒的种类进行分析;
C.同周期主族元素的金属性越强,对应最高价氧化物的水化物的碱性越强;
D.同主族元素,从上往下,元素的非金属性逐渐减弱,其氢化物的稳定性逐渐减弱.
B.根据微粒的种类进行分析;
C.同周期主族元素的金属性越强,对应最高价氧化物的水化物的碱性越强;
D.同主族元素,从上往下,元素的非金属性逐渐减弱,其氢化物的稳定性逐渐减弱.
解答:
解:A.同一主族的金属元素,从上到下金属性逐渐增强,故对应阳离子的氧化性逐渐减弱,故A错误;
B.氦原子与镁原子的最外层电子数相同,但化学性质不相似,故B错误;
C.同周期主族元素的金属性越强,对应最高价氧化物的水化物的碱性越强,故同周期金属元素的最高价氧化物对应水化物的碱性从左到右依次减弱,故C错误;
D.同主族元素,从上往下,元素的非金属性逐渐减弱,其氢化物的稳定性逐渐减弱,还原性增强,故D正确;
故选D.
B.氦原子与镁原子的最外层电子数相同,但化学性质不相似,故B错误;
C.同周期主族元素的金属性越强,对应最高价氧化物的水化物的碱性越强,故同周期金属元素的最高价氧化物对应水化物的碱性从左到右依次减弱,故C错误;
D.同主族元素,从上往下,元素的非金属性逐渐减弱,其氢化物的稳定性逐渐减弱,还原性增强,故D正确;
故选D.
点评:本题考查元素的性质及元素周期律的应用,为高频考点,难度不大.把握元素的位置及性质变化规律为解答的关键.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
化学与能源开发、环境保护、资源利用等密切相关,下列说法正确的是( )
| A、为提高农作物的产量和质量,应大量使用化肥和农药 |
| B、装饰装修材料中的甲醛、芳香烃及放射性物质都会造成室内污染 |
| C、氯气本身有毒,可以直接杀死水中的细菌和病毒,所以液氯可用于自来水的消毒剂 |
| D、棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O |
反应过程中固体物质质量增加的是 ( )
| A、氨气通过无水氯化钙粉末 |
| B、氢气通过灼热的氧化铜粉末 |
| C、铝与氧化铁发生铝热反应 |
| D、将锌粒投入到硝酸铜溶液中 |
Na2O2、CaC2都是离子化合物,都能与水反应放出气体.它们 ( )
| A、阴阳离子个数比均为1:1 |
| B、都含有非极性的共价键 |
| C、与水都发生氧化还原反应 |
| D、放出的都是可燃性气体 |
下列各组物质的性质比较中不正确的是( )
| A、热稳定性:H2S>PH3>SiH4 |
| B、原子半径:Na>Mg |
| C、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D、结合质子能力:Cl->S2- |
下列哪一个反应表示二氧化硫被还原( )
| A、SO2+2H2O+Cl2=H2SO4+2HCl |
| B、SO2+2NaOH=Na2SO3+H2O |
| C、SO2+2H2S=2H2O+3S↓ |
| D、SO2+PbO2=PbSO4 |

 .2CH3CHO
.2CH3CHO