题目内容
1.为探究Na、Mg、Al的金属活动性顺序,某课外小组同学进行了如下实验:| 实验 | ①将一小块金属钠放入滴有酚酞溶液的冷水中 ②将一小段用砂纸打磨后的镁带放入试管中,加入少量水,加热至水沸腾,冷却后,向试管中滴加酚酞溶液. ③将一小段镁带投入稀盐酸中 ④将一小片铝投入稀盐酸中 |
| 实验 现象 | ①剧烈反应,迅速生成大量的气体. ②浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红. ③反应不剧烈,产生无色气体. ④有气体产生,溶液变成红色. |
(1)在下表中填写与实验相对应的实验现象序号:
| 实验 | 1 | 2 | 3 | 4 |
| 实验现象 |
(3)实验结论是金属活动性顺序为Na>Mg>Al.
(4)用原子结构理论对上述实验结论进行解释:同周期元素从左至右,原子的电子层数相同,核电荷数逐渐增多,原子半径逐渐减小,原子核对电子的引力逐渐增强,失电子能力逐渐减弱,因此金属性逐渐减弱.
分析 (1)越是活泼的金属,和酸或者水反应越剧烈,置换出氢气越容易,生成碱的碱性越强;
(2)Na与水反应生成氢氧化钠和氢气;
(3)根据以上反应现象判断金属钠、镁、铝的活动性顺序;
(4)从原子半径和失电子能力角度来解释金属性强弱关系.
解答 解:(1)金属钠、镁、铝位于同一周期,按照从左到右的顺序失电子能力逐渐减小,和水及酸反应置换出氢气的程度是越来越难,所以:1对应的现象为②、2对应的现象为④、3对应的现象为①、4对应的现象为③,
故答案为:
| 实验步骤 | 1 | 2 | 3 | 4 |
| 实验现象 | ② | ④ | ① | ③ |
故答案为:2Na+2H2O=2NaOH+H2↑;
(3)根据金属和酸以及水的反应的剧烈程度,可以知道:金属活动性顺序为:Na>Mg>Al,
故答案为:金属活动性顺序为Na>Mg>Al;
(4)同周期元素从左到右核电荷数逐渐增多,原子半径逐渐减小,原子核对核外电子的吸引力逐渐增强,失电子能力逐渐减弱,金属性逐渐减弱,
故答案为:减小;减弱;金属性.
点评 本题考查学生同一周期元素性质的递变规律知识,题目难度不大,试题结合试验的方式考查,增加了题目的处理难度,注意熟练掌握元素周期律的内容及其应用.

练习册系列答案
相关题目
11.下列化学用语正确的是( )
| A. | 氯化钠的电子式: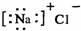 | B. | 磷原子的结构示意图: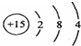 | ||
| C. | 乙烯的结构简式CH2CH2 | D. | 乙酸的分子式C2H4O2 |
12.某化学兴趣小组的同学设计了一套实验方案探究元素周期表中元素性质的变化规律:
1.同一周期内从左到右元素金属性的递变规律.
2.同一主族内从上到下元素非金属性的递变规律.
回答下列问题
(1)从上表(Ⅰ)中选择实验方法,从(Ⅱ)中选择相应的实验现象,上下对应地填写符合要求的答案在空格中(上下必须对应才得分,有几个填几个,不一定把空格填满).
(2)实验结论(用元素符号表示具体的强弱顺序):
元素的金属性:Na>Mg>Al,元素的非金属性:Cl>Br>I
(3)上表(Ⅰ)中实验方法1反应的离子方程式2Na+2H2O=2Na++2OH-+H2↑.
(4)上表(Ⅰ)中实验方法8反应的离子方程式2Al+6H+=2Al3++3H2↑.
(5)上表(Ⅱ)中实验现象F反应的化学方程式Br2+2NaI=2NaBr+I2.
1.同一周期内从左到右元素金属性的递变规律.
2.同一主族内从上到下元素非金属性的递变规律.
| 实验方法(Ⅰ) | 实验现象(Ⅱ) |
| 1.钠与冷水反应,再向反应后溶液中滴 加酚酞. | A.产生白烟 |
| 2.向新制的H2S饱和溶液中滴加新制的氯水 | B.反应不十分剧烈,产生的气体能燃烧,溶液变成浅红色.与酸反应剧烈,产生大量气泡且可以燃烧 |
| 3.镁带用砂纸打磨后在空气中燃烧 | C.产生大量气泡、气体可以燃烧 |
| 4.NaI溶液中加入溴水和CCl4 | D.下层溶液变橙色 |
| 5.镁带用砂纸打磨后与沸水反应,再向反应后溶液中滴加酚酞.镁带用砂纸打磨后与2mol/L盐酸反应. | E.浮于水面,熔成小球,迅速向四处游动,溶液变成红色 |
| 6.蘸浓氨水与浓盐酸的两玻璃棒接近 | F.下层溶液变紫色 |
| 7.NaBr溶液中加入氯水和CCl4 | G.发出耀眼的强光,生成白色物质 |
| 8.铝片用砂纸打磨后与2mol/L盐酸反应 | H.生成淡黄色沉淀 |
(1)从上表(Ⅰ)中选择实验方法,从(Ⅱ)中选择相应的实验现象,上下对应地填写符合要求的答案在空格中(上下必须对应才得分,有几个填几个,不一定把空格填满).
| 探究同一周期从左到右元素 金属性的递变规律 | 探究同一主族内从上到下元素 非金属性的递变规律 | |||||||
| Ⅰ | ||||||||
| Ⅱ | ||||||||
元素的金属性:Na>Mg>Al,元素的非金属性:Cl>Br>I
(3)上表(Ⅰ)中实验方法1反应的离子方程式2Na+2H2O=2Na++2OH-+H2↑.
(4)上表(Ⅰ)中实验方法8反应的离子方程式2Al+6H+=2Al3++3H2↑.
(5)上表(Ⅱ)中实验现象F反应的化学方程式Br2+2NaI=2NaBr+I2.
9.在一定条件下,NO跟NH3可发生反应生成N2和H2O.现有一定量的NO和NH3的混合气体恰好完全反应,所得产物中还原产物比氧化产物多2.8g,则原混合气体中NO和NH3总的物质的量为( )
| A. | 0.25mol | B. | 0.5mol | C. | 1mol | D. | 2mol |
16.已知短周期元素的离子aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述中正确的是( )
| A. | 原子序数d>c>b>a | B. | 离子半径C2->D->B+>A2+ | ||
| C. | 原子半径A>B>C>D | D. | 非金属性:C>D |
13.一定条件下,体积为1L的密闭容器中发生如下反应:SiF4(g)+2H2O(g)?SiO2(s)+4HF(g);△H=+148.9kJ•mol-1
(1)下列各项中能说明该反应已达化学平衡状态的是bcd(填字母序号).
a.v消耗(SiF4)=4v生成(HF)
b.容器内气体压强不再变化
c.容器内气体的总质量不再变化
d.HF的体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中t2>t1)所示.
通过计算可得:a=1.6b=0.8.
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应acd(填序号).
a.一定向正反应方向移动
b.一定向逆反应方向移动
c.一定是升高温度造成的
d.SiF4的平衡转化率一定增大.
(1)下列各项中能说明该反应已达化学平衡状态的是bcd(填字母序号).
a.v消耗(SiF4)=4v生成(HF)
b.容器内气体压强不再变化
c.容器内气体的总质量不再变化
d.HF的体积分数不再变化
(2)反应过程中测定的部分数据如下表(表中t2>t1)所示.
| 反应时间/min | n(SiF4)/mol | n(H2O)/mol |
| 0 | 1.20 | 2.40 |
| t1 | 0.80 | a |
| t2 | b | 1.60 |
(3)若只改变一个条件使上述反应的化学平衡常数变大,该反应acd(填序号).
a.一定向正反应方向移动
b.一定向逆反应方向移动
c.一定是升高温度造成的
d.SiF4的平衡转化率一定增大.
10.将8g NaOH溶解在10mL水中,再稀释成1L溶液,从中取出10mL,这10mL溶液的物质的量浓度为( )
| A. | 2 mol•L-1 | B. | 0.2 mol•L-1 | C. | 0.02mol•L-1 | D. | 20 mol•L-1 |
11.如表是元素周期表的一部分,针对表中①~⑩种元素,填写下列空白:
(1)被选作相对原子质量标准的核素是12C(填核素符号).
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH.
(3)最高价氧化物是两性氧化物的元素在第ⅢA族;写出它的氧化物与氢氧化钠溶液反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
(4)从⑤到⑧的元素中,Na原子半径最大(填元素符号).
(5)元素④与⑥形成的化合物属于离子(填“共价”或“离子”)化合物.
(6)若要比较⑤比⑥的金属性强弱,下列实验方法可行的是C.
A、将单质⑤置于⑥的盐溶液中,如果⑤不能置换出单质⑥,说明⑤的金属性弱
B、比较⑤和⑥的最高价氧化物对应水化物的水溶性,前者比后者溶解度大,故前者金属性强
C、将⑤、⑥的单质分别投入到水中,观察到⑤与水反应更剧烈,说明⑤的金属性强
D、将⑤、⑥的单质分别在O 2中燃烧,前者得到氧化物的颜色比后者得到氧化物的颜色深,则前者金属性强.
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH.
(3)最高价氧化物是两性氧化物的元素在第ⅢA族;写出它的氧化物与氢氧化钠溶液反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
(4)从⑤到⑧的元素中,Na原子半径最大(填元素符号).
(5)元素④与⑥形成的化合物属于离子(填“共价”或“离子”)化合物.
(6)若要比较⑤比⑥的金属性强弱,下列实验方法可行的是C.
A、将单质⑤置于⑥的盐溶液中,如果⑤不能置换出单质⑥,说明⑤的金属性弱
B、比较⑤和⑥的最高价氧化物对应水化物的水溶性,前者比后者溶解度大,故前者金属性强
C、将⑤、⑥的单质分别投入到水中,观察到⑤与水反应更剧烈,说明⑤的金属性强
D、将⑤、⑥的单质分别在O 2中燃烧,前者得到氧化物的颜色比后者得到氧化物的颜色深,则前者金属性强.
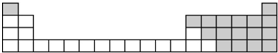
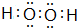 ,所含的化学键类型为共价键.
,所含的化学键类型为共价键.