题目内容
19.向含有a mol NaOH和a mol Ba(OH)2的混合液中通入b mol CO2气体,充分反应后(忽略水解对离子浓度变化的影响),下列说法不正确的是( )| A. | 当a=b时,发生的离子总反应为:2OH-+CO2+Ba2+═BaCO3↓+H2O | |
| B. | 当3a=2b时,发生的离子总反应为:6OH-+3CO2+2Ba2+═2BaCO3↓+3H2O+CO32- | |
| C. | 当$\frac{3}{2}$a<b<3a时,溶液中含有n(CO32-):n(HCO3-)=(3a-b):(2b-3a) | |
| D. | 当3a=b时,溶液中Na+、Ba2+与HCO3-的物质的量之比为1:1:3 |
分析 向含有a mol NaOH和a mol Ba(OH)2的混合液中通入b mol CO2气体,氢氧化钡优先反应:2OH-+CO2+Ba2+═BaCO3↓+H2O,amolBa(OH)2完全反应生成碳酸钡消耗amol二氧化碳;之后NaOH发生反应:2OH-+CO2═H2O+CO32-,amolNaOH转化成碳酸钠消耗0.5molCO2,此时总共消耗1.5amolCO2;氢氧化钠反应完全后,通入的二氧化碳发生反应:CO2+CO32-+H2O=2HCO3-,若再通入二氧化碳,BaCO3沉淀开始溶解,据此进行解答.
解答 解:A.当a=b时,只有氢氧化钡参与反应,反应的离子方程式为:2OH-+CO2+Ba2+═BaCO3↓+H2O,故A正确;
B.当3a=2b时,即b=1.5a,氢氧化钠和氢氧化钡恰好完全反应生成碳酸钠、碳酸钡沉淀,发生的离子总反应为:6OH-+3CO2+2Ba2+═2BaCO3↓+3H2O+CO32-,故B正确;
C.当$\frac{3}{2}$a<b<3a时,b=2a时发生反应:5OH-+4CO2+2Ba2+═2BaCO3↓+2H2O+HCO3-,则b≥2a时溶液中几乎不存在碳酸根离子,故C错误;
D.当3a=b时,氢氧化钠、氢氧化钡完全反应生成碳酸氢钠、碳酸氢钠,根据质量守恒定律可知溶液中Na+、Ba2+与HCO3-的物质的量之比为1:1:3,故D正确;
故选C.
点评 本题考查了离子方程式的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握发生反应的先后顺序,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
14.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 4.0 g重水(D2O)中所含质子数为2NA | |
| B. | 4.48 L N2与CO的混合物中所含分子数为0.2NA | |
| C. | 常温常压下16g的氧气与臭氧混合气体中,氧原子数为NA | |
| D. | 12.5 mL 16 mol•L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
4.大庆市某中学化学实验小组在实验室鉴定某无色溶液.已知溶液中的溶质仅由NH4+、K+、Ag+、Ca2+、Al3+、AlO2-、MnO4-、CO32-、SO42-中的若干种组成.取该溶液进行如下实验:
(1)取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液
(2)在(1)所得溶液中加入过量NH4HCO3溶液,有气体生成,同时产生白色沉淀甲;
(3)在(2)所得溶液中加入过量Ba(OH)2溶液并加热也有气体生成,同时产生白色沉淀乙
则下列离子在原溶液中一定存在的有( )
(1)取适量溶液,加入过量盐酸,有气体生成,并得到无色溶液
(2)在(1)所得溶液中加入过量NH4HCO3溶液,有气体生成,同时产生白色沉淀甲;
(3)在(2)所得溶液中加入过量Ba(OH)2溶液并加热也有气体生成,同时产生白色沉淀乙
则下列离子在原溶液中一定存在的有( )
| A. | K+、CO32、AlO2- | B. | SO42-、AlO2-、K+、CO32-、 | ||
| C. | CO32-、K+、Al3+ | D. | MnO4-、K+、CO32-、NH4+ |
11.现有X、Y、Z、W四种短周期元素,X、Y位于同主族,Z、W位于同主族且Z的核电荷数是W的2倍,Y、Z位于同周期,X与Z、W都不在同一周期.下列说法不正确的是( )
| A. | 简单离子半径:Z>W>Y | |
| B. | 气态氢化物的稳定性:Z<W | |
| C. | Z的氢化物能与其最高价氧化物对应的水化物反应 | |
| D. | 在X2和W2构成的燃料电池中,W2作负极 |
8.用NA表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A. | 标准状况下,22.4L氯气与足量铁粉充分反应,转移的电子数为2NA | |
| B. | 28g乙烯和环丁烷的混合气体中含有的碳原子数为3NA | |
| C. | 0.5molNa2O2中含有NA个阴离子 | |
| D. | 1L0.1mol/LAl2(SO4)3溶液中含有的阳离子总数为0.2NA |
7.下列说法正确的是( )
| A. | SO2具有漂白性,所以它能使品红溶液、溴水、KMnO4(H+)、石蕊试液褪色 | |
| B. | 能使品红溶液褪色的不一定是SO2 | |
| C. | SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同 | |
| D. | 等物质的量的SO2和Cl2相遇在溶液中具有漂白能力 |
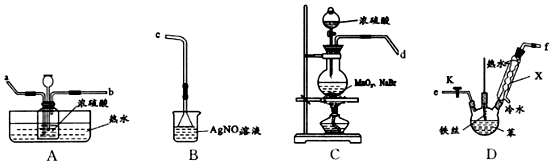
 ;仪器X的名称为球形冷凝管.
;仪器X的名称为球形冷凝管. ?
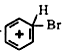
?
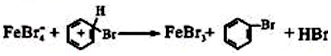 ;
;