题目内容
9.硫、氯的单质和化合物应用广泛.(1)将硫铁矿和焦炭按物质的量比3:2混合放在炼硫炉中,通入适量空气中,发生下列燃烧反应:
FeS2+C+O2-→Fe3O4+CO+S.
请配平上述化学反应方程式:3FeS2+2C+3O2═Fe3O4+2CO+6S.生成3mol硫,被氧化物质的物质的量为2.5mol.
(2)盐酸是应用广泛的酸之一,它具有:a.酸性;b.氧化性;c.还原性;d.挥发性.请回答下列问题:
①浓盐酸长时间露置在空气中,溶液的质量减轻,盐酸表现了d(填序号).
②实验室用稀盐酸和锌粒反应制取氢气,盐酸表现了ab(填序号),反应的离子方程式为Zn+2H+═Zn2++H2↑.
③用盐酸除去铁表面的铁锈,盐酸表现了a(填序号),反应的离子方程式为Fe2O3+6H+═2Fe3++3H2O.
分析 (1)FeS2+C+O2→Fe3O4+CO+S中,Fe、C、S元素的化合价升高,O元素的化合价降低,结合电子、原子守恒分析;
(2)①浓盐酸易挥发;
②用稀盐酸和锌粒反应制取氢气,H元素的化合价由+1价降低为0,且生成盐;
③用盐酸除去铁表面的铁锈,反应生成氯化铁和水,氯化铁为盐.
解答 解:(1)FeS2+C+O2→Fe3O4+CO+S中,Fe、C、S元素的化合价升高,O元素的化合价降低,FeS2、C均为还原剂被氧化,结合电子、原子守恒可知反应为3FeS2+2C+3O2═Fe3O4+2CO+6S,由 反应可知,生成6molS时,5mol还原剂被氧化,则生成3mol硫,被氧化的物质的物质的量为2.5 mol,
故答案为:3FeS2+2C+3O2═Fe3O4+2CO+6S;2.5mol;
(2)①浓盐酸易挥发,则浓盐酸长时间露置在空气中,溶液的质量减轻,故答案为:d;
②用稀盐酸和锌粒反应制取氢气,H元素的化合价由+1价降低为0,且生成盐,则盐酸表现氧化性和酸性,离子反应为Zn+2H+═Zn2++H2↑,
故答案为:ab;Zn+2H+═Zn2++H2↑;
③用盐酸除去铁表面的铁锈,反应生成氯化铁和水,氯化铁为盐,则盐酸表现酸性,离子反应为,故答案为:a;Fe2O3+6H+═2Fe3++3H2O.
点评 本题考查物质的性质及氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
14.含氯消毒液(主要成分NaClO)与含氯洁厕灵(主要成分HCl)混用可能会造成中毒,其原因是:NaClO+2HCl=Cl2↑+NaCl+H2O,下列说法中正确的是( )
| A. | NaCl的电子式为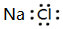 | |
| B. | NaClO只含有离子键 | |
| C. | 当释放2.24L Cl2时,一定有6.02×1022个氯分子扩散到室内 | |
| D. | 使用消毒液时滴加食醋可加快作用发挥,其原因用离子方程式表示为:ClO-+CH3COOH=HClO+CH3COO- |
20.两份铝屑,第一份与足量盐酸反应,第二份与足量氢氧化钠溶液反应,产生的氢气的体积比为1:1,则消耗的盐酸和氢氧化钠的物质的量比为( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 3:1 |
1. 50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图所示装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:
50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图所示装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:
(1)如果将环形玻璃搅拌棒改为环形金属(如铜)棒,对求得中和热数值的影响是偏低(填“偏高”、“偏低”或“无影响”).
(2)如果改用60mL 1.0mol•L-1盐酸跟50mL 1.1mol•L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量增加(填“增加”、“减少”或“不变”),所求中和热数值不变(填“增加”、“减少”或“不变”);
(3)不能用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,理由是H2SO4与Ba(OH)2反应生成的BaSO4沉淀时也有能量变化(或放热);
(4)该实验小组做了三次实验,每次取溶液各50mL,并记录如表原始数据.
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混合液的比热容C=4.184×10-3 kJ/(g•℃),则该反应的中和热为△H=-56.06kJ/mol(保留小数点后一位).
(5)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是acd(填字母).
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定HCl溶液的温度.
 50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图所示装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:
50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图所示装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:(1)如果将环形玻璃搅拌棒改为环形金属(如铜)棒,对求得中和热数值的影响是偏低(填“偏高”、“偏低”或“无影响”).
(2)如果改用60mL 1.0mol•L-1盐酸跟50mL 1.1mol•L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量增加(填“增加”、“减少”或“不变”),所求中和热数值不变(填“增加”、“减少”或“不变”);
(3)不能用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,理由是H2SO4与Ba(OH)2反应生成的BaSO4沉淀时也有能量变化(或放热);
(4)该实验小组做了三次实验,每次取溶液各50mL,并记录如表原始数据.
| 实验序号 | 起始温度t1/℃ | 终止温度(t2)℃ | 温差(t2•t1)℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.7 | 6.7 |
| 2 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
| 3 | 25.1 | 25.1 | 25.1 | 32.0 | 6.9 |
(5)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是acd(填字母).
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定HCl溶液的温度.
18.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D是地壳中含量最多的金属元素.下列说法正确的是( )
| A. | 元素C、D、E的最高价氧化物对应的水化物之间两两都可以发生反应 | |
| B. | 1mol由元素A、B组成且含有18 mol e-的化合物只有一种 | |
| C. | 含D元素的盐溶液只能显酸性,不可能显碱性 | |
| D. | 化合物AE与CE含有相同类型的化学键 |
19.向含有a mol NaOH和a mol Ba(OH)2的混合液中通入b mol CO2气体,充分反应后(忽略水解对离子浓度变化的影响),下列说法不正确的是( )
| A. | 当a=b时,发生的离子总反应为:2OH-+CO2+Ba2+═BaCO3↓+H2O | |
| B. | 当3a=2b时,发生的离子总反应为:6OH-+3CO2+2Ba2+═2BaCO3↓+3H2O+CO32- | |
| C. | 当$\frac{3}{2}$a<b<3a时,溶液中含有n(CO32-):n(HCO3-)=(3a-b):(2b-3a) | |
| D. | 当3a=b时,溶液中Na+、Ba2+与HCO3-的物质的量之比为1:1:3 |
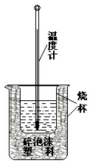 50ml 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如下图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如下图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题: 某化学兴趣小组用如图所示装置电解CuSO4溶液,测定铜的相对原子质量.
某化学兴趣小组用如图所示装置电解CuSO4溶液,测定铜的相对原子质量.