题目内容
10.某化学小组欲通过实验探究:I.苯与液溴发生取代反应;Ⅱ.苯与液溴在催化剂作用下的反应机理.所用装罝如图所示.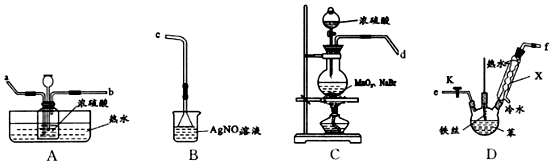
已知:MnO2+2NaBr+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Br2↑+MnSO4+Na2SO4+2H2O
(1)实验室制备溴苯的化学方程式为
 ;仪器X的名称为球形冷凝管.
;仪器X的名称为球形冷凝管.(2)制取溴苯的实验操作步骤如下:
①连接装罝,其接口顺序为(填字母):d接a,b接e,f接c;
②检査装置气密性;
③C中加入固体药品,C处滴加浓硫酸,再打开D处开关K,点燃C处酒精灯;插入铁丝于混合液中,一段时间后,D中液体沸腾,原因是该反应是放热反应;
④关闭C中活塞.
(3)A中对广口瓶进行热水浴的目的是防止Br2蒸气冷凝.
(4)若B中有淡黄色沉淀生成,能否确定苯与液溴发生了取代反应?否(答“能”或“否”).
(5)査阅文献:苯与液溴在FeBr3催化下的反应机理共分三步:
I Br2+FeBr3?Br++FeBr4-
ⅡBr++
 ?
?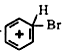
①请完成第三步反应:Ⅲ
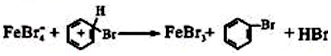 ;
;②该小组将A装置中浓硫酸替换成稀硫酸时实验失败,试从反应机理推测可能原因是有水情况下,无法生成Br+.
分析 c装置发生反应:MnO2+2NaBr+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$Br2↑+MnSO4+Na2SO4+2H2O,制备溴单质,为防止溴蒸汽冷凝,在A中对广口瓶进行热水浴,溴蒸汽在D中与苯发生反应: ,最后在硝酸银中吸收未反应溴蒸汽和溴化氢,防止污染空气,据此分析作答,
,最后在硝酸银中吸收未反应溴蒸汽和溴化氢,防止污染空气,据此分析作答,
(1)实验室用苯和溴在催化剂的作用下反应制备溴苯;
(2)①溴蒸汽由C制备,由d到a进入热水浴防止冷凝,由c到e进入D中反应,在B中吸收尾气,则顺序为d、a、b、e、f、c;
②C中加入固体药品,C处滴加浓硫酸,再打开D处开关K,点燃C处酒精灯,制得溴蒸汽反应;根据该反应是放热反应分析;
(3)为防止Br2蒸气冷凝,A中对广口瓶进行热水浴;
(4)溴蒸汽可与硝酸银反应生成沉淀,B中有淡黄色沉淀生成,不能确定苯与液溴发生了取代反应;
(5))①第三步反应为溴苯的生成,化学反应为: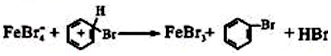 ;
;
②将A装置中浓硫酸替换成稀硫酸时实验失败,有水情况下,无法生成Br+.
解答 解:(1)实验室用苯和溴在催化剂的作用下反应制备溴苯,化学方程式为: ;仪器X为球形冷凝管;
;仪器X为球形冷凝管;
故答案为: ;球形冷凝管;
;球形冷凝管;
(2)①溴蒸汽由C制备,由d到a进入热水浴防止冷凝,由c到e进入D中反应,在B中吸收尾气,则顺序为d、a、b、e、f、c;
故答案为:a;b;e;f;
③C中加入固体药品,C处滴加浓硫酸,再打开D处开关K,点燃C处酒精灯,制得溴蒸汽反应;该反应是放热反应,插入铁丝于混合液中,一段时间后,D中液体沸腾;
故答案为:C处滴加浓硫酸;该反应是放热反应;
(3)为防止Br2蒸气冷凝,A中对广口瓶进行热水浴;
故答案为:防止Br2蒸气冷凝;
(4)溴蒸汽可与硝酸银反应生成沉淀;
故答案为:否;
(5)①第三步反应为溴苯的生成,化学反应为: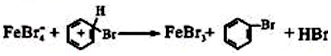 ;
;
故答案为: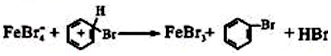 ;
;
②将A装置中浓硫酸替换成稀硫酸时实验失败,有水情况下,无法生成Br+;
故答案为:有水情况下,无法生成Br+.
点评 本题主要考查了溴苯的制备,学生知识综合应用、根据实验目的及物质的性质进行排列顺、实验基本操作能力及实验方案设计能力,综合性较强,注意把握物质性质以及对题目信息的获取于使用,难度中等.

| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 3:1 |
 50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图所示装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:
50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图所示装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:(1)如果将环形玻璃搅拌棒改为环形金属(如铜)棒,对求得中和热数值的影响是偏低(填“偏高”、“偏低”或“无影响”).
(2)如果改用60mL 1.0mol•L-1盐酸跟50mL 1.1mol•L-1氢氧化钠溶液进行反应,则与上述实验相比,所放热量增加(填“增加”、“减少”或“不变”),所求中和热数值不变(填“增加”、“减少”或“不变”);
(3)不能用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,理由是H2SO4与Ba(OH)2反应生成的BaSO4沉淀时也有能量变化(或放热);
(4)该实验小组做了三次实验,每次取溶液各50mL,并记录如表原始数据.
| 实验序号 | 起始温度t1/℃ | 终止温度(t2)℃ | 温差(t2•t1)℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.7 | 6.7 |
| 2 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
| 3 | 25.1 | 25.1 | 25.1 | 32.0 | 6.9 |
(5)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是acd(填字母).
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定HCl溶液的温度.
| A. | 元素C、D、E的最高价氧化物对应的水化物之间两两都可以发生反应 | |
| B. | 1mol由元素A、B组成且含有18 mol e-的化合物只有一种 | |
| C. | 含D元素的盐溶液只能显酸性,不可能显碱性 | |
| D. | 化合物AE与CE含有相同类型的化学键 |
| 选项 | 实验 | 现象 | 结论 |
| A | 向FeSO4溶液中先滴入KSCN 溶液再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+既有氧化性又有还原性 |
| B | 常温下将铜片放入浓硫酸中 | 生成刺激性气味的气体 | 反应生成了SO2 |
| C | 室温下,向浓度均为0.1mol•L-1的BaC12和CaCl2混合溶液中滴加Na2SO4溶液 | 出现白色沉淀 | Ksp(BaSO4)<Ksp(CaSO4) |
| D | 向Ba(NO3)2溶液中通入SO2气体 | 有白色沉淀生成 | 沉淀是BaSO4 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 4种 | B. | 6种 | C. | 7种 | D. | 9种 |
| A. | 当a=b时,发生的离子总反应为:2OH-+CO2+Ba2+═BaCO3↓+H2O | |
| B. | 当3a=2b时,发生的离子总反应为:6OH-+3CO2+2Ba2+═2BaCO3↓+3H2O+CO32- | |
| C. | 当$\frac{3}{2}$a<b<3a时,溶液中含有n(CO32-):n(HCO3-)=(3a-b):(2b-3a) | |
| D. | 当3a=b时,溶液中Na+、Ba2+与HCO3-的物质的量之比为1:1:3 |
| A. | 稀醋酸中加入少量醋酸钠能增大醋酸的电离程度 | |
| B. | 25℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7 | |
| C. | 50℃时,NH4Cl和HCl的混合液中:c(NH4+)+c(H+)=c(OH-)+c(Cl-) | |
| D. | 0.1molAgCl和0.1molAgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |