题目内容
6.下列有关热化学方程式正确的是( )| 已知条件 | 热化学方程式 | |
| A | CH4的燃烧热(△H)为-890kJ• mol-1 | CH4(g)+2O2(g)═CO2(g)+2H2O(g) △H=-890kJ• mol-1 |
| B | 中和热△H=-57.3kJ•mol-1 | CH3COOH(aq)+NaOH(aq)═H2O+CH3COONa (aq)△H=-57.3kJ•mol-1 |
| C | 一定条件下,0.5mol N2与1.5mol H2充分反应后放出30.5kJ的热量 | N2(g)+3H2(g)?2NH3(g)△H=-61kJ•mol-1 |
| D | 96g O2的能量比96g O3的能量低bkJ | 3O2(g)?2O3(g)△H=+bkJ• mol-1 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、1mol纯物质完全燃烧生成稳定的氧化物时放出的热量叫燃烧热;
B、强酸强碱的稀溶液反应只生成1mol液态水时放出的热量叫中和热;
C、可逆反应不能彻底;
D、反应热与化学计量数成正比关系.
解答 解:A、1mol纯物质完全燃烧生成稳定的氧化物时放出的热量叫燃烧热,水应该为液态,故A错误;
B、强酸强碱的稀溶液反应只生成1mol液态水时放出的热量叫中和热,醋酸为弱酸,故B错误;
C、可逆反应不能彻底,0.5mol N2与1.5mol H2充分反应后放出30.5kJ的热量,则1molN2与3mol H2充分反应后放出的热量比61kJ要大,故C错误;
D、反应热与化学计量数成正比关系,反应无总能量比生成物低则为吸热反应,3O2(g)?2O3(g)△H=+bkJ•mol-1,故D正确.
故选:D.
点评 本题考查了化学反应中能量变化的原因、反应热的含义、热化学方程式书写时△H的条件、燃烧热的概念,题目难度不大.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
16.苹果酯的结构简式如图所示,下列说法不正确的是( )
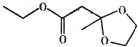

| A. | 苹果酯分子中含有14个氢原子 | |
| B. | 苹果酯能在NaOH溶液中发生水解反应 | |
| C. | 苹果酯能与金属钠反应产生氢气 | |
| D. | 苹果酯与C2H5OOCCH2CH2COOC2H5互为同分异构体 |
17.天然气脱硫的方法有多种,一种是干法脱硫,其涉及的反应:H2(g)+CO(g)+SO2(g)?H2O(g)+CO2(g)+S(s)+Q(Q>0).要提高脱硫率可采取的措施是( )
| A. | 加催化剂 | B. | 分离出硫 | C. | 减压 | D. | 加生石灰 |
1.下列各组中的性质比较,不正确的是( )
| A. | 水溶性:SO2>Cl2>CO2 | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 稳定性:NH3>H2O>HF | D. | 沸点:F2<Cl2<Br2<I2 |
11.在一定温度下的定容密闭容器中,当物质的下列物理量不再变化时.表明反应:A(g)+B(g)?C(g)+D(g)已达平衡的是( )
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | B的物质的量浓度 | D. | 气体的总物质的量 |
18.从矿物学资料查得,当胆矾溶液渗人地下,遇黄铁矿(FeS2)时可生成辉铜矿(Cu2S),同时还生成FeSO4和H2SO4,下列有关叙述中正确的是( )
| A. | 在反应中,FeS2是氧化剂,不是还原剂 | |
| B. | 在反应中,CuSO4是氧化剂,FeS2是还原剂 | |
| C. | 反应中Cu2+与FeS2的物质的量之比是14:5 | |
| D. | 反应中每生成1mol Cu2S共得2mol电子 |
11.常温下,0.05mol•L-1Ba(OH)2溶液的pH为( )
| A. | 13 | B. | 1 | C. | 1.3 | D. | 12.7 |
