题目内容
20.常温下,下列各组离子一定能在指定溶液由大量共存的是( )| A. | 使甲基橙变红色的溶液中:Na+、Fe2+、MnO4-、AlO2- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | pH=0的溶液中:Al3+、Ag(NH3)2+、Cl-、SO42- | |
| D. | 加入Mg能放出H2的溶液中:Ca2+、NH4+、ClO-、NO3- |
分析 A.使甲基橙变红色的溶液,显酸性;
B.$\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液,显酸性;
C.pH=0的溶液,显酸性;
D.加入Mg能放出H2的溶液,溶液显酸性.
解答 解:A.使甲基橙变红色的溶液,显酸性,酸性溶液中不能大量存在AlO2-,且Fe2+、MnO4-发生氧化还原反应,不能共存,故A错误;
B.$\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液,显酸性,该组离子之间不反应,可大量共存,故B正确;
C.pH=0的溶液,显酸性,不能大量存在Ag(NH3)2+,故C错误;
D.加入Mg能放出H2的溶液,溶液显酸性,不能大量存在ClO-,故D错误;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应等为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应及复分解反应,题目难度不大.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
10.下列实验或操作方法正确的是( )
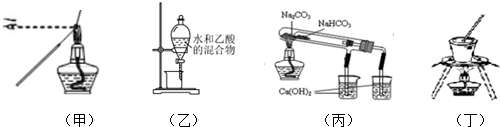

| A. | 甲图装置:用蘸有待测液的铁丝,检验K+ | |
| B. | 乙图装置:分离水和乙酸 | |
| C. | 丙图装置:验证NaHCO3和Na2CO3的热稳定性 | |
| D. | 丁图装置:从食盐水中提取食盐 |
11.能用键能知识加以解释的是( )
| A. | 稀有气体的化学性质很不活泼 | B. | H2O的沸点比H2S高 | ||
| C. | 干冰易升华 | D. | 氮气的化学性质很稳定 |
8.下列说法错误的是( )
| A. | 二氧化碳和环氧丙烷在催化作用下可生成一种可降解的高聚物,可减少二氧化碳对环境的影响 | |
| B. | 化石燃料的燃烧和含硫金属矿石的冶炼等都是造成SO2污染的重要原因 | |
| C. | 氟氯烃的大量使用会破坏臭氧层,火箭、导弹将大量废气排放到高空,也会加速臭氧分解 | |
| D. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 |
2.(1)已知Na2S2O3+H2SO4═Na2SO4+S↓+SO2+H2O.甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如表(所取溶液体积均为10mL):
其他条件不变时:探究浓度对化学反应速率的影响,应选择①②或③④.(填实验编号);探究温度对化学反应速率的影响,应选择①④.(填实验编号).
(2)甲同学设计如图实验流程探究Na2S2O3的化学性质.
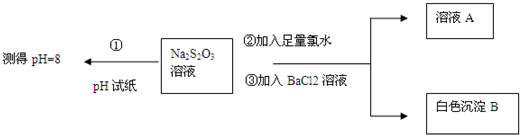
(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和还原 性.
(Ⅱ)生成白色沉淀B的离子方程式是SO42-+Ba2+=BaSO4↓.
(Ⅲ)已知Na2S2O3溶液与Cl2反应时,1mol Na2S2O3转移8mol电子.该反应的离子方程式是S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+.
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.1 | 0.2 |
| ③ | 50 | 0.2 | 0.1 |
| ④ | 50 | 0.1 | 0.1 |
(2)甲同学设计如图实验流程探究Na2S2O3的化学性质.

(Ⅰ)甲同学设计实验流程的目的是证明Na2S2O3溶液具有碱性和还原 性.
(Ⅱ)生成白色沉淀B的离子方程式是SO42-+Ba2+=BaSO4↓.
(Ⅲ)已知Na2S2O3溶液与Cl2反应时,1mol Na2S2O3转移8mol电子.该反应的离子方程式是S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+.
19. 中和滴定是化学定量实验之一.某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白:
中和滴定是化学定量实验之一.某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白:
(1)在中和滴定的过程中有如下操作:①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液 ③检查滴定管是否漏水 ④滴定 ⑤洗涤,则在操作过程中正确的顺序是③⑤①②④.(写序号)
(2)选用的指示剂是b.(a、石蕊 b、甲基橙)
(3)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化.
(4)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是D.
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
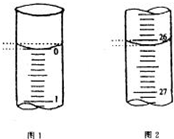
(5)若滴定开始和结束时,酸式滴定管中的液面如图所示,请将数据填入下面表格的空白处.
(6)请根据上表中数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=0.1044mol/L.
(7)滴定终点的判定依据是溶液颜色由黄色突变为橙色,且半分钟内不褪色.
 中和滴定是化学定量实验之一.某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白:
中和滴定是化学定量实验之一.某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,请填写下列空白:(1)在中和滴定的过程中有如下操作:①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液 ③检查滴定管是否漏水 ④滴定 ⑤洗涤,则在操作过程中正确的顺序是③⑤①②④.(写序号)
(2)选用的指示剂是b.(a、石蕊 b、甲基橙)
(3)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化.
(4)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是D.
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(5)若滴定开始和结束时,酸式滴定管中的液面如图所示,请将数据填入下面表格的空白处.
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L 盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | |||
| 第二次 | 25.00 | 2.00 | 28.08 | 26.08 |
| 第三次 | 25.00 | 0.22 | 26.34 | 26.12 |
(7)滴定终点的判定依据是溶液颜色由黄色突变为橙色,且半分钟内不褪色.