题目内容
11.能用键能知识加以解释的是( )| A. | 稀有气体的化学性质很不活泼 | B. | H2O的沸点比H2S高 | ||
| C. | 干冰易升华 | D. | 氮气的化学性质很稳定 |
分析 A.稀有气体分子中不含化学键,稀有气体原子的最外层已经达到稳定结构,所以化学性质很不活泼;
B.沸点与氢键和分子间作用力有关;
C.干冰易升华是因为CO2分子之间的分子间作用力小的缘故;
D.N2分子中含有三键,键能大,所以氮气的化学性质很稳定.
解答 解:A.稀有气体分子中不含化学键,稀有气体原子的最外层已经达到稳定结构,所以化学性质很不活泼,故A错误;
B.含有氢键的沸点较高,分子间作用力越大,沸点越高,水分子间含有氢键沸点较高,与键能无关,故B错误;
C.干冰易升华是因为CO2分子之间的分子间作用力小的缘故,故C错误;
D.N2分子中含有三键,键能大,所以氮气的化学性质很稳定,故D正确;
故选D.
点评 本题考查了键能对物质性质的影响,较为简单,注意稀有气体是单原子分子,不含化学键,干冰升华是物理变化,与化学键无关.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
2.下列指定微粒的数目不相等的是( )
| A. | 钾和镁的次外层电子数 | |
| B. | 等质量的乙烯和丙烯中含有的共用电子对数 | |
| C. | 等体积的CO和NO含有的原子数 | |
| D. | 等物质的量的钠分别在常温下和点燃条件下与氧气反应转移的电子数 |
19.下列不属于有机物的是( )
| A. | CO | B. | CH4 | C. | CH3CH3 | D. | CH2=CH2 |
6.能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一.
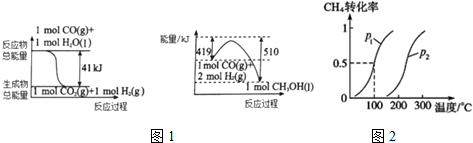
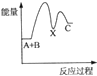
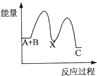
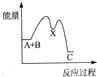
(1)利用工业废气CO2可制取甲醇,已知常温常压下下列反应的能量关系如图1:则CO2与H2反应生成液态CH3OH的热化学方程式为CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-50KJ/mol.
(2)CH4和H2O(g)通过下列转化也可以制得CH3OH:
I.CH4(g)+H2O(g)?CO(g)+3H2(g);△H1>0
Ⅱ.CO(g)+2H2(g)?CH3OH(g);△H2<0
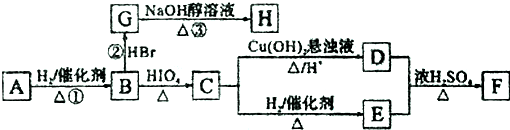
将1.0molCH4和3.0molH2O(g)通入反应室(容积为100L)中,在一定条件下发生反应I,CH4的转化率与温度、压强的关系如图2所示.
①图中的p1<p2(填“<”、“>”或“=”),判断的理由是该反应正方向为体积增大的方向,相同温度下,压强越大甲烷的转化率减小,P2 的转化率比P1小,说明P2<P1.
②若反应Ⅱ在恒容密闭容器进行,下列能判断反应Ⅱ达到平衡状态的是cd(填序号).
a.生成CH3OH的速率与消耗CO的速率相等 b.混合气体的密度不变
c.混合气体的总物质的量不变 d.CH3OH、CO、H2的浓度都不再发生变化
③在某温度下,将一定量的CO和H2投入10L的密闭容器中发生反应II,5min时达到平衡,各物质的物质的浓度(mol•L-1)变化如下表所示:
若5min时只改变了某一条件,则所改变的条件是加了1mol氢气.

(1)利用工业废气CO2可制取甲醇,已知常温常压下下列反应的能量关系如图1:则CO2与H2反应生成液态CH3OH的热化学方程式为CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-50KJ/mol.
(2)CH4和H2O(g)通过下列转化也可以制得CH3OH:
I.CH4(g)+H2O(g)?CO(g)+3H2(g);△H1>0
Ⅱ.CO(g)+2H2(g)?CH3OH(g);△H2<0
将1.0molCH4和3.0molH2O(g)通入反应室(容积为100L)中,在一定条件下发生反应I,CH4的转化率与温度、压强的关系如图2所示.
①图中的p1<p2(填“<”、“>”或“=”),判断的理由是该反应正方向为体积增大的方向,相同温度下,压强越大甲烷的转化率减小,P2 的转化率比P1小,说明P2<P1.
②若反应Ⅱ在恒容密闭容器进行,下列能判断反应Ⅱ达到平衡状态的是cd(填序号).
a.生成CH3OH的速率与消耗CO的速率相等 b.混合气体的密度不变
c.混合气体的总物质的量不变 d.CH3OH、CO、H2的浓度都不再发生变化
③在某温度下,将一定量的CO和H2投入10L的密闭容器中发生反应II,5min时达到平衡,各物质的物质的浓度(mol•L-1)变化如下表所示:
| 2min | 5min | 10min | |
| CO | 0.07 | 0.06 | 0.05 |
| H2 | 0.14 | 0.12 | 0.20 |
| CH3OH | 0.03 | 0.04 | 0.05 |
3.苯分子实际上不具有碳碳单键和碳碳双键的简交替结构,下面是某同学收集的有关事实,其中可以作为证据的有( )
①苯的间位二元取代物只有一种;②苯的邻位二元取代物只有一种;③苯不能使酸性KMnO4溶液褪色;④苯不能与溴水反应.
①苯的间位二元取代物只有一种;②苯的邻位二元取代物只有一种;③苯不能使酸性KMnO4溶液褪色;④苯不能与溴水反应.
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | 全部 |
20.常温下,下列各组离子一定能在指定溶液由大量共存的是( )
| A. | 使甲基橙变红色的溶液中:Na+、Fe2+、MnO4-、AlO2- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | pH=0的溶液中:Al3+、Ag(NH3)2+、Cl-、SO42- | |
| D. | 加入Mg能放出H2的溶液中:Ca2+、NH4+、ClO-、NO3- |
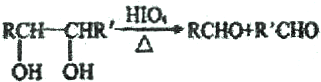 .
.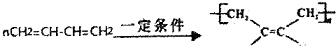 ,若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为CH3CHBrCHBrCH3+2NaOH$→_{△}^{醇}$H3CC≡CCH3↑+2NaBr+2H2O.
,若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为CH3CHBrCHBrCH3+2NaOH$→_{△}^{醇}$H3CC≡CCH3↑+2NaBr+2H2O. .
.