题目内容
15.FeCl3在溶液中分三步水解:Fe3++H2O?Fe(OH)2++H+ K1
Fe(OH)2++H2O?Fe(OH)2++H+ K2
…K3.
①写出第三步水解的离子方程式:Fe(OH)2++H2O?Fe(OH)3+H+,该步水解平衡常数的表达式为K3=$\frac{c({H}^{+})}{c(Fe(OH{)_{2}}^{-})}$.
②K1和K2的大小关系是,理由是K1>K2,第一步水解会抑制第二步水解.
分析 ①FeCl3在溶液中分三步水解:铁离子逐个结合水电离出的氢氧根离子,促进水电离平衡正向进行,平衡常数表达式中固体和纯液体不写入;
②第一步水解显示酸性会抑制第二步水解.
解答 解:①FeCl3在溶液中分三步水解:铁离子逐个结合水电离出的氢氧根离子,促进水电离平衡正向进行,
FeCl3在溶液中分三步水解:
Fe3++H2O?Fe(OH)2++H+ K1
Fe(OH)2++H2O?Fe(OH)2++H+ K2
Fe(OH)2++H2O?Fe(OH)3+H+K3.
平衡常数表达式中固体和纯液体不写入;
第三步的平衡常数为:K3=$\frac{c({H}^{+})}{c(Fe(OH{)_{2}}^{-})}$,
故答案为:Fe(OH)2++H2O?Fe(OH)3+H+;$\frac{c({H}^{+})}{c(Fe(OH{)_{2}}^{-})}$;
②第一步水解显酸性,水解生成的氢离子会抑制第二步水解,K1和K2的大小关系是K1>K2,
故答案为:K1>K2,第一步水解会抑制第二步水解.
点评 本题考查了盐类水解的原理分析,平衡常数书写,注意电离分步进行时逐步减弱,题目较简单.

练习册系列答案
相关题目
6.能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一.
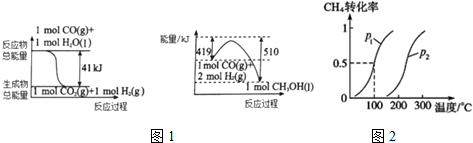
(1)利用工业废气CO2可制取甲醇,已知常温常压下下列反应的能量关系如图1:则CO2与H2反应生成液态CH3OH的热化学方程式为CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-50KJ/mol.
(2)CH4和H2O(g)通过下列转化也可以制得CH3OH:
I.CH4(g)+H2O(g)?CO(g)+3H2(g);△H1>0
Ⅱ.CO(g)+2H2(g)?CH3OH(g);△H2<0
将1.0molCH4和3.0molH2O(g)通入反应室(容积为100L)中,在一定条件下发生反应I,CH4的转化率与温度、压强的关系如图2所示.
①图中的p1<p2(填“<”、“>”或“=”),判断的理由是该反应正方向为体积增大的方向,相同温度下,压强越大甲烷的转化率减小,P2 的转化率比P1小,说明P2<P1.
②若反应Ⅱ在恒容密闭容器进行,下列能判断反应Ⅱ达到平衡状态的是cd(填序号).
a.生成CH3OH的速率与消耗CO的速率相等 b.混合气体的密度不变
c.混合气体的总物质的量不变 d.CH3OH、CO、H2的浓度都不再发生变化
③在某温度下,将一定量的CO和H2投入10L的密闭容器中发生反应II,5min时达到平衡,各物质的物质的浓度(mol•L-1)变化如下表所示:
若5min时只改变了某一条件,则所改变的条件是加了1mol氢气.

(1)利用工业废气CO2可制取甲醇,已知常温常压下下列反应的能量关系如图1:则CO2与H2反应生成液态CH3OH的热化学方程式为CO2(g)+3H2(g)=CH3OH(l)+H2O(l)△H=-50KJ/mol.
(2)CH4和H2O(g)通过下列转化也可以制得CH3OH:
I.CH4(g)+H2O(g)?CO(g)+3H2(g);△H1>0
Ⅱ.CO(g)+2H2(g)?CH3OH(g);△H2<0
将1.0molCH4和3.0molH2O(g)通入反应室(容积为100L)中,在一定条件下发生反应I,CH4的转化率与温度、压强的关系如图2所示.
①图中的p1<p2(填“<”、“>”或“=”),判断的理由是该反应正方向为体积增大的方向,相同温度下,压强越大甲烷的转化率减小,P2 的转化率比P1小,说明P2<P1.
②若反应Ⅱ在恒容密闭容器进行,下列能判断反应Ⅱ达到平衡状态的是cd(填序号).
a.生成CH3OH的速率与消耗CO的速率相等 b.混合气体的密度不变
c.混合气体的总物质的量不变 d.CH3OH、CO、H2的浓度都不再发生变化
③在某温度下,将一定量的CO和H2投入10L的密闭容器中发生反应II,5min时达到平衡,各物质的物质的浓度(mol•L-1)变化如下表所示:
| 2min | 5min | 10min | |
| CO | 0.07 | 0.06 | 0.05 |
| H2 | 0.14 | 0.12 | 0.20 |
| CH3OH | 0.03 | 0.04 | 0.05 |
3.苯分子实际上不具有碳碳单键和碳碳双键的简交替结构,下面是某同学收集的有关事实,其中可以作为证据的有( )
①苯的间位二元取代物只有一种;②苯的邻位二元取代物只有一种;③苯不能使酸性KMnO4溶液褪色;④苯不能与溴水反应.
①苯的间位二元取代物只有一种;②苯的邻位二元取代物只有一种;③苯不能使酸性KMnO4溶液褪色;④苯不能与溴水反应.
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | 全部 |
10.下列说法不正确的是( )
| A. | 天津港爆炸案中对剧毒的氯化钠(NaCN)喷洒双氧水消毒,是利用了双氧水的氧化性 | |
| B. | 碳酸钙分解、氢氧化钡晶体和氧化铵固体反应,高温下铝与氧化铁反应都是吸热反应 | |
| C. | 镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 | |
| D. | 屠呦呦女士利用乙醚萃取青蒿素获得了2015年度诺贝尔生理学或医学奖,为人类防治疟疾作出了重大贡献 |
20.常温下,下列各组离子一定能在指定溶液由大量共存的是( )
| A. | 使甲基橙变红色的溶液中:Na+、Fe2+、MnO4-、AlO2- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | pH=0的溶液中:Al3+、Ag(NH3)2+、Cl-、SO42- | |
| D. | 加入Mg能放出H2的溶液中:Ca2+、NH4+、ClO-、NO3- |
7.下列有关实验原理或实验操作正确的是( )
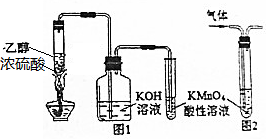

| A. | 用图1所示装置制取乙烯并验证其某些性质 | |
| B. | 用图2装置除去甲烷中的乙烯 | |
| C. | 在坩埚中灼烧CuSO4•5H2O晶体以除去结晶水 | |
| D. | 0.5g淀粉、5mL20%H2SO4和5mL蒸馏水混合,加热5min后冷却,然后向其中加入新制银氨溶液,水浴加热,无银镜反应,说明淀粉没有水解 |
14.某学生欲测定未知物质的量浓度的氢氧化钠溶液:准确称取3.90g烧碱样品,将样品配成250mL待测液,用0.2000mol•L-1标准盐酸滴定待测烧碱溶液选择酚酞作指示剂.请填写下列空白:
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手控制酸式滴定管活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化.直到因加入一滴盐酸,溶液的颜色由红色变为无色,且在半分钟内不变色,即停止滴定.
(2)根据下列数据,计算待测烧碱溶液的浓度:0.4000mol•L-1.
(3)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是DE(填序号).
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出.
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手控制酸式滴定管活塞,右手摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化.直到因加入一滴盐酸,溶液的颜色由红色变为无色,且在半分钟内不变色,即停止滴定.
(2)根据下列数据,计算待测烧碱溶液的浓度:0.4000mol•L-1.
| 滴定次数 | 待测液体积 (mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
| 第三次 | 10.00 | 0.70 | 23.70 |
A.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出.
 .
.
 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2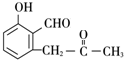 +2H2O.
+2H2O.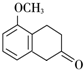 +
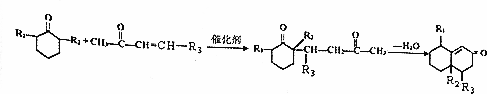
+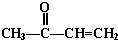 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$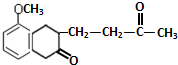 .
.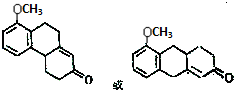 .
.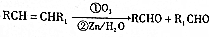 )
)