题目内容
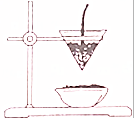 下图为教材铝热反应演示实验示意图
下图为教材铝热反应演示实验示意图(1)引发铝热反应的实验操作是
(2)某同学推测,铝热反应所得到的熔融反应是铁铝合金.理由是:该反应放热能使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金.为此,该同学选用
(3)将红热的铁丝伸入氯气中,可以观察到
考点:探究铝热反应,铁的化学性质,检验三价铁与二价铁
专题:
分析:(1)加少量KClO3,插上Mg条并将其点燃来引发铝热反应;
(2)金属铝能和氢氧化钠反应放出氢气而金属铁和氢氧化钠不反应;
(3)铁丝在氯气中燃烧产生棕红色的烟,可溶性的铁盐溶液呈棕黄色;铁离子部分水解,可加入盐酸抑制铁离子的水解;铁离子与硫氰根离子反应生成硫氰化铁,溶液变成红色;铁离子与氢氧根离子反应生成氢氧化铁沉淀.
(2)金属铝能和氢氧化钠反应放出氢气而金属铁和氢氧化钠不反应;
(3)铁丝在氯气中燃烧产生棕红色的烟,可溶性的铁盐溶液呈棕黄色;铁离子部分水解,可加入盐酸抑制铁离子的水解;铁离子与硫氰根离子反应生成硫氰化铁,溶液变成红色;铁离子与氢氧根离子反应生成氢氧化铁沉淀.
解答:
解:(1)引发铝热反应的操作方法为:加少量KClO3,插上Mg条并将其点燃,
故答案为:(在铝热剂上面)加少量KClO3,插上Mg条并将其点燃;
(2)金属铝能和氢氧化钠反应放出氢气而金属铁和氢氧化钠不反应,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,可以用氢氧化钠溶液证明上述所得的块状熔融物中含有金属铝,操作方法为:取适量冷却后的块状熔融物置于试管中,加入氢氧化钠溶液,现象为:有气体产生,
故答案为:NaOH;
(3)铁丝在氯气中燃烧生成棕红色的烟,为氯化铁固体,氯化铁为可溶性的铁盐,其水溶液呈棕黄色;铁离子在溶液中部分水解,则向反应后的生成物中加入水,得浑浊液,要使其变澄清,可加入少量的盐酸;振荡后分别在两支试管中各倒入适量液体,向其中一支试管滴入KSCN溶液,铁离子与硫氰根离子反应生成络合物硫氰化铁,则观察到溶液呈红色;若向另一支试管中滴入氢氧化钠溶液,铁离子与氢氧化钠反应生成氢氧化铁沉淀,反应的离子方程式为:Fe3++3OH-═Fe(OH)3↓,
故答案为:(剧烈燃烧)产生棕黄色的烟;盐酸;红;Fe3++3OH-═Fe(OH)3↓.
故答案为:(在铝热剂上面)加少量KClO3,插上Mg条并将其点燃;
(2)金属铝能和氢氧化钠反应放出氢气而金属铁和氢氧化钠不反应,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,可以用氢氧化钠溶液证明上述所得的块状熔融物中含有金属铝,操作方法为:取适量冷却后的块状熔融物置于试管中,加入氢氧化钠溶液,现象为:有气体产生,
故答案为:NaOH;
(3)铁丝在氯气中燃烧生成棕红色的烟,为氯化铁固体,氯化铁为可溶性的铁盐,其水溶液呈棕黄色;铁离子在溶液中部分水解,则向反应后的生成物中加入水,得浑浊液,要使其变澄清,可加入少量的盐酸;振荡后分别在两支试管中各倒入适量液体,向其中一支试管滴入KSCN溶液,铁离子与硫氰根离子反应生成络合物硫氰化铁,则观察到溶液呈红色;若向另一支试管中滴入氢氧化钠溶液,铁离子与氢氧化钠反应生成氢氧化铁沉淀,反应的离子方程式为:Fe3++3OH-═Fe(OH)3↓,
故答案为:(剧烈燃烧)产生棕黄色的烟;盐酸;红;Fe3++3OH-═Fe(OH)3↓.
点评:本题考查了常见金属单质及其化合物性质、铝热反应等知识,为常考题型,题目难度中等,注意掌握常见金属单质及其化合物性质,明确铝热反应及其操作方法,能够正确书写常见反应的化学方程式、离子方程式.

练习册系列答案
 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
化学与人类生产、生活、社会可持续发展密切相关,下列说法不正确的是( )
| A、“天宫一号”中使用的碳纤维,是一种新型无机非金属材料 |
| B、为防止富脂食品氧化变质,常在包装袋中放入生石灰 |
| C、开发新能源,减少对化石燃料的依赖,可以促进低碳经济 |
| D、“静电除尘”、“燃烧固硫”、“汽车尾气催化净化”都能提高空气质量 |
短周期元素X、Y、Z、W、U原子序数依次递增.X与W位于同一主族,Z元素的单质既能与盐酸反应也能与NaOH溶液反应,W原子的最外层电子数是次外层电子数的一半,Z、W、U原子的最外层电子数之和为13.Y元素的单质在X的某种氧化物中可燃.下列说法正确的是( )
| A、X、W、U的最高价氧化物对应的水化物酸性由强到弱的顺序为:U>W>X |
| B、Y、Z元素的单质作电极,在NaOH溶液中构成原电池,Z电极上产生大量气泡 |
| C、室温下,0.05 mol/L U的气态氢化物的水溶液的pH>1 |
| D、Y、Z、U元素的简单离子半径由大到小的顺序:Y>Z>U |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、32g O3所含有的原子数为2NA |
| B、18g NH4+中所含的离子数为NA |
| C、22.4LCO2所含的原子数为3NA |
| D、1 mol/L碳酸钠溶液中所含钠离子的总数为2 NA |
下列离子方程式中,正确的是( )
| A、明矾净水原理:Al3++3H2O=Al(OH)3↓+3H+ |
| B、向偏铝酸钠溶液中通入少量的CO2气体 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| C、向澄清石灰水中滴加盐酸 Ca(OH)2+2H+=Ca2++2H2O |
| D、向碳酸氢钙溶液中加入过量的氢氧化钠溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
常温下,下列有关醋酸的叙述中不正确的是( )
| A、Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
| B、将pH=a的醋酸稀释为pH=a+1的过程中,c(OH-)不断增大 |
| C、等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,a+b=14 |
| D、浓度均为0.1 mol-1的CH3COOH溶液和氨水等体积混合后:c(CH3COO-)+c(OH-)=c(NH4+)+c(H+) |
如表是周期表中短周期的一部分,已知B与C的原子序数之和是A原子序数的4倍,则下列说法中正确的是( )
| A | ||
| C | B |
| A、A元素的最高正价为+6价 |
| B、A、B、C依次是氧、氯、磷 |
| C、B元素的单质常温下是一种黄绿色气体 |
| D、C单质常用来制作计算机的芯片 |