题目内容
如表是周期表中短周期的一部分,已知B与C的原子序数之和是A原子序数的4倍,则下列说法中正确的是( )
| A | ||
| C | B |
| A、A元素的最高正价为+6价 |
| B、A、B、C依次是氧、氯、磷 |
| C、B元素的单质常温下是一种黄绿色气体 |
| D、C单质常用来制作计算机的芯片 |
考点:元素周期律和元素周期表的综合应用
专题:
分析:由短周期元素在周期表中位置,可A处于第二周期,B、C处于第三周期,已知B与C的原子序数之和是A原子序数的4倍,设A的原子序数x,则B的原子序数为x+7、C的原子序数为x+9,则:x+7+x+9=4x,解得:x=8,则A为O元素、B为Cl元素、C为P元素,据此对各选项进行判断.
解答:
解:根据图示可知,可A处于第二周期,B、C处于第三周期,已知B与C的原子序数之和是A原子序数的4倍,设A的原子序数x,则B的原子序数为x+7、C的原子序数为x+9,则:x+7+x+9=4x,解得:x=8,则A为O元素、B为Cl元素、C为P元素,
A.A为O元素,氧元素没有正化合价,故A错误;
B.根据分析可知,A、B、C依次是氧、氯、磷元素,故B正确;
C.B为Cl元素,Cl常温下单质为黄绿色的氯气,故C正确;
D.C为P,而常用来制作计算机的芯片的为Si单质,故D错误;
故选BC.
A.A为O元素,氧元素没有正化合价,故A错误;
B.根据分析可知,A、B、C依次是氧、氯、磷元素,故B正确;
C.B为Cl元素,Cl常温下单质为黄绿色的氯气,故C正确;
D.C为P,而常用来制作计算机的芯片的为Si单质,故D错误;
故选BC.
点评:本题考查了元素周期律与元素周期表的应用,题目难度中等,根据题干信息正确推断各元素名称为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
 瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图所示,有关说法正确的是( )
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图所示,有关说法正确的是( )| A、电极2发生氧化反应 |
| B、电池工作时,Na+向负极移动 |
| C、电流由电极1经外电路流向电极2 |
| D、电极1发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O |
将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积可能是( )
| A、1.5mL | B、2.4mL |
| C、3.6mL | D、4mL |
用98%浓硫酸配制200mL 0.5mol.L-1的硫酸溶液,一定需要使用的玻璃仪器是( )
①玻璃棒 ②烧杯 ③烧瓶 ④量筒 ⑤漏斗.
①玻璃棒 ②烧杯 ③烧瓶 ④量筒 ⑤漏斗.
| A、①②③ | B、①②④ |
| C、②③⑤ | D、③④⑤ |
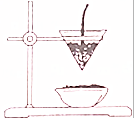 下图为教材铝热反应演示实验示意图
下图为教材铝热反应演示实验示意图
