题目内容
短周期元素X、Y、Z、W、U原子序数依次递增.X与W位于同一主族,Z元素的单质既能与盐酸反应也能与NaOH溶液反应,W原子的最外层电子数是次外层电子数的一半,Z、W、U原子的最外层电子数之和为13.Y元素的单质在X的某种氧化物中可燃.下列说法正确的是( )
| A、X、W、U的最高价氧化物对应的水化物酸性由强到弱的顺序为:U>W>X |
| B、Y、Z元素的单质作电极,在NaOH溶液中构成原电池,Z电极上产生大量气泡 |
| C、室温下,0.05 mol/L U的气态氢化物的水溶液的pH>1 |
| D、Y、Z、U元素的简单离子半径由大到小的顺序:Y>Z>U |
考点:原子结构与元素的性质,原子结构与元素周期律的关系
专题:
分析:X、Y、Z、W、U是分别位于短周期的元素,原子序数依次递增.Z元素的单质既能与盐酸反应也能与NaOH溶液反应,则Z为Al;W原子的最外层电子数是次外层电子数的一半,其原子序数至少大于4,W只能处于第三周期,最外层电子数为4,则W为Si;X与W位于同一主族,则X为C元素;Y元素的单质在X的某种氧化物中可燃,可推知Y为Mg;Z、W、U原子的最外层电子数之和为13,U原子最外层电子数=13-3-4=6,结合原子序数可知,U为S元素,据此解答.
解答:
解:X、Y、Z、W、U是分别位于短周期的元素,原子序数依次递增.Z元素的单质既能与盐酸反应也能与NaOH溶液反应,则Z为Al;W原子的最外层电子数是次外层电子数的一半,其原子序数至少大于4,W只能处于第三周期,最外层电子数为4,则W为Si;X与W位于同一主族,则X为C元素;Y元素的单质在X的某种氧化物中可燃,可推知Y为Mg;Z、W、U原子的最外层电子数之和为13,U原子最外层电子数=13-3-4=6,结合原子序数可知,U为S元素,
A.X、W、U的最高价氧化物对应的水化物分别为碳酸、硅酸、硫酸,则酸性U>X>W,故A错误;
B.Y为Mg,Z为Al,Mg、Al作电极,在NaOH溶液中构成原电池,Mg电极上产生大量气泡,故B错误;
C.U为硫,其氢化物的为弱酸,在溶液中部分电离,则0.05 mol/L H2S的水溶液的pH>1,故C正确;
D.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2->Mg2+>Al3+,故D错误,
故选C.
A.X、W、U的最高价氧化物对应的水化物分别为碳酸、硅酸、硫酸,则酸性U>X>W,故A错误;
B.Y为Mg,Z为Al,Mg、Al作电极,在NaOH溶液中构成原电池,Mg电极上产生大量气泡,故B错误;
C.U为硫,其氢化物的为弱酸,在溶液中部分电离,则0.05 mol/L H2S的水溶液的pH>1,故C正确;
D.电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2->Mg2+>Al3+,故D错误,
故选C.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,题目难度中等,注意对基础知识的全面掌握,侧重于考查学生的分析能力和对基础知识的应用能力.

练习册系列答案
相关题目
下列有关盐酸的说法中正确的是( )
| A、纯净的盐酸是纯净物 |
| B、盐酸就是液态氯化氢 |
| C、盐酸中所有阳离子所带的正电荷数与所有阴离子所带的负电荷数相等 |
| D、浓盐酸有腐蚀性,稀盐酸没有腐蚀性 |
 瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图所示,有关说法正确的是( )
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图所示,有关说法正确的是( )| A、电极2发生氧化反应 |
| B、电池工作时,Na+向负极移动 |
| C、电流由电极1经外电路流向电极2 |
| D、电极1发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O |
下列各图中,表示正反应是吸热反应的图是( )
A、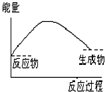 |
B、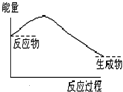 |
C、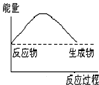 |
D、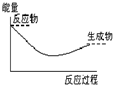 |
今有NH3、O2、NO2在标准状况下的混合气体20.16L,通过稀硫酸后,溶液质量增加了34.1g,气体缩小至2.24L(标况下),将余烬木条插入其中,木条不复燃,则原混合气中NH3、O2、NO2物质的量比为( )
| A、1:1:7 |
| B、2:2:5 |
| C、3:1:4 |
| D、5:2:2 |
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、1 mol AlCl3在熔融状态时离子总数为0.4NA |
| B、标准状况下,2.24L苯中含有的C-H键的数目为0.6NA |
| C、2.2g分子式为 2H218O的水中含有的中子数为1.2 NA |
| D、电解饱和食盐水时,当阴极产生H2 22.4L时,电路中转移的电子数为2NA |
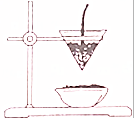 下图为教材铝热反应演示实验示意图
下图为教材铝热反应演示实验示意图