题目内容
7.下列离子反应方程式正确的是( )| A. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | 将金属Na加入冷水中:2 Na+2 H2O═2 Na++2 OH-+H2↑ | |
| C. | 盐酸滴入澄清石灰水:Ca(OH)2+2 H+═Ca2++2 H2O | |
| D. | 澄清石灰水吸收氯气:Cl2+OH-═Cl-+ClO-+H+ |
分析 A.电荷不守恒;
B.钠与水反应生成氢氧化钠和氢气;
C.澄清石灰水中氢氧化钙应拆成离子形式;
D.氯气与氢氧化钙溶液反应生成氯化钙、次氯酸钙和水.
解答 解:A.铜片插入硝酸银溶液中,离子方程式:Cu+2Ag+═Cu2++2Ag,故A错误;
B.将金属Na加入冷水中,离子方程式:2 Na+2 H2O═2 Na++2 OH-+H2↑,故B正确;
C.盐酸滴入澄清石灰水,离子方程式:OH-+H+═H2O,故C错误;
D.澄清石灰水吸收氯气,离子方程式:Cl2+2OH-═Cl-+ClO-+H2O,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确离子方程式书写方法及离子反应实质是解题关键,注意离子反应遵循客观事实、遵循原子个数、电荷数守恒规律,注意化学式的拆分,题目难度不大.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
18.下列离子方程式正确的是( )
| A. | 向盐酸中滴加氨水:H++OH-═H2O | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| C. | 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O═2SO32-+4Cl-+6H+ | |
| D. | 铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2 NO↑+4H2O |
15.下列说法正确的是( )
| A. | 一定温度下,反应 MgCl2(l)═Mg(l)+Cl2(g)的△H>0、△S>0 | |
| B. | 放热反应的反应速率总是大于吸热反应的反应速率 | |
| C. | 在H2S溶液中,C(H+)和C(S2-)的比值为2:1 | |
| D. | 1 mol/L和0.1 mol/L的两瓶氨水中c(OH-)之比为10:1 |
2.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 在常温常压下,11.2 L氧气所含的分子数为0.5NA | |
| B. | 在常温常压下,1molHe的体积为22.4 L | |
| C. | 32 g氧气所含的原子数目为2NA | |
| D. | 在同温同压下,相同体积的任何气体所含的原子数相等 |
19.甲烷和氯气的混合气体在光照条件下发生反应,生成氯化氢、一氯甲烷、二氯甲烷、三氯甲烷和四氯甲烷.下列有关说法正确的是( )
| A. | 该反应既是取代反应又是置换反应 | |
| B. | 一氯甲烷的电子式是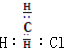 | |
| C. | 二氯甲烷分子有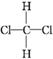 和 和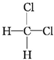 两种空间结构 两种空间结构 | |
| D. | 三氯甲烷和四氯甲烷是工业上重要的溶剂 |
10.常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通CO2气体,只能生成HX和NaHCO3;往NaY溶液中通入CO2则生成HY和Na2CO3.有关叙述正确的是( )
| A. | 结合H+的能力:Y>CO${\;}_{3}^{2-}$>X>HCO${\;}_{3}^{-}$ | |
| B. | 三种酸的电离常数Ki(HX)>Ki(HY)>Ki(H2CO3) | |
| C. | 溶液碱性:NaX>Na2CO3>NaY>NaHCO3 | |
| D. | NaX溶液中通入足量CO2后的离子浓度:c(Na+)>c(HCO${\;}_{3}^{-}$)>c (X)>c(OH)>c(H+) |
 .
.