题目内容
17.(1)除去KCl溶液的K2CO3所用的试剂是盐酸,离子方程式为2H++CO32-=H2O+CO2↑.(2)除去Na2CO3粉末中混入的NaHCO3杂质用加热方法,化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)除去铁粉中混有铝粉的试剂是氢氧化钠溶液,离子方程式为2Al+2OH-+2H2O=2AlO2-+H2↑.
分析 (1)除去杂质K2CO3,还不能引进杂质,可选适量稀盐酸为除杂试剂;
(2)碳酸氢钠加热分解生成碳酸钠、二氧化碳气体和水,据此可除去碳酸钠中混有的碳酸氢钠;
(3)铝能够与氢氧化钠溶液反应,而铁不反应,可用氢氧化钠溶液做除杂试剂.
解答 解:(1)可用稀盐酸除去KCl溶液的K2CO3杂质,反应的离子方程式为:2H++CO32-=H2O+CO2↑,故答案为:盐酸;2H++CO32-=H2O+CO2↑;
(2)可通过加热的方法除去Na2CO3粉末中混入的NaHCO3杂质,反应的化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,故答案为:加热;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(3)可用氢氧化钠溶液除去铁粉中混有铝粉,反应的撩蜂吃螫为:2Al+2OH-+2H2O=2AlO2-+H2↑,故答案为:氢氧化钠溶液;2Al+2OH-+2H2O=2AlO2-+H2↑.
点评 本题考查了离子方程式书写、物质的分离与提纯方法,题目难度中等,明确离子方程式的书写原则为解答关键,注意掌握除杂试剂的选用方法,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
7.下列各组离子能大量共存的是( )
| A. | H+、Na+、HCO3-、Cl- | B. | Fe3+、SCN-、Cl-、NO3- | ||
| C. | Mg2+、Cu2+、SO42-、NO3- | D. | Fe2+、SO42-、H+、NO3- |
8.某温度下将Cl2通入KOH溶液里,反应后得到KCI、KC1O、KC1O3的混合溶液,经测定ClO- 与ClO3-的物质的量浓度之比为11:1,则C12与KOH反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )
| A. | 1:3 | B. | 4:3 | C. | 2:1 | D. | 3:4 |
5.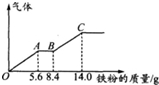 -定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
-定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
 -定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
-定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )| A. | NO,1.5mol/L | B. | H2,1.5mol/L | C. | NO,2.5mol/L | D. | H2,2.5mol/L |
12.0.3mol硫化亚铜跟适量硝酸恰好完全反应.反应方程式为:3Cu2S+22HNO3═6Cu(NO3)2+3H2SO4+10NO+8H2O,则反应中未被还原的硝酸的物质的量为( )
| A. | 2.2mol | B. | 1.2mol | C. | 0.6mol | D. | 1.0mol |
2.下列各组微粒的空间构型相同的是( )
①NH3和H2O
②NH4+和H3O+
③NH3和H3O+
④O3和SO2
⑤CO2和BeCl2
⑥NH4+和SO42-
⑦BF3和Al2Cl6.
①NH3和H2O
②NH4+和H3O+
③NH3和H3O+
④O3和SO2
⑤CO2和BeCl2
⑥NH4+和SO42-
⑦BF3和Al2Cl6.
| A. | 全部 | B. | 除④⑥⑦以外 | C. | ③④⑤⑥ | D. | ②⑤⑥ |
9.设NA代表阿伏加德罗常数,下列说法中正确的是( )
| A. | 100mL1mol/L的碳酸钠溶液中含有CO32-为1NA | |
| B. | 常温、常压下,0.5mol臭氧中含有氧原子为1.5NA | |
| C. | 标准状况下,1mol NO2气体与水反应生成NO3-为NA | |
| D. | 78gNa2O2中含有O2-为2NA |
7.下列离子反应方程式正确的是( )
| A. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | 将金属Na加入冷水中:2 Na+2 H2O═2 Na++2 OH-+H2↑ | |
| C. | 盐酸滴入澄清石灰水:Ca(OH)2+2 H+═Ca2++2 H2O | |
| D. | 澄清石灰水吸收氯气:Cl2+OH-═Cl-+ClO-+H+ |