题目内容
16.NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控.(1)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示.
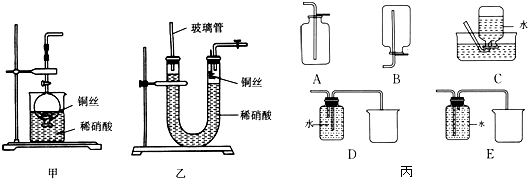
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是CD(填字母).
A.铁B.铝C.铂D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是2NO+O2=2NO2(填化学方程式).
(2)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO.反应开始后,可以在U形管右端观察到无色的NO气体.
①长玻璃管的作用是防止稀硝酸溢出.
②让反应停止的操作方法及原因是关闭U形管右端导气管上的活塞,反应产生的气体将U形管右端内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止.
(3)以下收集NO气体的装置(图丙),合理的是C、D(填选项代号).
(4)假设实验中12.8 g Cu全部溶解,需要通入标况下2.24LO2才能使NO全部溶于水.
分析 (1)①由题意可知,这种成分不能与稀硝酸反应,而Fe、Al均与硝酸反应;
②反应生成的NO被空气中的氧气氧化为二氧化氮;
(2)为了证明产生的气体是NO,则该实验装置要防止产生的气体与空气接触,长玻璃管的作用是防止稀硝酸溢出;关闭活塞,产生的气体使稀硝酸液面下降,从而使铜丝与稀硝酸分开,反应停止.
(3)NO能与空气中的氧气反应,故不能用排空气法来收集NO,只能用排水法,C和D装置符合题意,E装置是洗气装置.
(4)由反应过程可知,铜失去的电子数与O2得到的电子数相等,以此计算.
解答 解:(1)①由题意可知,这种成分不能与稀硝酸反应,而Fe、Al均与硝酸反应,所以AB不行,故答案为:CD;
②反应生成的NO被空气中的氧气氧化为二氧化氮,呈红棕色,发生反应为2NO+O2=2NO2,故答案为:2NO+O2=2NO2;
(2)为了证明产生的气体是NO,则该实验装置要防止产生的气体与空气接触,长玻璃管的作用是防止稀硝酸溢出;关闭活塞,产生的气体使稀硝酸液面下降,从而使铜丝与稀硝酸分开,反应停止,
故答案为:防止稀硝酸溢出;关闭U形管右端导气管上的活塞,反应产生的气体将U形管右端内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止;
(3)NO能与空气中的氧气反应,故不能用排空气法来收集NO,只能用排水法,C和D装置符合题意,E装置是洗气装置,故答案为:C、D;
(4)由反应过程可知,铜失去的电子数与O2得到的电子数相等,则有n(O2)=$\frac{1}{2}$(Cu)=0.1 mol,V(O2)=2.24 L,故答案为:2.24L.
点评 本题考查性质实验方案的设计,为高频考点,把握物质的性质、实验装置的作用、性质实验分析是解题关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
7.下列离子反应方程式正确的是( )
| A. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | 将金属Na加入冷水中:2 Na+2 H2O═2 Na++2 OH-+H2↑ | |
| C. | 盐酸滴入澄清石灰水:Ca(OH)2+2 H+═Ca2++2 H2O | |
| D. | 澄清石灰水吸收氯气:Cl2+OH-═Cl-+ClO-+H+ |
4.下列说法中不正确的是( )
| A. | 标准状况下,1.12 L的H2O所含的原子数必大于1.5×6.02×1023 | |
| B. | 含有相同氧原子数的SO2和CO2的物质的量相等 | |
| C. | 常温常压下,48 g O3中含有的氧原子数为3NA | |
| D. | 标准状况下,2.24 L NH3和CH4的混合气体,所含电子总数为2NA |
11.下列说法正确的是( )
| A. | 乙炔和苯均为不饱和烃,都只能发生加成反应 | |
| B. | 加新制的Cu(OH)2悬浊液并加热可检验尿液中的葡萄糖 | |
| C. | 油脂在酸的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| D. | 可以用蛋白质的焰色反应,来鉴别部分蛋白质 |
19.下列反应中,NH3既显还原性,又显碱性的是( )
| A. | NH3+HCl═NH4Cl | B. | 4NH3+5O2$\frac{\underline{\;Pt\;}}{△}$4NO+6H2O | ||
| C. | 3CuO+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O | D. | 8NH3+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$6NH4Cl+N2 |
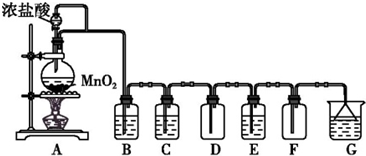
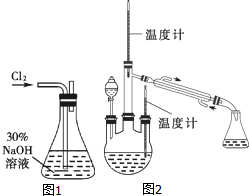 肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl
肼是重要的化工原料.某探究小组利用下列反应制取水合肼(N2H4•H2O).CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4•H2O+NaCl