题目内容
18.2001年美国科学家宣布他们发现了核电荷数为116的元素,试推断该元素在元素周期表中的位置为七周期第ⅥA族,若已知该元素原子核内有155个中子,则其质量数为271.分析 核电荷数为116的元素,七个电子层,最外层只有6个电子,是第七周期,第ⅥA族,质量数为中子数和质子数,由此分析解答.
解答 解:核电荷数为116的元素,七个电子层,最外层只有6个电子,是第七周期,第ⅥA族,质量数=中子数+质子数=116+155=271,
故答案为:七;第ⅥA;271.
点评 本题考查了质量数、质子数和中子数之间的关系等知识点,难度不大,明确:质量数为中子数和质子数.

练习册系列答案
相关题目
12.碳、硫、氧、氮是中学常见元素,下列说法不正确的是 ( )
| A. | CO2、SO2、NH3都是直线形分子 | |
| B. | CO2、NH3、H2S 的键角依次减小 | |
| C. | H2O2、N2H4分子的中心原子都是 sp3杂化 | |
| D. | C、N、F元素的电负性依次增大 |
9. X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)Y位于元素周期表第三周期第VIA族,Y和Z的最高价氧化物对应的水化物的酸性较强的是HClO4(写化学式).
(2)XY2是一种常用的溶剂,XY2的分子中存在2个σ键.在H-Y、H-Z两种共价键中,键的极性较强的是H-Cl,键长较长的是H-S.
(3)W的基态原子价电子排布式是3d104s1.
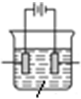
工业上以W2Y为原料制备W的化学方程式为Cu2S+2O2$\frac{\underline{\;高温\;}}{\;}$2Cu+2SO2 ,通过该方法冶炼得到的W的单质含有锌、铁、镍、银、金等杂质,除去这些杂质常用的方法叫电解精炼,请标出右图所示装置中电极材料名称及电解质溶液名称.
(4)W形成的氧化物W2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有16个W原子.
 X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(2)XY2是一种常用的溶剂,XY2的分子中存在2个σ键.在H-Y、H-Z两种共价键中,键的极性较强的是H-Cl,键长较长的是H-S.
(3)W的基态原子价电子排布式是3d104s1.
工业上以W2Y为原料制备W的化学方程式为Cu2S+2O2$\frac{\underline{\;高温\;}}{\;}$2Cu+2SO2 ,通过该方法冶炼得到的W的单质含有锌、铁、镍、银、金等杂质,除去这些杂质常用的方法叫电解精炼,请标出右图所示装置中电极材料名称及电解质溶液名称.
(4)W形成的氧化物W2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有16个W原子.
10.关于电化学的下列说法正确的是( )


| A. | 工业上用电解MgCl2溶液的方法冶炼Mg | |
| B. | 钢铁发生吸氧腐蚀的正极反应式为4OH--4e-═O2↑+2H2O | |
| C. | 如图中发生反应的方程式为:Fe+2H+=Fe2++H2↑ | |
| D. | 碱性锌锰干电池放电时的正极反应为:MnO2+H2O+e-=MnOOH+OH- |
7.下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是( )
| A. | 金刚石和晶体硅 | B. | CO2和SiO2 | C. | KCl和HBr | D. | NaOH和NaCl |
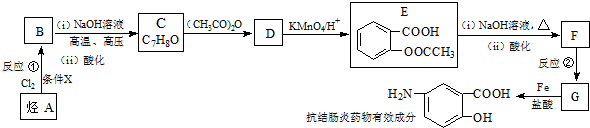
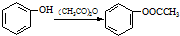
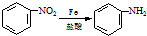
 ;反应①的反应条件是FeCl3作催化剂;反应②的反应类型是取代反应;
;反应①的反应条件是FeCl3作催化剂;反应②的反应类型是取代反应; ;
;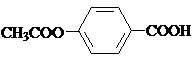 ,
, ;
;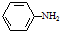 )易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此按先后顺序写出以A为原料合成邻氨基苯甲酸(
)易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此按先后顺序写出以A为原料合成邻氨基苯甲酸(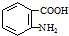 )合成路线中两种中间产物的结构简式(部分反应条件已略去)
)合成路线中两种中间产物的结构简式(部分反应条件已略去)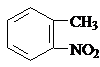 ,
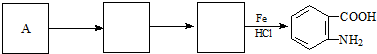
,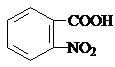 .
.
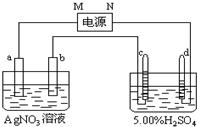
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题: