题目内容
7.下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是( )| A. | 金刚石和晶体硅 | B. | CO2和SiO2 | C. | KCl和HBr | D. | NaOH和NaCl |
分析 根据晶体的类型和所含化学键的类型分析,离子化合物含有离子键,可能含有共价键,共价化合物只含共价键,双原子分子或多原子分子含有共价键.
解答 解:A、金刚石和晶体硅都只含共价键的原子晶体,所以化学键类型相同,晶体类型也相同,故A正确;
B、固体CO2是分子晶体,SiO2只原子晶体,晶体类型不同,故B错误;
C、KCl是离子晶体,KCl中只含离子键,固体HBr分子晶体,HBr中只含共价键,故C错误;
D、NaOH是离子晶体,NaOH中既含离子键又含共价键,NaCl是离子晶体,NaCl中只含离子键,故D错误;
故选:A.
点评 本题考察了化学键类型和晶体类型的关系.判断依据为:离子晶体中阴阳离子以离子键结合,原子晶体中原子以共价键结合,分子晶体中分子之间以范德华力结合,分子内部存在化学键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4═2CuI↓+13I2+12K2SO4+12H2O,下列描述正确的是( )
| A. | I2仅是还原产物 | |
| B. | Cu(IO3)2既是氧化剂又是还原剂 | |
| C. | 氧化产物与还原产物物质的量比为13:2 | |
| D. | 当1 mol氧化剂参加反应时,被氧化的物质的物质的量为11mol |
12.关于氢键的下列说法中正确的是( )
| A. | 每个水分子内含有两个氢键 | |
| B. | 只要有氢元素就能形成氢键 | |
| C. | 分子间能形成氢键使物质的熔点和沸点升高 | |
| D. | HF的稳定性很强,是因为其分子间能形成氢键 |
19.某卤代烃与氢氧化钠的醇溶液在加热条件下反应产生丙烯,将剩余的溶液用硝酸酸化后,加入硝酸银溶液生成浅黄色沉淀.则原卤代烃的结构简式可能是( )
| A. | CH3CH2CH2-Cl | B. | 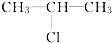 | C. | CH3CH2CH2-Br | D. | 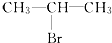 |
16.25℃时,常见的无机酸在水溶液中的电离子平衡常数如表,下列选项正确的是( )
| 氢氰酸(HCN) | 碳酸(H2C03) | 氢氟酸(HF) |
| K=4.9×10-10 | K1=4.4×10-7 K2=4.7×10-11 | K=6.61×10-4 |
| A. | 氰化钠溶液中通入少量CO2:2CN-+H2O+CO2═2HCN+CO32- | |
| B. | NaCN与HCN的混合溶液中一定有:c(Na+)>c(CN-)>c(HCN)>c(H+)>c(OH+) | |
| C. | 0.2 mol•L-1 HCN溶液与0.1mol•L-1NaOH溶液等体积混合后,溶液中各种离子的浓度关系有:2[c(H+)-c(OH+)]=c(CN+)-c(HCN) | |
| D. | 等体积、等浓度的NaCN和NaF溶液中所含离子总数前者大于后者 |
17.室温下,用0.10mol•L-1盐酸分别滴定20.00mL 0.10mol•L-1氢氧化钠溶液和氨水,滴定过程中溶液pH随加入盐酸体积V(HCl)的变化关系如图.下列说法不正确的是( )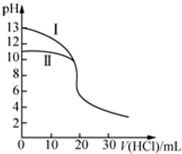

| A. | Ⅱ表示的是滴定氨水的曲线,当V(HCl)=20 mL时:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 当pH=7时,滴定氨水消耗的V(HCl)<20 mL,且c(NH4+)=c(Cl-) | |
| C. | 滴定氢氧化钠溶液时,若V(HCl)>20 mL,则一定有:c(Cl-)>c(Na+)>c(H+)>c(OH-) | |
| D. | 当滴定氨水消耗V(HCl)=10 mL时,有:2[c(OH-)-c(H+)]=c(NH4+)-c(NH3•H2O) |
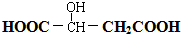 . 请回答:
. 请回答: .
.